US Pharm. 2016;41(12):HS16-HS19.
要旨:大麻(カンナビス)は一般的に副作用のない良性物質と考えられているが,カンナビノイド充血症候群(CHS)は大麻の慢性使用の後遺症である. 臨床医は、難治性の吐き気および嘔吐を呈し、その症状が温水浴で緩和される長期大麻使用者においては、CHSを強く疑うべきである。 制吐剤が効かない場合は、CHSの診断に役立つはずである。 CHSを成功裏に解決する唯一の治療は、大麻の断薬であるが、ハロペリドールは潜在的な治療選択肢として研究されている。
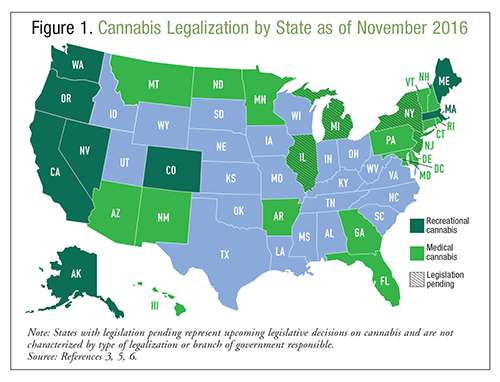
大麻(カンナビス)は、カンナビス・サティバとして知られる麻の植物から得られる天然産物で、一般に副作用のない良性の物質と考えられています。1 大麻は中毒や治療のために喫煙、気化、摂取され、これらの目的のために何世紀も前から使用されてきました。 2014年の薬物使用と健康に関する全国調査によると、>2200 万人のアメリカ人が前月に大麻を使用し、この物質は最もよく使用される違法薬物となっています。2 米国では、合法化率が高まっており、大麻の使用は今後も増加すると予測されています3。 アルコール関連疾患に関する全国疫学調査によると、医療用大麻を合法化している州の住民は、合法化していない州の住民に比べて、大麻の使用を支持する傾向が2倍ある4。現在、28州で医療用として、また8州で娯楽用として大麻を使用することが可能である。 図1参照)3,5,6 合法化に加え、21州とコロンビア特別区では、少量の大麻所持を非犯罪化している。 大麻使用に関連する医療緊急事態は、2009年から2011年にかけて29%増加しましたが、この増加の原因が大麻の効能によるものか、合法化の進展によるものか、その他の要因によるものかは不明です(1)。
人間の体にはエンドカンナビノイド系として知られる固有のカンナビノイド系があり、食欲、睡眠、痛み、感情、運動を調節する神経伝達物質(すなわちアナンダマイド)が含まれています7、8 カンナビノイドとは、体内のカンナビノイド受容体に影響を与えるあらゆる化合物を指しています。 治療目的の受容体には、カンナビノイド1型および2型(CB1、CB2)があります。 CB1は脳に大量に存在し、脊髄や末梢神経組織にはそれほど多くありませんが、CB2は末梢組織や免疫系に大量に存在します8。 大麻に含まれる他のカンナビノイドには、カンナビジオールやカンナビゲロールがあり、これらは精神作用はありません。 内在系が影響を及ぼす活動は多岐にわたるため、多くの人がカンナビノイドを中毒や治療目的で使用してきました。
カンナビノイド充血症候群
大麻は、HIV/AIDSに伴う食欲不振や消耗の治療における食欲増進、化学療法による吐き気・嘔吐を緩和するために使用されてきました。 大麻は吐き気や嘔吐の治療に使用されることがありますが、カンナビノイド充血症候群(CHS)として知られる逆説的な吐き気や嘔吐の症候群を引き起こす可能性もあります。 CHSは、慢性的な大麻の使用を特徴とする臨床診断です。9 CHSの特徴は、周期的な吐き気と嘔吐で、標準的な制吐療法には反応しないものの、強制的な温浴には反応する場合があります3、9 CHSを記録した最初のケースレポート(2004)は、オーストラリアで9人の患者について記述しています。 発症前に大麻を慢性的に使用しており、症状には吐き気と嘔吐が含まれていました。 ほとんどの患者は、症状を緩和するために熱いお湯で入浴していたと報告しています。
コロラド州では、大麻が合法化された2009年以降、CHSの割合は2倍に増加しています3。しかし、CHSは臨床医に認識されないことが多く、その結果、患者の検査が広範囲に及び、費用がかかることに注意が必要です。 CHSの診断は困難であり、周期性嘔吐症候群(CVS)を含む他の多くの疾患と誤診される可能性があります。 大麻を使用する患者の中にはCVSを呈する者もいるが、CVSとCHSの間にはいくつかの鑑別因子が存在する。 CVSは通常、片頭痛の個人歴または家族歴、精神障害の既往、強迫性温浴の欠如を伴う。11 CHS患者はしばしば、症状のために救急部(ED)を受診している。 Soriano-Coらによる症例報告では、CHSと診断された患者は、頻繁に臨床医を訪れ、救急外来を受診し、入院する傾向があることが示されています。12 平均すると、CHSと診断されるまでに5回の臨床医訪問、7回の救急外来受診、3回の入院を経験しており、どの医療環境においてもCHS患者が見られることが示されています12 さらに診断を複雑にするのがK2(別名スパイス)などの人工カナビノイドで、尿中薬物検査では検出できません13。 CHS は、吐き気や嘔吐を引き起こす他の疾患と区別する必要があり、診断は一般に除外の対象となります。
病態生理学
CHSの病態生理学については複数の仮説がありますが、大麻には多数の活性物質があり、さまざまな作用点があるため、明確な病態生理学的プロセスは不明となっています。
低用量ではTHCは制吐作用を示すことが知られていますが、大量かつ慢性的な大麻の使用では、逆の作用が見られるとされています。 THCは分布量が多いため、時間とともに蓄積されることが示唆されている。 THCは、腸管神経系のCB1受容体を直接活性化し、胃の運動性を低下させ、過剰な活性化により吐き気や嘔吐のリスクを高める可能性がある。9 THCの作用と構造の両方を模倣した合成カンナビノイドは、その強力な作動薬効果によりCB1受容体の過剰刺激を引き起こすと推測される14。 これらのCB1受容体は視床下部にも存在し、体温調節を損なうことで嘔吐を誘発し、温浴による症状の緩和をもたらす可能性がある。
危険因子、臨床経過、診断
大麻の慢性使用はCHS発症の主要危険因子である。 9 大麻の日常的な使用は、頻度の低い使用よりもCHSを引き起こしやすいようだが、大麻の量はCHSにつながりうる。15
CHSにはいくつかの段階があり、前嘔吐、催吐、回復として分類されている9、16 前嘔吐期は数か月から数年間続くことがあり、吐き気、嘔吐への恐怖、腹部不快感によって特徴づけられる。 一般に、大麻使用者は吐き気を軽減するために、前嘔吐期に大麻の摂取量を増やします。11 通常24~48時間続く嘔吐期には、患者は頻繁に吐き気と嘔吐を経験し、その程度はひどくなります。
症状を緩和するために、患者は温浴、すなわち熱い風呂またはシャワーに何時間も入っていることを始めるかもしれません。 温浴は、末梢血管の拡張と脾循環からの再分配に影 響を与え、体温調節と胃への血流減少を助け、結果として 嘔吐を減少させる。残念ながら、温浴は脱水と急性腎 障害のリスクを高める可能性がある17。
多くの患者は、充血期の症状に対して医療を求める。 その結果、患者はCHS、膵炎、胃不全麻痺など、CHSの一部の症状に類似した他のさまざまな症状について、広範な陰性検査を受ける可能性があります。 吐き気と嘔吐が治まると、通常は48時間以内に、患者は回復期に入ります。 回復には数日から数ヶ月を要し、大麻の使用を中止することが必要である。 11
CHSが患者の他の疾患状態に与える影響を考慮することは重要です。 CHS患者が腎不全以外のCHS関連の医学的問題を発症したという症例報告もある。 Gregoire氏らは、双極性躁病と大麻の使用歴があり、CHSを発症した患者を紹介しています。19 患者は難治性の嘔吐をリチウムに起因すると考え、リチウムの摂取を中止し、躁転が起こりました。 19
CHSの診断基準も提案されている。 診断には長期的な大麻の使用が不可欠である。 CHSを発症するまでの期間はさまざまですが、ほとんどの患者は、慢性的な大麻使用から1~5年後に発症しています。 大麻使用1年前にCHSと同様の症状を呈していても、診断を否定するものではありません。 CHSの主な特徴としては、激しい周期的な吐き気と嘔吐、大麻をやめると症状が治まる、湯船につかると楽になる、心窩部または胸部周囲の腹痛、毎週大麻を使用する、などがあげられる。 CHSの診断につながる特徴としては、年齢<>5 kg、朝の症状発現、腸の正常習慣、他の検査での正常所見が挙げられます15。 表1はCHSの診断を裏付ける一般的な所見をまとめたものです14

考えられる治療
CHSの充血期を呈するすべての患者に支持療法が適応される。 患者が耐えられるのであれば、水分補給のために経口摂取が推奨される。 11 嘔吐により電解質障害が起こる可能性があるため、電解質のモニタリングと補充が指示される。
強制的な入浴は、CHSに伴う症状を最小限に抑えるために患者が行う、特徴的な学習行動である。 先に述べたように、温浴は体温調節に役立つと考えられる。 もう一つの理論は、末梢血管の拡張と脾循環からの再分配により、胃への血流が減少し、嘔吐が減少するというものである。
制吐薬は、CHSの症状を軽減するために使用されているが、成功した例はない。 制吐薬が効かない場合、臨床医はCHSを疑う必要がある。 症例報告では、患者はオンダンセトロン、プロメタジン、クロルプロマジン、メトクロプラミドで吐き気と嘔吐の治療効果が得られなかった21。小さなケースシリーズでは、患者の87.5%が標準的な制吐療法に反応しなかった12
ハロペリドールは中脳および中皮質の経路でドーパミンD2受容体に拮抗し抗精神病作用を発揮する。 ハロペリドールは伝統的に激越の治療に用いられるが、一般外科や腫瘍科では制吐薬としてうまく使用されている。 D2受容体は化学受容体トリガーゾーンにも存在し、このことがこれらの制吐作用を説明する可能性がある。 WitsilとMycykは、標準的な制吐療法に抵抗性の吐き気と嘔吐を有する4人の患者において、この仮説をレトロスペクティブに評価した21。 この小規模なケーススタディは、ハロペリドールがCHS関連の悪心・嘔吐を十分に緩和し、入院を防ぐ可能性があることを示し、医療システムのコスト削減につながる可能性があります。19 ハロペリドールによるQTc延長のリスクは、特に過度の嘔吐の結果、電解質障害を有する患者で考慮する必要があります。
大麻の中止は、CHSに関連する症状を緩和・予防する唯一の治療法です。 CHSを最初に記述した研究では、大麻を断つことで、10人中7人の患者の吐き気と嘔吐が止まりましたが、他の患者は継続的に病気に苦しみ続けました。 10 これらの知見は、最近の症例報告でも再現されています。
結論
大麻が多くの州で合法化されるにつれて、その使用は増加し、CHSの症例がより多く報告されると思われます。 臨床医は,大麻や合成カンナビノイドの使用歴があり,難治性の吐き気や嘔吐を含む症状を呈し,症状コントロールのために温浴を使用したという報告がある患者には,CHSを疑うべきである。 この推測は、他の疾患に対する広範で費用のかかる検査を防ぐことができます。 薬剤師は、大麻使用に伴うリスクについて患者にカウンセリングを行い、CHSの症状がある患者には適切なフォローアップケアを紹介する役割を担っています。 文献上の症例報告では、CHSの危険因子が特定されています。 残念ながら、CHSは比較的報告数が少なく、その正確なメカニズムは不明です。 CHSの診断と治療は、現在のところ、小規模な症例報告に基づいています。
適切な治療を行うために、今後も情報が入手可能になり次第、評価する必要があります。 米国国立薬物乱用研究所(NIDA)。 マリファナとは何か www.drugabuse.gov/publications/research-reports/marijuana/what-marijuana. 2016年8月25日アクセス分
2.NIDA. 米国におけるマリファナの使用範囲は?www.drugabuse.gov/publications/research-reports/marijuana/what-scope-marijuana-use-in-united-states. Accessed August 25, 2016.
3. キムHS、モンテAA. コロラド州の大麻合法化と救急医療への影響。 Ann Emerg Med. 2016;68:71-75.
4. Cerdá M, Wall M, Keyes KM, et al. Medical marijuana laws in 50 states: investigating the relationship between state legalization of medical marijuana and marijuana use, abuse and dependence.50州の医療大麻法:州の医療大麻の合法化と大麻使用、乱用、依存の関係を調査する。 Drug Alcohol Depend. 2012;120:22-27.
5. CNN Money. 大麻が合法な場所 http://money.cnn.com/interactive/news/economy/marijuana-legalization-map/index.html. Accessed August 25, 2016.
6. マリファナ・ポリシー・プロジェクト(Marijuana Policy Project). 2016年マリファナ政策改革法案。www.mpp.org/states/key-marijuana-policy-reform. 2016年11月13日アクセス.
7.NIDA. マリファナはどのようにその効果を生み出すのか www.drugabuse.gov/publications/research-reports/marijuana/how-does-marijuana-produce-its-effects. Accessed August 2016.
8. Manzanares J, Julian MD, Carrascosa A. Role of the cannabinoid system in pain control and therapeutic implications for the management of acute and chronic pain episodes.(カンナビノイドシステムの疼痛制御における役割と急性および慢性疼痛エピソードの管理に対する治療的意義)。 Curr Neuropharmacol。 2006;4:239-257.
9. ガリ JA、サワヤ RA、フリーデンバーグ FK. カンナビノイド充血症候群。 Curr Drug Abuse Rev. 2011;4:
241-249.
10.。 Allen JH, de Moore GM, Heddle R, Twartz JC. カンナビノイド充血症:慢性的な大麻乱用に伴う周期的な充血。 Gut. 2004;53:1566-1570.
11. Ruffle JK, Bajgoric S, Samra K, et al. Cannabinoid hyperemesis syndrome: an important differential diagnosis of persistent unexplained vomiting(カンナビノイド充血性症候群:持続的な原因不明の嘔吐の重要な鑑別診断)。 Eur J Gastroenterol Hepatol. 2015;27:1403-1408.
12. ソリアーノ・コM、バトケM、カッペルMS. 慢性的なマリファナ使用に伴う持続的な悪心・嘔吐、腹痛、強迫的な入浴を特徴とする大麻充血症候群:米国における8症例の報告. Dig Dis Sci. 2010;55:3113-3119.
13. Ukaigwe A, Karmacharya P, Donato A. A gut gone to pot: a case of cannabinoid hyperemesis syndrome due to K2, a synthetic cannabinoid. Case Rep Emerg Med. 2014;2014:167098.
14. ホプキンスCY、ギルクリストBL. 合成カンナビノイドによるカンナビノイド充血症候群の一例。 J Emerg Med. 2013;45:544-546.
15. Simonetto DA、Oxentenko AS、Herman ML、Szostek JH. カンナビノイド充血症:98人のケースシリーズ。 Mayo Clin Proc.2012;87:114-119.
16。 ルーML、アギトMD。 カンナビノイド充血症候群:マリファナは制吐剤と催吐剤の両方である。 クリーブクリンJメッド。 2015;82:429-434.
17. Habboushe J, Sedor J. Cannabinoid hyperemesis acute renal failure: a common sequela of cannabinoid hyperemesis syndrome.(カンナビノイド充血症候群の一般的な後遺症)。 Am J Emerg Med. 2014;32:690.e1-e2.
18. Srihari P, Liu M, Punzell S, et al. 強迫的シャワーと急性腎障害に関連するカンナビノイド充血症候群。 プリムケアコンパニオンCNS Disord. 2016;18(1).
19. Gregoire P, Tau M, Robertson D. Cannabinoid hyperemesis syndrome and the onset of a manic episode.(カンナビノイド充血症候群と躁病エピソードの発症)。 BMJ Case Rep.2016;2016.
20。 Bagdure S, Smalligan RD, Sharifi H, Khandheria B. Cannabinoid Hyperemesisにおける強制的入浴の効果の減退. アムJアディクト。 2012;21:184-185.
21. Witsil JC, Mycyk MB. ハロペリドール、カンナビノイド充血症候群の新規治療法。 Am J Ther. 2014年11月12日.
22. シュルツェDR、キャロルFI、マクマホンLR.Schulze DR, Carroll FI, McMahon LR. アカゲザルにおけるドーパミントランスポーターとカンナビノイド受容体リガンドの相互作用. サイコファーマコロジー(Berl). 2012;222:425-438.
23. Desai RI, Thakur GA, Vemuri VK, et al. CB1アゴニスト慢性投与時の耐性と行動・身体依存の解析:CB1アゴニスト、アンタゴニスト、非カンナビノイド薬の効果.2012.11.12. J Pharmacol Exp Ther. 2013;344:319-328.
24. Hickey JL, Witsil JC, Mycyk MB. カンナビノイド充血症候群の治療におけるハロペリドール。 Am J Emerg Med. 2013;31:1003.e5-e6.
25. Pélissier F, Claudet I, Gandia-Mailly P, et al. 救急部における大麻充血症候群:専門のアディクションチームはどのように役立つのか? パイロットスタディ。 J Emerg Med. 2016;51:544-551.