はじめに
進行した慢性腎臓病(ACKD)、推定糸球体濾過量(eGFR)30ml/min/1.73m2未満、DOQI分類によるステージ4および5、の高齢患者の数1は劇的に増加しており2、いくつかのシリーズではこの25年間で2倍になっています3。 当地では、アンダルシア州の透析・移植患者のデータベースであるKidney Transplant Coordination Data System of Andalusia (SICATA) の2013年のデータによると、70歳以上の患者が透析プログラムにおける事故患者の38%、有病患者の41.4%を占めています4。 平均寿命の延長と医学の進歩により、腎動脈硬化や糖尿病(DM)の発症期間が長くなっていることが要因です。 5 このような患者さんの多くは、腎動脈硬化症、数カ所の動脈硬化、心不全を伴う心疾患、血管アクセス困難などの合併症を持ち、依存度が高く、脆弱性が高いため、腎代替療法(RRT)が保存療法と比較して最善の選択肢かどうかは現在不明です。 したがって、RRTは彼らの生存率11-13、ましてやQOLを向上させないかもしれない。 この点で、特定の患者が、透析技術そのもの(腹膜透析の交換、透析センターへの移動、スケジュール管理、他の介護者や家族への依存など)によるライフスタイルの変化により、どのような影響を受けるかを考慮する必要があります。14,15
現在、高齢のACKD患者に対するより保存的な治療の可能性を評価することに関心が高まっています7。 しかし、この患者群における保存的治療は、「治療の欠如」や「専門性の低い医療」を意味するものではないことを明記しなければならない8。
本研究の目的は、当院の外来患者における高齢のACKD(ステージ4および5)患者の長期経過を明らかにし、CKDステージ5の患者で透析を受けたグループと保存的治療を行ったグループの生存率をレトロスペクティブに比較することである。
方法
セビリアのHospital Universitario Virgen del Rocío(病院面積140万人)の腎臓内科のACKDクリニックで2007年1月1日から2008年12月31日までに経過観察を開始し、5年間経過を観察した70歳以上の全患者を含む、後ろ向き観察研究;観察期間の終わりは2013年12月31日でした。 患者の特定と経過観察の情報収集には、自院のデータベースを使用した。
ACKDクリニック初診時の腎機能は、MDRD-4式を用いてベースラインの推定GFRとして算出した。 また、フォローアップ期間中に患者がステージ5(eGFR
15ml/min/1.73m2)に到達した場合には、腎機能を計算した。 腎臓病の原因、血液透析を開始した患者の場合はバスキュラーアクセス、DMの既往、虚血性心疾患(虚血エピソードと理解)、Charlson comorbidity indexの算出、離床前のクリニックでの追跡期間、離床理由(死亡、透析、観察期間の終了が2013年12月末)などを医療記録から抜粋した。 死亡した患者については、既知の疾患経過を経て当院で発生した場合と自宅で発生した場合に、その日付と原因を記録した。 他院で死亡した場合は死因を特定できなかった。
量的変数は正規分布を示さなかったため,中央値,25%および75%で記述的分析を行い,質的変数は数およびパーセントで表現した。 マン・ホイットニーU検定とカイ二乗検定を用い,透析を受けた患者と受けなかった患者,死亡した患者と追跡調査終了時に生存していた患者の間の差を分析した。 解析は、グループ全体(314人)とステージ5の患者(162人)の両方で行われました。 両群の生存率の推定と比較には、Kaplan-Meier法とlog-rank法を使用した。 Cox比例ハザード回帰を用いて、透析およびその他の独立変数が生存に及ぼす影響を調査した。 まず、各変数(年齢、eGFR、DM歴、虚血性心疾患歴、Charlson指数、透析治療)と生存率(従属変数)の相関を二変量回帰分析で独立に分析した。 そして、有意であった変数と特定の臨床的意義があると考えられる変数をCox回帰分析に含めた。 IBM SPSS-19統計パッケージが使用された。結果
最初に、指定された追跡期間中にACKDオフィスで連続して初診された70歳以上の患者348人が調査された。 追跡期間中に腎機能が回復し、一般腎臓内科に通院・復帰した患者は16名であった。 同様に、18人の患者がフォローアップから外れた。 これらの348人の患者は、対象期間中に初めて受診した全年齢の患者571人の61%を占めた。 最終的に314名の患者さんが抽出され、そのうち242名がCKDステージ4で追跡調査を開始し、90名(37%)がステージ5に進行した。 初診時(72人)または経過観察中(上記の90人)に162人がステージ5(eGFR
15ml/min/1.73m2)に到達した。 図1はこの情報を模式的に表したものです。
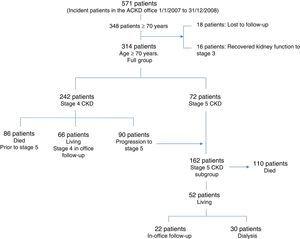
eGFRが30ml/min/1.73m2を超えているケースもあったが、一過性の改善で捨てられた患者さんはいない。 この改善が持続するケースでは、一般腎臓内科のクリニックに送り返された。 全グループ(314例)とステージ5のCKD患者のサブグループ(162例)の両方の人口統計データとその他の特徴を表1に示す。 表2は、2つのグループにおける追跡調査年ごとの生存率と、初診時(ベースライン)から追跡調査期間終了または死亡までの全生存率を示したものである。 eGFRがステージ4から始まりステージ5に進行した90名に関しては、eGFRが15cc/m/1.73m2未満になった時点からの生存率を考慮した。
Demographic data.を参照。
| Full group (n=314) | CKD 5 subgroup (n=162) | |
|---|---|---|
| Age in years, n (range) | 77 (74–81) | 77 (74–81) |
| Male, n (%) | 143 (46) | 89 (55) |
| Diabetes mellitus, n (%) | 157 (50) | 81 (50) |
| Charlson index, n (range) | 8 (7–9) | 7 (6–9) |
| Ischaemic heart disease, n (%) | 159 (51) | 78 (48) |
| Baseline eGFR (ml/min/1.73m2), n (range) | 20 (16–26) | 14 (12–14) |
| In-office follow-up (months), n (range) | 41 (13–64) | 15 (6–35) |
| Deaths, n (%) | 196 (64) | 110 (68) |
| Survival (months), median (25–75th percentile) | 56 (25–67) | 53 (29–67) |
Survival by year of follow-up and total.
| Full group (n=314) | CKD 5 subgroup (n=162) | |
|---|---|---|
| 1 year | 261 | 121 |
| 2 years | 235 | 97 |
| 3 years | 231 | 75 |
| 4 years | 169 | 52 |
| 5 years | 131 | 33 |
| Survival since baseline, months, median (25–75th percentile) | 56 (25–67) | 53 (29–67) |
| Survival since stage 5, months, median (25–75th percentile) | 33 (12–57) |
In the group of 69 patients who underwent dialysis (87% haemodialysis, 13% peritoneal dialysis), 35 patients (51%) had a vascular access, 18 patients (26%, in 10 cases vascular access was requested) started with a transitory venous catheter, type of access was unknown in 7 patients (10%), and 9 patients had a peritoneal catheter (13%). The median time in dialysis was 27 months (9–51) for the entire group of ≥70 y.o., 30 months (14–46) for the 46 patients ≥75 y.o., and 14 months (2–39) for the 15 patients ≥80 y.o. For the subgroup of 54 patients 70–80 y.o., the median time in dialysis was 30 months (10–52). None of the patients received a transplant.
Comparison of deaths vs. surviving patients (full group and stage 5 subgroup)
The difference between patients who died and alive was analysed; Table 3 displays the results in both the full group and in the subgroup with stage 5 CKD. The most frequent causes of death in the full group (196 deaths) were: cardiovascular disease in 137 patients (70%) and cancer in 24 patients (12%). Data regarding the cause of death was not available in 15 patients (8%).
Death vs. no death.
| Full group | Grade 5 CKD subgroup | |||||
|---|---|---|---|---|---|---|
| No death n=118 | Death n=196 | p | No death n=52 | Death n=110 | p | |
| Age in years, median (25–75th percentile) | 77 (73–79) | 77 (74–82) | 0.01 | 77 (73–80) | 77 (75–81) | 0.1 |
| Sex (M), n (%) | 69 (58) | 102 (52) | 0.1 | 29 (56) | 60 (55) | 0.5 |
| Diabetes mellitus, n (%) | 51 (43) | 106 (54) | 0.04 | 22 (42) | 59 (54) | 0.1 |
| Charlson index, median (25–75th percentile) | 8 (7–9) | 8 (7–9) | 0.9 | 7 (6–9) | 8 (6–9) | 0.2 |
| Ischaemic heart disease, n (%) | 52 (44) | 107 (55) | 0.03 | 23 (44) | 55 (50) | 0.3 |
| eGFR (ml/min/1.73m2), median (25–75th percentile) | 21.2 (16.8–26.5) | 19.7 (14.1–5.8) | 0.05 | 16.6 (14.3–20.8) | 15.1 (12.5–21.5) | 0.1 |
| Stage 5 eGFR (ml/min/1.73m2), median (25–75th percentile) | 13 (12.2–14.5) | 13.5 (12–14.3) | 0.3 | |||
| In-office follow-up (months), median (25–75th percentile) | 66 (60–74) | 25 (7–46) | 61 (35–70) | 25 (7–46) | ||
| In-office follow-up since stage 5 (months), median (25–75th percentile) | 30 (11–63) | 11 (3–24) | ||||
| Survival since baseline (months), median (25–75th percentile) | 69 (64–77) | 36 (12–50) | 70 (65–77) | 39 (15–56) | ||
| Survival since stage 5 (months), median (25–75th percentile) | 58 (39–71) | 21 (8–41) | ||||
| Dialysis, n (%) | 30 (25) | 39 (20) | 0.1 | 30 (58) | 39 (35) | 0.006 |
Comparison of dialysis vs. conservative treatment (subgroup of 162 stage 5 patients)
Table 4 shows the demographic data for the group comparing those who received dialysis and those who did not.
Dialysis vs. no dialysis stage 5 CKD subgroup (n=162).
| Dialysis n=69 | No dialysis n=93 | p | |
|---|---|---|---|
| Age, median (25–75th percentile) | 76 (73–79) | 78 (75–82) | 0.004 |
| Sex (M) | 35 (51%) | 54 (58%) | 0.2 |
| Diabetes mellitus | 34 (49%) | 47 (51%) | 0.5 |
| Charlson index, median (25–75th percentile) | 7 (6–8) | 8 (7–9) | |
| Ischaemic heart disease | 36 (52%) | 42 (45%) | 0.2 |
| In-office follow-up, months, median (25–75th percentile) | 10 (5–21) | 22 (5–42) | 0.008 |
| Survival, months | 65 (52–70) | 39 (14–60) | |
| Survival since stage 5, months, median (25–75th percentile) | 46 (27–62) | 21 (7–42) | |
| Stage 5 eGFR (ml/min/1.73m2), median (25–75th percentile) | 14 (11–14) | 14 (12–14) | 0.7 |
The Kaplan–Meier analysis confirmed that the survival was better in patients that were dialyzed: 69 vs. 93 patients in conservative treatment aged 70 or older (log-rank: 15.4; p
0.001). さらに、75歳以上(中央値77、25~75パーセンタイル:74~81歳)の患者120人を対象にサブ解析を行ったところ(46人対透析なし74人)、透析を受けている患者で生存率が高かった(log-rank:8.9、p値0.003)。 同様に、80歳以上の患者55人(中央値82、25〜75パーセンタイル:81〜84歳、15人対透析なし40人)を分析したところ、この群では透析を受けている患者は保存療法と比べて統計的に生存率が上昇しなかった(log-rank:1.6、p=0.2)。 図2は3つの患者群の年齢別の生存曲線です。

年齢層別の生存率に対する透析治療の効果(ステージ5のCKD患者):透析対透析なし
Cox回帰(ステージ5の患者162人のサブグループ)
このグループにおいて、どの変数が時間の経過とともに生存に影響を与えるかを判断するために、生存時間を従属変数としてCox回帰分析が完了しました。 二変量回帰を用いて最初に独立して評価した変数のうち、以下の結果が得られた:診察室でのフォローアップ時間(HR:0.95、p
0.001)、ベースラインのeGFR(MDRD-4)(HR:0.96、p=0.001)、年齢(HR:1.04、p=0.008)、透析(HR:1.68、p=0.01)。 性別、Charlson指数で測定した併存疾患、糖尿病歴、虚血性心疾患歴とは統計的に有意な相関はなかった。
生存率との二変量回帰で統計的に有意な変数と臨床的に関連性のある有意ではない変数(虚血性心疾患とDM)をCox回帰モデルでそれぞれどのような影響を与えるか調べたところ、年齢、MDRD-4のeGFRで測定した腎機能、透析、在室時間であることが判明した。 虚血性心疾患の既往、DMの既往、年齢は多変量解析において統計的に有意でなかった。 結果のハザード比は、我々の研究では、透析、診察室でのフォローアップ時間、およびベースラインの腎機能が、我々の患者グループの生存に最も重要な変数であることを示す(表5)。
| HR (95% CI) | p | |
|---|---|---|
| Age | 0.99 (0.95–1.04) | 0.8 |
| Diabetes mellitus | 1.06 (0.69–1.6) | 0.7 |
| Charlson index | 0.89 (0.79–1.03) | 0.1 |
| Ischaemic heart disease | 0.88 (0.59–1.32) | 0.5 |
| Baseline eGFR | 1.10 (1.06–1.14) | |
| Time in office | 0.93 (0.92–0.95) | |
| Treatment with dialysis | 0.05 (0.03–0.10) |
Influence of comorbidity on survival (full group and stage 5 subgroup)
An additional survival analysis was performed (Fig. 3) among the group of stage 5 patients with ischaemic heart disease (n=78) to determine whether dialysis still had a favourable effect on survival in this subgroup of patients. The results showed that dialysis did favour survival (36 dialysis vs. 42 without dialysis; log-rank 14.7; p
0.001). Similarly, the effect of dialysis in the group of patients with DM (n=81) was analysed, demonstrating that patients treated with dialysis had a better survival (34 vs. 47 patients without dialysis; log-rank 26; p0.001). また、シャルソン指数が高い(群中央値7以上)患者(n=80)においても、透析による生存率の差は有意であった(log-rank 6.9;p=0.008)
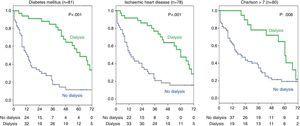
虚血性心疾患、糖尿病、または高Charlson併存症指数を有する患者サブグループ。 透析治療が生存に与える影響
ステージ5のCKD患者におけるDMまたは虚血性心疾患の既往と高いシャルソン指数の影響も分析されましたが、有意差は認められませんでした(図4)。 グループ全体(314人)では、この分析により虚血性心疾患は生存に影響を与えることがわかった(カイ二乗検定、表2)log-rank 4.2; p=0.04. As for DM, the difference is close to statistical significance (log-rank 3.3; p=0.06), and there were no differences in survival for a Charlson index over 8 (group median) (Fig. 5).
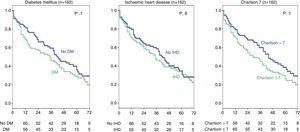
Influence of history of ischaemic heart disease, diabetes mellitus, and Charlson index on survival. Stage 5 chronic kidney disease subgroup (162 patients).
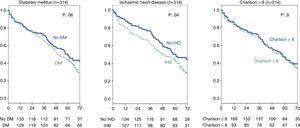
Influence of history of ischaemic heart disease, diabetes mellitus, and Charlson index on survival. Full group (314 patients).
Discussion
The results from our study in patients with advance age (≥70 years) with stage 5 CKD show that survival was higher in those treated with dialysis than in a conservative treatment; however this advantage is lost in patients ≥80 years. In addition to dialysis, survival in stage 5 patients was improved inpatients with a long time of follow up in the outpatient clinic and was not changed in relation to a higher comorbidity as measured by the Charlson index and a history of DM or ischaemic heart disease.
倫理的・技術的な理由から、この分野では無作為化試験は不可能である。いくつかの研究(すべて観察研究、ほとんどが英国で実施)は、透析プログラムに組み込まれた高齢患者の臨床転帰を観察しており、透析と保存療法の高齢者の臨床転帰を比較した報告は少数である。 一般に、透析を受けた患者の方が生存率が高いことが示されているが、虚血性心疾患の既往がある患者ではこの利点は失われる11。Charlson index16で測定した合併症や、透析開始後6ヶ月でいくつかの死亡危険因子を持つ患者では、透析を開始することが考慮されている17。 同様に、Da Silva-Ganeの研究で示されたように、入院日数や透析日数を差し引くと、生存期間の長さが有意でない場合があります16。透析患者の生存期間404日の差は、血液透析に割り当てられた326日を差し引くと、ある程度失われてしまいます。 腹膜透析の場合は、患者が移動する必要がないため、解釈が異なります。
この研究の結果は、以前に発表されたものと非常によく似ています。 Hussainによる研究18では、70歳以上でeGFRが15ml/min/1.73m2の患者の生存率を保存的治療と透析治療で比較しましたが、私たちの研究と同様に、80歳以上の患者とCharlson indexなどで測定した併存疾患の高い患者で生存率が低下しています。 Murtaghの研究11でも、私たちの研究と同様に、透析治療を受けた患者、特にACKD外来に早期に紹介され、eGFRが高い患者で生存期間が長いことが確認されている。 この生存率の優位性が、透析そのものによるものなのか、あるいはそのような外来で患者を正しくスクリーニングしケアすることによるものなのかは不明である。 しかし、この利点は、合併症指数、特に虚血性心疾患の有無が高い症例では大幅に失われた。 逆に、我々の研究では、ステージ5のCKD群では合併症に関連した差は見られず(ステージ4と5の患者314人の全グループでは差が見られた)、DMと虚血性心疾患を持つ患者においても、透析が生存にもたらすプラスの効果は依然として存在していた。 その理由の1つは、患者数が少ないために統計的検出力が低下したこと、また、多くの患者がDMと虚血性心疾患の両方を併発していることであろう。 また、多くの患者がDMと虚血性心疾患を併せ持つため、患者のサンプルは均質である。 透析を受けた患者と受けなかった患者では、DMと虚血性心疾患の有病率に差はありませんでしたが、透析を受けた患者では、若年であることとCharlson指数に差がありました。これは、患者がスクリーニングされて、若年で共存疾患の少ない人が透析に組み込まれ、治療に加えて生存にも有利になったことを示唆しています。 このことは、高齢者一人ひとりの合併症に基づいて治療法(透析か保存療法か)を個別化することの重要性について警告している先行研究と一致しています6-10,14-16
本研究では、外来診療に長期間通院した患者(CKDステージ4と5の全グループおよびCKDステージ5グループ)が、個別分析でも多変量解析で異なる変数を調整した後も良い生存期間を示しています。 この結果は、ACKDを受診した患者を1年間追跡調査したDe Nicolaの論文19など、これまでに発表された他の結果とも類似しています。 彼らは、より長い期間受診した患者の死亡リスクはより低かったと結論付けている。 ACKDを受診した患者を1年間追跡調査した結果、ACKDを受診した患者の方が死亡率が低いという結果が得られており、ACKD受診前のフォローアップは、RRTにおける短期・中期の予後を左右する患者それぞれの状況に応じて透析手段を選択するための重要な要素であるといえる20。
もうひとつの注目すべき点は、ベースラインで著しく悪化したにもかかわらず、我々の患者では腎機能の悪化が緩やかで、eGFR中央値が20ml/min/1.73m2に近いことです(5年間のフォローアップ後:27%がステージ5に到達せず、35%がステージ5に進行する前に死亡、37%がステージ5に進行した)。 このような経過は以前にも報告されており、低濾過量とアルブミン尿を併発した患者に多く見られるアルブミン尿がないことが、一部または多くの症例で正当化されているのかもしれない23,24。いずれにしても、現在の知識では、ACKD患者が進行する患者としない患者を識別することができない。 我々の研究では、ステージ4でフォローアップを開始した患者の死亡の可能性は、ステージ5への進行の可能性と同様であった。 他の研究では、死亡のリスクは末期CKDに進行するよりも高かった25,26。
本研究の限界として、家族のサポート、自律性、RRTまたは保存療法開始後のQOLデータなど、死亡率や生存率を左右する可能性のある追加データを入手できないことが挙げられる。 また,高齢のサブグループで透析を受けた患者の数が少ないことも指摘しなければならない。 本研究は単一施設で行われたものであり、得られた知見は他の患者群に完全に適用されない可能性がある。 この研究では、透析を受けなかった患者について、治療を断念したのか、拒否したのか、医学的禁忌があったのかについての情報が欠落している。
本研究は単一センターで行われたため、均一な患者集団であること、適用された治療が現在のCKD患者対応ガイドラインに従ってすべての患者で均一であることが利点である。 また、組み入れ期間が短かったため、同じような基準で、同じ薬剤が使用できる全患者に同じような治療が行われたことが有利に働きました。
他の研究では、治療意図や、RRTか保存的治療かの最初の決定に基づいて、患者を比較している。 私たちの研究は、患者が行った治療の結果を比較するもので、現実を反映しており、患者へのカウンセリングツールとして使用できるデータの有用性を高めています。 患者は具体的な治療結果について尋ねるので、治療方法を決定することができる。 透析か保存療法か。 透析療法は多くの場合、QOL(生活の質)を悪化させ、私たちの研究によると、保存療法を行った人と比べて生存期間を延長しないケースもありました。 27
結論として、私たちの高齢者グループ(70歳以上)において、年齢や合併症指数が低く、スクリーニングされた患者では、透析治療により生存率が向上することが確認されました。 この結果は、ACKDオフィスでの長期間のフォローアップによって有利に働いた。