Dosage Form: powder for oral suspension
Medically reviewed by Drugs.com. Last updated on April 1, 2019.
- Overview
- Side Effects
- Dosage
- Professional
- Tips
- Interactions
- More
- INDICATIONS & USAGE
- Respiratory Tract Infections
- Otitis Media
- Infecções da pele e da estrutura da pele
- Infecções ósseas
- Infecções do tracto geniturinário
- DOSAGE & ADMINISTRAÇÃO
- Pacientes Adultos e Pediátricos com Menos de 15 Anos de Idade
- Pacientes Pediátricos (acima de 1 ano de idade)
- Ajustes de dosagem em pacientes adultos e pediátricos com pelo menos 15 anos de idade com deficiência renal
- FORMAS DE DOSAGEM & STRENGTHS
- Contraindicações
- Avencimentos e Precauções
- Reações de hipersensibilidade
- Diarreia associada à Clostridium difficile
- Seroconversão do teste direto de Coombs
- Potencial de convulsões
- Tempo prolongado de protrombina
- Desenvolvimento de bactérias resistentes a drogas
- Reacções Adversas
- Experiência de Ensaios Clínicos
- Interacções drásticas
- Metformina
- Probenecid
- Interacção com testes laboratoriais ou de diagnóstico
- USA EM POPULAÇÕES ESPECÍFICAS
- Gravidez
- Mães amaldiçoadas
- Uso Pediátrico
- Uso Geriátrico
- Imparidade renal
- Overdose
- Cefalexina Suspensão Descrição
- Mecanismo de Ação
- Farmacocinética
- Nonclinical Toxicology
- Carcinogenesis & Mutagenesis & Impairment Of Fertility
- How Supplied/Storage and Handling
- Informações de Aconselhamento a Pacientes
- Frequently asked questions
- More about cephalexin
- Consumer resources
- Professional resources
- Related treatment guides
INDICATIONS & USAGE
Respiratory Tract Infections
Cephalexin is indicated for the treatment of respiratory tract infections caused by susceptible isolates of Streptococcus pneumoniae and Streptococcus pyogenes.
Otitis Media
Cephalexin is indicated for the treatment of otitis media caused by susceptible isolates of Streptococcus pneumoniae, Haemophilus influenzae, Staphylococcus aureus, Streptococcus pyogenes, and Moraxella catarrhalis.
Infecções da pele e da estrutura da pele
p>Cefalexina é indicada para o tratamento de infecções da pele e da estrutura da pele causadas por isolados sensíveis das seguintes bactérias Gram-positivas: Staphylococcus aureus e Streptococcus pyogenes.
Infecções ósseas
Cefalexina está indicada para o tratamento de infecções ósseas causadas por isolados sensíveis de Staphylococcus aureus e Proteus mirabilis.
Infecções do tracto geniturinário
p>Cefalexina está indicada para o tratamento de infecções do tracto geniturinário, incluindo prostatites agudas, causadas por isolados susceptíveis de Escherichia coli, Proteus mirabilis e Klebsiella pneumoniae.Para reduzir o desenvolvimento de bactérias resistentes a drogas e manter a eficácia da cefalexina e outros medicamentos antibacterianos, a cefalexina deve ser usada apenas para tratar infecções comprovadamente ou fortemente suspeitas de serem causadas por bactérias suscetíveis. Quando a cultura e a informação de susceptibilidade estão disponíveis, esta informação deve ser considerada na selecção ou modificação da terapia antibacteriana. Na ausência desses dados, a epidemiologia local e os padrões de susceptibilidade podem contribuir para a seleção empírica da terapia.
DOSAGE & ADMINISTRAÇÃO
Pacientes Adultos e Pediátricos com Menos de 15 Anos de Idade
A dose usual de cefalexina oral é de 250 mg a cada 6 horas, mas uma dose de 500 mg a cada 12 horas pode ser administrada. O tratamento é administrado por 7 a 14 dias.
Para infecções mais graves, doses maiores de cefalexina oral podem ser necessárias, até 4 gramas diários em duas a quatro doses igualmente divididas.
Pacientes Pediátricos (acima de 1 ano de idade)
A dose diária total recomendada de cefalexina oral para pacientes pediátricos é de 25 a 50 mg/kg em doses igualmente divididas por 7 a 14 dias. No tratamento das infecções por estreptococos hemolíticos β, recomenda-se uma duração de pelo menos 10 dias. In severe infections, a total daily dose of 50 to 100 mg/kg may be administered in equally divided doses.
For the treatment of otitis media, the recommended daily dose is 75 to 100 mg/kg given in equally divided doses.
| Weight 10 kg (22 lb) 20 kg (44 lb) 40 kg (88 lb) |
Cephalexin Suspension 125mg/5mL ½ to 1 tsp q.i.d. 1 to 2 tsp q.i.d. 2 to 4 tsp q.i.d. |
250mg/5mL ¼ to ½ tsp q.i.d. ½ to 1 tsp q.i.d. 1 to 2 tsp q.i.d. |
| Weight 10 kg (22 lb) 20 kg (44 lb) 40 kg (88 lb) |
125mg/5mL 1 to 2 tsp b.i.d. 2 to 4 tsp b.i.d. 4 to 8 tsp b.i.d. |
250mg/5mL ½ to 1 tsp b.i.d 1 to 2 tsp b.i.d. 2 to 4 tsp b.i.d. |
Direcções de Mistura
125 mg por 5 mL (100 mL quando misturado): Preparar o tempo de suspensão na distribuição. Adicionar ao frasco um total de 67 mL de água. Para facilitar a preparação, bater o frasco para soltar o pó, adicionar a água em 2 porções, agitando bem após cada adição. A suspensão resultante conterá cefalexina mono-hidratada equivalente a 125 mg de cefalexina em cada 5 mL (colher de chá).
125 mg por 5 mL (200 mL quando misturada): Preparar o tempo de suspensão na distribuição. Adicione ao frasco um total de 134 mL de água. Para facilitar a preparação, bata na garrafa para soltar o pó, adicione a água em 2 porções, agitando bem após cada adição. A suspensão resultante conterá cefalexina mono-hidratada equivalente a 125 mg de cefalexina em cada 5 mL (colher de chá).
250 mg por 5 mL (100 mL quando misturada): Preparar o tempo de suspensão na distribuição. Adicione ao frasco um total de 67 mL de água. Para facilitar a preparação, bata na garrafa para soltar o pó, adicione a água em 2 porções, agitando bem após cada adição. A suspensão resultante conterá cefalexina mono-hidratada equivalente a 250 mg de cefalexina em cada 5 mL (colher de chá).
250 mg por 5 mL (200 mL quando misturada): Preparar o tempo de suspensão na dispensação. Adicione ao frasco um total de 134 mL de água. Para facilitar a preparação, bata na garrafa para soltar o pó, adicione a água em 2 porções, agitando bem após cada adição. A suspensão resultante conterá cefalexina monoidrata equivalente a 250 mg de cefalexina em cada 5 mL (colher de chá).
* Após a mistura, conservar em geladeira. Pode ser mantida por 14 dias sem perda significativa de potência.
Ajustes de dosagem em pacientes adultos e pediátricos com pelo menos 15 anos de idade com deficiência renal
Administrar os seguintes regimes de dosagem de cefalexina para pacientes com deficiência renal .
Tabela 1. Recommended Dose Regimen for Patients with Renal Impairment
| Renal function | Dose regimen recommendation |
| Creatinine clearance ≥60 mL/min | No dose adjustment |
| Creatinine clearance 30 to 59 mL/min | No dose adjustment; maximum daily dose should not exceed 1 g |
| Creatinine clearance 15 to 29 mL/min | 250 mg, every 8 hours or every 12 hours |
| Creatinine clearance 5 to 14 mL/min not yet on dialysis* | 250 mg, every 24 hours |
| Creatinine clearance 1 to 4 mL/min not yet on dialysis* | 250 mg, a cada 48 horas ou a cada 60 horas |
*Não há informação suficiente para fazer recomendações de ajuste de dose em pacientes em hemodiálise.
FORMAS DE DOSAGEM & STRENGTHS
Cephalexin For Oral Suspension USP
125 mg/5mL e 250 mg/5mL
Contraindicações
A cefalexina está contra-indicada em pacientes com hipersensibilidade conhecida à cefalexina ou outros membros da classe de antibacterianos da cefalosporina.
Avencimentos e Precauções
Reações de hipersensibilidade
Reações alérgicas na forma de erupção cutânea, urticária, angioedema, anafilaxia, eritema multiforme, síndrome de Stevens-Johnson ou necrólise epidérmica tóxica têm sido relatadas com o uso de cefalexina. Antes de iniciar a terapia com cefalexina, pergunte se o paciente tem histórico de reações de hipersensibilidade à cefalexina, cefalosporinas, penicilinas ou outros medicamentos. A hipersensibilidade cruzada entre os medicamentos antibacterianos beta-lactam pode ocorrer em até 10% dos pacientes com histórico de alergia à penicilina.
Se ocorrer uma reação alérgica à cefalexina, descontinuar o medicamento e instituir tratamento adequado.
Diarreia associada à Clostridium difficile
Diarreia associada à Clostridium difficile (CDAD) tem sido relatada com o uso de quase todos os agentes antibacterianos, incluindo a cefalexina, e pode variar em gravidade desde diarréia leve até colite fatal. O tratamento com agentes antibacterianos altera a flora normal do cólon levando ao crescimento excessivo de C. difficile.
C. difficile produz toxinas A e B, que contribuem para o desenvolvimento da CDAD. As cepas produtoras de hipertoxina de C. difficile causam aumento de morbidade e mortalidade, uma vez que estas infecções podem ser refratárias à terapia antimicrobiana e podem requerer colectomia. O CDAD deve ser considerado em todos os pacientes que apresentam diarréia após o uso de antibióticos. O histórico médico cuidadoso é necessário uma vez que o CDAD foi relatado para ocorrer mais de dois meses após a administração de agentes antibacterianos.
Se houver suspeita ou confirmação de CDAD, o uso contínuo de antibióticos não direcionados contra C. difficile pode precisar ser descontinuado. O manejo apropriado de líquidos e eletrólitos, suplementação protéica, tratamento antibiótico de C. difficile e avaliação cirúrgica devem ser instituídos como clinicamente indicados.
Seroconversão do teste direto de Coombs
Testes Coombs diretos positivos foram relatados durante o tratamento com os antibacterianos cefalosporínicos, incluindo cefalexina. Hemólise intravascular aguda induzida pela terapia com cefalexina tem sido relatada. Se a anemia se desenvolver durante ou após a terapia com cefalexina, realizar um trabalho diagnóstico de anemia hemolítica induzida por drogas, interromper a cefalexina e instituir terapia apropriada.
Potencial de convulsões
p>Cefalosporinas siderais têm sido implicadas em desencadear convulsões, particularmente em pacientes com comprometimento renal, quando a dosagem não foi reduzida. Se ocorrerem convulsões, descontinuar a cefalexina. A terapia anticonvulsiva pode ser administrada se clinicamente indicada.
Tempo prolongado de protrombina
As cefalosporinas podem estar associadas a tempo prolongado de protrombina. Aqueles em risco incluem pacientes com comprometimento renal ou hepático, ou mau estado nutricional, assim como pacientes que recebem um curso prolongado de terapia antibacteriana, e pacientes que recebem terapia anticoagulante. Monitorar o tempo de protrombina em pacientes de risco e gerenciar como indicado.
Desenvolvimento de bactérias resistentes a drogas
Prescrição de cefalexina na ausência de uma infecção bacteriana comprovada ou fortemente suspeita é improvável que traga benefícios ao paciente e aumenta o risco do desenvolvimento de bactérias resistentes a drogas.
p>O uso prolongado de cefalexina pode resultar no crescimento excessivo de organismos não-susceptíveis. A observação cuidadosa do paciente é essencial. Se ocorrer superinfecção durante a terapia, devem ser tomadas medidas apropriadas.
Reacções Adversas
Os seguintes eventos graves são descritos com mais detalhes na secção Avisos e Precauções:
– Reacções de hipersensibilidade
– Diarreia associada ao Clostridium difficile
– Seroconversão do teste directo de Coombs
– Potencial de convulsão
– Efeito na actividade de protrombina
– Desenvolvimento de bactérias resistentes a drogas
Experiência de Ensaios Clínicos
Porque os ensaios clínicos são conduzidos em condições muito variáveis, As taxas de reacções adversas observadas nos ensaios clínicos de um medicamento não podem ser comparadas directamente com as taxas nos ensaios clínicos de outro medicamento e podem não reflectir as taxas observadas na prática.
Em ensaios clínicos, a reacção adversa mais frequente foi a diarreia. Também ocorreram náuseas e vómitos, dispepsia, gastrite e dor abdominal. Assim como com penicilinas e outras cefalosporinas, hepatite transitória e icterícia colestática foram relatadas.
Outras reações incluíram reações de hipersensibilidade, prurido genital e anal, candidíase genital, vaginite e corrimento vaginal, tontura, fadiga, dor de cabeça, agitação, confusão, alucinações, artralgia, artrite e desordem articular. Foi relatada nefrite intersticial reversível. Eosinofilia, neutropenia, trombocitopenia, anemia hemolítica e ligeiras elevações na transaminase de aspartato (AST) e na transaminase de alanina (ALT) foram relatadas.
Além das reações adversas listadas acima que foram observadas em pacientes tratados com cefalexina, as seguintes reações adversas e outros testes laboratoriais alterados foram relatados para drogas antibacterianas da classe cefalosporina:
Outras reações adversas: Febre, colite, anemia aplástica, hemorragia, disfunção renal e nefropatia tóxica.
Testes laboratoriais abrigados: Protrombina prolongada, aumento do nitrogênio uréico no sangue (BUN), aumento da creatinina, elevação da fosfatase alcalina, elevação da bilirrubina, elevação da desidrogenase láctica (LDH), pancitopenia, leucopenia e agranulocitose.
Interacções drásticas
Metformina
Administração de cefalexina com metformina resulta em aumento das concentrações plasmáticas de metformina e diminuição da depuração renal de metformina.
A monitorização cuidadosa do paciente e o ajuste da dose de metformina é recomendado em pacientes que tomam concomitantemente cefalexina e metformina .
Probenecid
A excreção renal da cefalexina é inibida pela probenecid. A co-administração de probenecid com cefalexina não é recomendada.
Interacção com testes laboratoriais ou de diagnóstico
Pode ocorrer uma reacção falso-positiva quando se testa a presença de glucose na urina usando solução de Benedict ou solução de Fehling.
USA EM POPULAÇÕES ESPECÍFICAS
Gravidez
Gravidez Categoria B
Não há estudos adequados e bem controlados em mulheres grávidas. Como os estudos de reprodução animal nem sempre são preditivos da resposta humana, esta droga só deve ser usada durante a gravidez se for claramente necessária.
Estudos de reprodução foram realizados em ratos e ratos usando doses orais de cefalexina monohidratada 0.6 e 1,5 vezes a dose máxima diária humana (66 mg/kg/dia) com base na superfície corporal, e não revelaram evidências de comprometimento da fertilidade ou danos ao feto.
Mães amaldiçoadas
Cefalexina é excretada no leite humano. A segurança e a eficácia da cefalexina em pacientes pediátricos foi estabelecida em ensaios clínicos para as dosagens descritas na seção de dosagem e administração.
Uso Pediátrico
A segurança e a eficácia da cefalexina em pacientes pediátricos foi estabelecida em ensaios clínicos para as dosagens descritas na seção de dosagem e administração.
Uso Geriátrico
Dos 701 sujeitos em 3 estudos clínicos publicados sobre cefalexina, 433 (62%) tinham 65 anos ou mais. Não foram observadas diferenças gerais de segurança ou eficácia entre esses sujeitos e os mais jovens, e outras experiências clínicas relatadas não identificaram diferenças nas respostas entre os pacientes idosos e os mais jovens.
Esse medicamento é substancialmente excretado pelo rim, e o risco de reações tóxicas a esse medicamento pode ser maior em pacientes com função renal comprometida. Como é mais provável que pacientes idosos tenham função renal diminuída, cuidados devem ser tomados na seleção da dose .
Imparidade renal
Cefalexina deve ser administrada com cautela na presença de função renal diminuída (clearance de creatinina < 30 mL/min, com ou sem diálise). Sob tais condições, observação clínica cuidadosa e estudos laboratoriais a monitorização da função renal deve ser realizada porque a dosagem segura pode ser inferior à normalmente recomendada .
Overdose
Symptoms of oral overdose podem incluir náuseas, vómitos, angústia epigástrica, diarreia e hematúria. Em caso de overdose, instituir medidas gerais de suporte.
Diurese forçada, diálise peritoneal, hemodiálise ou hemoperfusão de carvão vegetal não foram estabelecidas como benéficas para uma overdose de cefalexina.
Cefalexina Suspensão Descrição
p>Cefalexina suspensão oral, USP é um medicamento cefalosporino semi-sintético antibacteriano destinado à administração oral. É mono-hidratado de ácido 7-(D-α- Amino-α-fenilacetamido)-3-metil-3-cephem-4-carboxílico. A cefalexina tem a fórmula molecular C16H17N3O4S-H2O e o peso molecular é 365,41,
Cefalexina tem a seguinte fórmula estrutural:br>
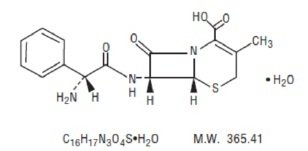
p>Ingredientes inativos: Dióxido de silício coloidal, FD&C Vermelho # 40, metilcelulose (15 premium LV), metilcelulose (4AC premium), benzoato de sódio, sabor morango, sacarose, goma xantana.h2>Cefalexina Suspensão – Farmacologia Clínica
Mecanismo de Ação
Cefalexina é um medicamento antibacteriano cefalosporino .
Farmacocinética
Absorção:
p>Cefalexina é estável a ácido e pode ser administrada sem considerar as refeições. Após doses de 250 mg, 500 mg e 1 g, foram obtidos níveis séricos médios de pico de aproximadamente 9, 18, e 32 mcg/mL, respectivamente, a 1 hora. Os níveis séricos foram detectáveis 6 horas após a administração (a um nível de detecção de 0,2 mcg/mL).
Distribuição:
Cefalexina é aproximadamente 10% a 15% ligada às proteínas plasmáticas.
Excreção:
Cefalexina é excretada na urina por filtração glomerular e secreção tubular. Estudos mostraram que mais de 90% da droga foi excretada inalterada na urina em 8 horas. Durante este período, os picos de concentração de urina após as doses de 250 mg, 500 mg e 1 g foram aproximadamente 1.000, 2.200 e 5.000 mcg/mL, respectivamente.
Interações de Drogas:
Em indivíduos saudáveis, dadas doses únicas de 500 mg de cefalexina e metformina, a metformina plasmática média Cmax e AUC aumentaram em média 34% e 24%, respectivamente, e a metformina média de depuração renal diminuiu 14%. Não há informações disponíveis sobre a interação entre cefalexina e metformina após múltiplas doses de qualquer um dos fármacos.
h3>Microbiologia
Mecanismo de Ação
p>Cefalexina é um agente bactericida que atua pela inibição da síntese bacteriana da parede celular.br>>p>Resistência
Estafilococos resistentes à meticilina e a maioria dos enterococos isolados são resistentes à cefalexina. A cefalexina não é ativa contra a maioria dos isolados de Enterobacter spp., Morganella morganii, e Proteus vulgaris. A cefalexina não tem actividade contra Pseudomonas spp., ou Acinetobacter calcoaceticus. O Streptococcus pneumoniae resistente à penicilina é geralmente resistente cruzado a drogas antibacterianas beta-lactâmicas.
Atividade antimicrobiana
Cefalexina demonstrou ser activa contra a maioria dos isolados das seguintes bactérias, tanto in vitro como em infecções clínicas .
Bactérias Gram-positivas
Staphylococcus aureus (apenas isolados com meticilina susceptível) Streptococcus pneumoniae (isolados com penicilina susceptível) Streptococcus pyogenes
Gram-bactéria negativa Escherichia coli Haemophilus influenzae Klebsiella pneumoniae Moraxella catarrhalis Proteus mirabilis
SusceptibilidadeTeste
Para informações específicas sobre critérios interpretativos do teste de susceptibilidade e métodos de teste associados e padrões de controle de qualidade reconhecidos pela FDA para este medicamento, por favor, veja: https://www.fda.gov/STIC.
Nonclinical Toxicology
Carcinogenesis & Mutagenesis & Impairment Of Fertility
Lifetime studies in animals have not been performed to evaluate the carcinogenic potential of cephalexin. Tests to determine the mutagenic potential of cephalexin have not been performed. In male and female rats, fertility and reproductive performance were not affected by cephalexin oral doses up to 1.5 times the highest recommended human dose based upon body surface area.
How Supplied/Storage and Handling
Cephalexin for oral suspension* USP (a strawberry flavored formula) is supplied as follows:
125 mg/5 mL:
Bottles of 100 mL (NDC 67877-544-88)
Bottles of 200 mL (NDC 67877-544-68)
250 mg/5 mL:
Bottles of 100 mL (NDC 67877-545-88)
Bottles of 200 mL (NDC 67877-545-68)
Directions for mixing are included on the label.
Localização a 20o a 25o C (68o a 77o F) .
Agite bem antes de usar. Manter bem fechado.
* Após a mistura, armazenar em geladeira. Pode ser mantido por 14 dias sem perda significativa de potência.
Informações de Aconselhamento a Pacientes
- Aconselhar os pacientes que podem ocorrer reações alérgicas, incluindo reações alérgicas graves, e que reações graves requerem tratamento imediato. Pergunte ao paciente sobre qualquer reação de hipersensibilidade anterior à cefalexina, outros beta-lactams (incluindo cefalosporinas) ou outros alergênios (5.1)
>Avisar aos pacientes que a diarréia é um problema comum causado por drogas antibacterianas e geralmente resolve quando a droga é descontinuada. Por vezes, pode ocorrer frequentemente diarreia aquosa ou com sangue e pode ser um sinal de uma infecção intestinal mais grave. Se se desenvolver diarreia grave, aquosa ou com sangue, aconselhe os pacientes a contactar o seu prestador de cuidados de saúde.li>Conselhe os pacientes que os medicamentos antibacterianos, incluindo cefalexina, só devem ser usados para tratar infecções bacterianas. Eles não tratam infecções virais (por exemplo, a constipação comum). Quando a cefalexina é prescrita para tratar uma infecção bacteriana, diga aos pacientes que, embora seja comum sentir-se melhor no início do tratamento, o medicamento deve ser tomado exactamente como indicado. Pular doses ou não completar o curso completo da terapia pode (1) diminuir a eficácia do tratamento imediato e (2) aumentar a probabilidade de as bactérias desenvolverem resistência e não serem tratadas pela cefalexina ou outros medicamentos antibacterianos no futuro.
p>Fabricados na Índia por:
Alkem Laboratories Ltd,
Mumbai – 400013, ÍNDIA.
Distribuído por:
Laboratórios de Ascendência, LLC
Parsippany, NJ 07054
Revisado: Dezembro, 2018
PT 2851
h2>PACKAGE LABEL.PRINCIPAL DISPLAY PANEL
NDC 67877-544-88
Cephalexin for Oral Suspension, USP 125 mg por 5 mL
quando reconstituído de acordo com as instruções.
Dose Pediátrica Usual: 25 a 50 mg por kg por dia em quatro doses divididas. Para infecções mais graves, a dose pode ser duplicada. Ver literatura anexa.
Apenas Rx
Apenas para uso oral
100 mL (quando misturado)
Laboratórios de Ascensão, LLC
br>>div>> br>>p>NDC 67877-545-88
br>>p>NDC 67877-545-88
Cefalexina para Suspensão Oral, USP 250 mg por 5 mL
quando reconstituída de acordo com as instruções.
Dose Pediátrica USP: 25 a 50 mg por kg por dia, em quatro doses divididas. Para infecções mais graves, a dose pode ser duplicada.
Veja a literatura que acompanha o medicamento.
Apenas Rx
Apenas para uso oral
100 mL (quando misturado)
Laboratórios de Ascendência, LLC

|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
| CEPHALEXIN cephalexin for suspension |
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
Labeler – Ascend Laboratories, LLC (141250469)
| Establishment | |||
| Name | Address | ID/FEI | Operations |
| Alkem Laboratories Limited | 915628612 | MANUFACTURE(67877-544, 67877-545) | |
Frequently asked questions
- What are the best antibiotics for a tooth infection?
- Cephalexin – can this be used to treat an abscess in the mouth or gum infection?
- If people are allergic to amoxicillin can they take cephalexin?
- What is the best antibiotic to treat strep throat?
- Can you take cephalexin for a spider bite?
- Can you take antibiotics while pregnant?
- Cephalexin – is this a drug that can be abused by teens?
More about cephalexin
- Side Effects
- During Pregnancy or Breastfeeding
- Dosage Information
- Patient Tips
- Drug Images
- Drug Interactions
- Compare Alternatives
- Support Group
- Pricing & Coupons
- En Español
- 415 Reviews
- Drug class: first generation cephalosporins
Consumer resources
- Patient Information
- Cephalexin (Advanced Reading)
Professional resources
- Prescribing Information
- Cephalexin (Professional Patient Advice)
- Cephalexin (FDA)
- Cephalexin Tablets (FDA)
Other brands Keflex, Daxbia, Panixine
Related treatment guides
- Bacterial Infection
- Bladder Infection
- Bacterial Endocarditis Prevention
- Acne
- … +7 more
Medical Disclaimer