Photoelektrischer Effekt und die Teilchennatur des Lichts
Im Jahr 1905 schlug Albert Einstein (1879-1955) vor, Licht als Energiequanten zu beschreiben, die sich wie Teilchen verhalten. Ein Photon ist ein Teilchen der elektromagnetischen Strahlung, das keine Masse hat und ein Energiequant trägt. Die Energie der Photonen des Lichts wird gemäß der Gleichung \(E = h \nu\) quantisiert. Viele Jahre lang wurde Licht nur mit Hilfe von Wellenkonzepten beschrieben, und für Wissenschaftler, die in der klassischen Physik ausgebildet waren, war dieser Welle-Teilchen-Dualismus des Lichts nur schwer zu akzeptieren. Ein Schlüsselkonzept, das Einstein mit Hilfe der Teilchennatur des Lichts erklärte, war der photoelektrische Effekt.
Der photoelektrische Effekt ist ein Phänomen, das auftritt, wenn Licht auf eine Metalloberfläche fällt und den Ausstoß von Elektronen aus diesem Metall bewirkt. Es wurde beobachtet, dass nur bestimmte Frequenzen des Lichts in der Lage sind, den Ausstoß von Elektronen zu bewirken. Wenn die Frequenz des einfallenden Lichts zu niedrig war (z. B. rotes Licht), wurden keine Elektronen ausgestoßen, auch wenn die Lichtintensität sehr hoch war oder das Licht lange auf die Oberfläche traf. War die Frequenz des Lichts höher (z. B. grünes Licht), konnten Elektronen aus der Metalloberfläche herausgeschleudert werden, auch wenn die Intensität sehr gering war oder das Licht nur kurz einstrahlte. Diese Mindestfrequenz, die nötig ist, um einen Elektronenauswurf zu bewirken, wird als Schwellenfrequenz bezeichnet.
Die klassische Physik konnte den photoelektrischen Effekt nicht erklären. Wenn man die klassische Physik auf diese Situation anwendet, könnte das Elektron im Metall schließlich genug Energie sammeln, um von der Oberfläche ausgestoßen zu werden, selbst wenn das einfallende Licht eine niedrige Frequenz hat. Einstein benutzte die Teilchentheorie des Lichts, um den photoelektrischen Effekt zu erklären, wie in der folgenden Abbildung dargestellt.
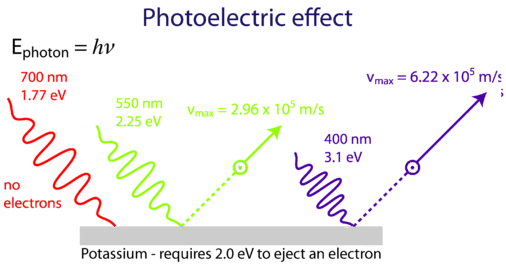
Niedrigfrequentes Licht (rot) ist nicht in der Lage, den Ausstoß von Elektronen aus der Metalloberfläche zu verursachen. Bei oder oberhalb der Schwellenfrequenz (grün) werden Elektronen herausgeschleudert. Noch höherfrequentes einfallendes Licht (blau) bewirkt den Ausstoß der gleichen Anzahl von Elektronen, aber mit größerer Geschwindigkeit.
Betrachten Sie die Gleichung \(E = h \nu\). \(E\) ist die Mindestenergie, die erforderlich ist, damit ein Elektron aus dem Metall herausgeschleudert werden kann. Wenn die Frequenz des einfallenden Lichts, \(\nu\), unter der Schwellenfrequenz liegt, wird nie genug Energie vorhanden sein, um den Ausstoß von Elektronen zu bewirken. Ist die Frequenz gleich oder höher als die Schwellenfrequenz, werden Elektronen herausgeschleudert. Wenn die Frequenz über den Schwellenwert hinaus ansteigt, bewegen sich die ausgestoßenen Elektronen einfach schneller. Eine Erhöhung der Intensität des einfallenden Lichts, die über der Schwellenfrequenz liegt, führt dazu, dass sich die Anzahl der ausgestoßenen Elektronen erhöht, aber sie bewegen sich nicht schneller. Der photoelektrische Effekt wird in so genannten photoelektrischen Zellen angewandt, die häufig in Alltagsgegenständen (z. B. einem Taschenrechner) zu finden sind und die Lichtenergie zur Stromerzeugung nutzen.

Photoelektrische Zellen wandeln Lichtenergie in elektrische Energie um, die diesen Taschenrechner mit Strom versorgt.