Dosage Form: powder for oral suspension
Medically reviewed by Drugs.com. Last updated on April 1, 2019.
- Overview
- Side Effects
- Dosage
- Professional
- Tips
- Interactions
- More
- INDICATIONS & USAGE
- Respiratory Tract Infections
- Otitis Media
- Haut- und Hautstrukturinfektionen
- Knocheninfektionen
- Infektionen des Urogenitaltrakts
- Anwendung
- DOSIERUNG & ADMINISTRATION
- Erwachsene und pädiatrische Patienten im Alter von mindestens 15 Jahren
- Pädiatrische Patienten (über 1 Jahr)
- Dosierungsanpassungen bei erwachsenen und pädiatrischen Patienten im Alter von mindestens 15 Jahren mit eingeschränkter Nierenfunktion
- DOSIERUNGSFORMEN& STÄRKEN
- Kontraindikationen
- Warnungen und Vorsichtsmaßnahmen
- Überempfindlichkeitsreaktionen
- Clostridium-difficile-assoziierte Diarrhoe
- Direkte Coombs-Test-Serokonversion
- Krampfpotenzial
- Verlängerte Prothrombinzeit
- Entwicklung arzneimittelresistenter Bakterien
- Nebenwirkungen
- Erfahrungen aus klinischen Studien
- Arzneimittelinteraktionen
- Metformin
- Probenecid
- Wechselwirkungen mit Labor- oder Diagnosetests
- VERWENDUNG IN BESONDEREN POPULATIONEN
- Schwangerschaft
- Stillende Mütter
- Anwendung in der Pädiatrie
- Anwendung in der Geriatrie
- Nierenschwäche
- Überdosierung
- Cephalexin Suspension Beschreibung
- Cephalexin Suspension – Klinische Pharmakologie
- Wirkmechanismus
- Pharmakokinetik
- Mikrobiologie
- Nonclinical Toxicology
- Carcinogenesis & Mutagenesis & Impairment Of Fertility
- How Supplied/Storage and Handling
- Patientenberatung
- PACKUNGSKENNZEICHNUNG.HAUPTANZEIGEFELD
- Frequently asked questions
- More about cephalexin
- Consumer resources
- Professional resources
- Related treatment guides
INDICATIONS & USAGE
Respiratory Tract Infections
Cephalexin is indicated for the treatment of respiratory tract infections caused by susceptible isolates of Streptococcus pneumoniae and Streptococcus pyogenes.
Otitis Media
Cephalexin is indicated for the treatment of otitis media caused by susceptible isolates of Streptococcus pneumoniae, Haemophilus influenzae, Staphylococcus aureus, Streptococcus pyogenes, and Moraxella catarrhalis.
Haut- und Hautstrukturinfektionen
Cephalexin ist angezeigt zur Behandlung von Haut- und Hautstrukturinfektionen, die durch empfindliche Isolate der folgenden grampositiven Bakterien verursacht werden: Staphylococcus aureus und Streptococcus pyogenes.
Knocheninfektionen
Cephalexin ist indiziert für die Behandlung von Knocheninfektionen, die durch empfängliche Isolate von Staphylococcus aureus und Proteus mirabilis verursacht werden.
Infektionen des Urogenitaltrakts
Cephalexin ist angezeigt zur Behandlung von Infektionen des Urogenitaltrakts, einschließlich akuter Prostatitis, die durch empfindliche Isolate von Escherichia coli, Proteus mirabilis und Klebsiella pneumoniae verursacht werden.
Anwendung
Um die Entwicklung arzneimittelresistenter Bakterien zu verringern und die Wirksamkeit von Cephalexin und anderen antibakteriellen Arzneimitteln aufrechtzuerhalten, sollte Cephalexin nur zur Behandlung von Infektionen verwendet werden, die nachweislich oder mit hoher Wahrscheinlichkeit durch anfällige Bakterien verursacht werden. Wenn Informationen über Kulturen und Anfälligkeiten vorliegen, sollten diese Informationen bei der Auswahl oder Änderung der antibakteriellen Therapie berücksichtigt werden. In Ermangelung solcher Daten können die lokale Epidemiologie und Empfindlichkeitsmuster zur empirischen Auswahl der Therapie beitragen.
DOSIERUNG & ADMINISTRATION
Erwachsene und pädiatrische Patienten im Alter von mindestens 15 Jahren
Die übliche Dosis von oralem Cephalexin beträgt 250 mg alle 6 Stunden, es kann jedoch auch eine Dosis von 500 mg alle 12 Stunden verabreicht werden. Die Behandlung wird 7 bis 14 Tage lang verabreicht.
Bei schwereren Infektionen können höhere Dosen von oralem Cephalexin erforderlich sein, bis zu 4 g täglich in zwei bis vier gleichmäßig verteilten Dosen.
Pädiatrische Patienten (über 1 Jahr)
Die empfohlene tägliche Gesamtdosis von oralem Cephalexin für pädiatrische Patienten beträgt 25 bis 50 mg/kg, verabreicht in gleichmäßig verteilten Dosen über 7 bis 14 Tage. Bei der Behandlung von β-hämolytischen Streptokokkeninfektionen wird eine Dauer von mindestens 10 Tagen empfohlen. In severe infections, a total daily dose of 50 to 100 mg/kg may be administered in equally divided doses.
For the treatment of otitis media, the recommended daily dose is 75 to 100 mg/kg given in equally divided doses.
| Weight 10 kg (22 lb) 20 kg (44 lb) 40 kg (88 lb) |
Cephalexin Suspension 125mg/5mL ½ to 1 tsp q.i.d. 1 to 2 tsp q.i.d. 2 to 4 tsp q.i.d. |
250mg/5mL ¼ to ½ tsp q.i.d. ½ to 1 tsp q.i.d. 1 to 2 tsp q.i.d. |
| Weight 10 kg (22 lb) 20 kg (44 lb) 40 kg (88 lb) |
125mg/5mL 1 to 2 tsp b.i.d. 2 to 4 tsp b.i.d. 4 to 8 tsp b.i.d. |
250mg/5mL ½ to 1 tsp b.i.d 1 to 2 tsp b.i.d. 2 to 4 tsp b.i.d. |
Hinweise zum Mischen
125 mg pro 5 mL (100 mL, wenn gemischt): Suspensionszeit bei der Abgabe vorbereiten. Geben Sie insgesamt 67 mL Wasser in die Flasche. Um die Zubereitung zu erleichtern, klopfen Sie auf die Flasche, um das Pulver zu lockern, fügen Sie das Wasser in 2 Portionen hinzu und schütteln Sie es nach jeder Zugabe gut. Die resultierende Suspension enthält Cephalexin-Monohydrat entsprechend 125 mg Cephalexin pro 5 mL (Teelöffel).
125 mg pro 5 mL (200 mL, wenn gemischt): Suspensionszeit bei der Abgabe vorbereiten. Geben Sie insgesamt 134 mL Wasser in die Flasche. Um die Zubereitung zu erleichtern, klopfen Sie auf die Flasche, um das Pulver zu lockern, fügen Sie das Wasser in 2 Portionen hinzu und schütteln Sie es nach jeder Zugabe gut. Die resultierende Suspension enthält Cephalexin-Monohydrat entsprechend 125 mg Cephalexin pro 5 mL (Teelöffel).
250 mg pro 5 mL (100 mL, wenn gemischt): Suspensionszeit bei der Abgabe vorbereiten. Geben Sie insgesamt 67 mL Wasser in die Flasche. Um die Zubereitung zu erleichtern, klopfen Sie auf die Flasche, um das Pulver zu lockern, fügen Sie das Wasser in 2 Portionen hinzu und schütteln Sie es nach jeder Zugabe gut. Die resultierende Suspension enthält Cephalexin-Monohydrat entsprechend 250 mg Cephalexin pro 5 mL (Teelöffel).
250 mg pro 5 mL (200 mL, wenn gemischt): Suspensionszeit bei der Abgabe vorbereiten. Geben Sie insgesamt 134 mL Wasser in die Flasche. Um die Zubereitung zu erleichtern, klopfen Sie auf die Flasche, um das Pulver zu lockern, fügen Sie das Wasser in 2 Portionen hinzu und schütteln Sie es nach jeder Zugabe gut. Die resultierende Suspension enthält Cephalexin-Monohydrat entsprechend 250 mg Cephalexin pro 5 ml (Teelöffel).
*Nach dem Mischen im Kühlschrank lagern. Die Haltbarkeit beträgt 14 Tage ohne nennenswerten Wirkungsverlust.
Dosierungsanpassungen bei erwachsenen und pädiatrischen Patienten im Alter von mindestens 15 Jahren mit eingeschränkter Nierenfunktion
Verabreichen Sie die folgenden Dosierungsschemata für Cephalexin an Patienten mit eingeschränkter Nierenfunktion.
Tabelle 1. Recommended Dose Regimen for Patients with Renal Impairment
| Renal function | Dose regimen recommendation |
| Creatinine clearance ≥60 mL/min | No dose adjustment |
| Creatinine clearance 30 to 59 mL/min | No dose adjustment; maximum daily dose should not exceed 1 g |
| Creatinine clearance 15 to 29 mL/min | 250 mg, every 8 hours or every 12 hours |
| Creatinine clearance 5 to 14 mL/min not yet on dialysis* | 250 mg, every 24 hours |
| Creatinine clearance 1 to 4 mL/min not yet on dialysis* | 250 mg, alle 48 Stunden oder alle 60 Stunden |
*Es liegen keine ausreichenden Informationen vor, um Empfehlungen zur Dosisanpassung bei Hämodialysepatienten zu geben.
DOSIERUNGSFORMEN& STÄRKEN
Cephalexin zum Einnehmen USP
125 mg/5 ml und 250 mg/5 ml
Kontraindikationen
Cephalexin ist kontraindiziert bei Patienten mit bekannter Überempfindlichkeit gegen Cephalexin oder andere Mitglieder der Cephalosporin-Klasse von antibakteriellen Arzneimitteln.
Warnungen und Vorsichtsmaßnahmen
Überempfindlichkeitsreaktionen
Allergische Reaktionen in Form von Hautausschlag, Urtikaria, Angioödem, Anaphylaxie, Erythema multiforme, Stevens-Johnson-Syndrom oder toxischer epidermaler Nekrolyse sind bei der Anwendung von Cephalexin berichtet worden. Bevor eine Therapie mit Cephalexin eingeleitet wird, sollte man sich erkundigen, ob der Patient in der Vergangenheit Überempfindlichkeitsreaktionen auf Cephalexin, Cephalosporine, Penicilline oder andere Medikamente gezeigt hat. Eine Kreuzüberempfindlichkeit zwischen Betalaktam-Antibiotika kann bei bis zu 10 % der Patienten mit einer Penicillin-Allergie in der Vorgeschichte auftreten.
Wenn eine allergische Reaktion auf Cephalexin auftritt, muss das Medikament abgesetzt und eine entsprechende Behandlung eingeleitet werden.
Clostridium-difficile-assoziierte Diarrhoe
Clostridium-difficile-assoziierte Diarrhoe (CDAD) wurde bei der Anwendung von fast allen antibakteriellen Mitteln, einschließlich Cephalexin, berichtet und kann in ihrem Schweregrad von leichter Diarrhoe bis zu tödlicher Kolitis reichen. Die Behandlung mit antibakteriellen Mitteln verändert die normale Darmflora, was zu einem übermäßigen Wachstum von C. difficile führt.
C. difficile produziert die Toxine A und B, die zur Entwicklung von CDAD beitragen. Hypertoxin-produzierende Stämme von C. difficile verursachen eine erhöhte Morbidität und Mortalität, da diese Infektionen auf eine antimikrobielle Therapie nicht ansprechen und eine Kolektomie erforderlich machen können. Eine CDAD muss bei allen Patienten in Betracht gezogen werden, die nach der Einnahme von Antibiotika Durchfall haben. Eine sorgfältige Anamnese ist erforderlich, da CDAD über zwei Monate nach der Verabreichung von antibakteriellen Wirkstoffen auftreten kann.
Wenn CDAD vermutet oder bestätigt wird, muss die laufende Einnahme von Antibiotika, die nicht gegen C. difficile gerichtet sind, möglicherweise eingestellt werden. Ein angemessenes Flüssigkeits- und Elektrolytmanagement, eine Proteinzufuhr, eine antibiotische Behandlung von C. difficile und eine chirurgische Untersuchung sollten je nach klinischer Indikation eingeleitet werden.
Direkte Coombs-Test-Serokonversion
Positive direkte Coombs-Tests wurden während der Behandlung mit den antibakteriellen Cephalosporin-Medikamenten, einschließlich Cephalexin, berichtet. Es wurde über eine akute intravaskuläre Hämolyse berichtet, die durch eine Cephalexin-Therapie ausgelöst wurde. Wenn sich während oder nach einer Cephalexin-Therapie eine Anämie entwickelt, ist eine Diagnostik auf eine arzneimittelinduzierte hämolytische Anämie durchzuführen, Cephalexin abzusetzen und eine geeignete Therapie einzuleiten.
Krampfpotenzial
Einige Cephalosporine wurden mit der Auslösung von Krampfanfällen in Verbindung gebracht, insbesondere bei Patienten mit Nierenfunktionsstörungen, wenn die Dosierung nicht reduziert wurde. Wenn Krampfanfälle auftreten, ist Cephalexin abzusetzen. Falls klinisch indiziert, kann eine antikonvulsive Therapie durchgeführt werden.
Verlängerte Prothrombinzeit
Cephalosporine können mit einer verlängerten Prothrombinzeit in Verbindung gebracht werden. Zu den Risikopatienten gehören Patienten mit eingeschränkter Nieren- oder Leberfunktion oder schlechtem Ernährungszustand sowie Patienten, die eine langwierige antibakterielle Therapie erhalten, und Patienten, die eine gerinnungshemmende Therapie erhalten.
Entwicklung arzneimittelresistenter Bakterien
Die Verschreibung von Cephalexin in Abwesenheit einer nachgewiesenen oder stark vermuteten bakteriellen Infektion wird dem Patienten wahrscheinlich keinen Nutzen bringen und erhöht das Risiko der Entwicklung arzneimittelresistenter Bakterien.
Die längerfristige Anwendung von Cephalexin kann zu einer Überwucherung von nicht-empfänglichen Organismen führen. Eine sorgfältige Beobachtung des Patienten ist unerlässlich. Wenn es während der Therapie zu einer Superinfektion kommt, sollten geeignete Maßnahmen ergriffen werden.
Nebenwirkungen
Die folgenden schwerwiegenden Ereignisse sind im Abschnitt „Warnhinweise und Vorsichtsmaßnahmen“ ausführlicher beschrieben:
– Überempfindlichkeitsreaktionen
– Clostridium-difficile-assoziierte Diarrhoe
– Direkte Coombs-Test-Serokonversion
– Krampfanfallspotenzial
– Auswirkung auf die Prothrombin-Aktivität
– Entwicklung arzneimittelresistenter Bakterien
Erfahrungen aus klinischen Studien
Da klinische Studien unter sehr unterschiedlichen Bedingungen durchgeführt werden, ist die
Da klinische Studien unter sehr unterschiedlichen Bedingungen durchgeführt werden, können die in den klinischen Studien eines Arzneimittels beobachteten Nebenwirkungsraten nicht direkt mit den Raten in den klinischen Studien eines anderen Arzneimittels verglichen werden und spiegeln möglicherweise nicht die in der Praxis beobachteten Raten wider.
In den klinischen Studien war die häufigste unerwünschte Wirkung Durchfall. Übelkeit und Erbrechen, Dyspepsie, Gastritis und Bauchschmerzen sind ebenfalls aufgetreten. Wie bei Penicillinen und anderen Cephalosporinen wurde über vorübergehende Hepatitis und cholestatische Gelbsucht berichtet.
Andere Reaktionen waren Überempfindlichkeitsreaktionen, genitaler und analer Juckreiz, genitale Candidiasis, Vaginitis und vaginaler Ausfluss, Schwindel, Müdigkeit, Kopfschmerzen, Unruhe, Verwirrung, Halluzinationen, Arthralgie, Arthritis und Gelenkbeschwerden. Reversible interstitielle Nephritis ist berichtet worden. Eosinophilie, Neutropenie, Thrombozytopenie, hämolytische Anämie und leichte Erhöhungen der Aspartat-Transaminase (AST) und der Alanin-Transaminase (ALT) wurden berichtet.
Zusätzlich zu den oben aufgeführten Nebenwirkungen, die bei mit Cephalexin behandelten Patienten beobachtet wurden, sind die folgenden Nebenwirkungen und andere veränderte Labortests für antibakterielle Arzneimittel der Cephalosporin-Klasse berichtet worden:
Sonstige Nebenwirkungen: Fieber, Kolitis, aplastische Anämie, Blutungen, Nierenfunktionsstörung und toxische Nephropathie.
Veränderte Labortests: Verlängerte Prothrombinzeit, erhöhter Blut-Harnstoff-Stickstoff (BUN), erhöhtes Kreatinin, erhöhte alkalische Phosphatase, erhöhtes Bilirubin, erhöhte Laktatdehydrogenase (LDH), Panzytopenie, Leukopenie und Agranulozytose.
Arzneimittelinteraktionen
Metformin
Die Verabreichung von Cephalexin mit Metformin führt zu erhöhten Metformin-Plasmakonzentrationen und einer verminderten renalen Clearance von Metformin.
Bei Patienten, die gleichzeitig Cephalexin und Metformin einnehmen, wird eine sorgfältige Patientenüberwachung und Dosisanpassung von Metformin empfohlen.
Probenecid
Die renale Ausscheidung von Cephalexin wird durch Probenecid gehemmt. Die gleichzeitige Verabreichung von Probenecid mit Cephalexin wird nicht empfohlen.
Wechselwirkungen mit Labor- oder Diagnosetests
Eine falsch-positive Reaktion kann auftreten, wenn mit Benedict’s Lösung oder Fehling’s Lösung auf das Vorhandensein von Glukose im Urin getestet wird.
VERWENDUNG IN BESONDEREN POPULATIONEN
Schwangerschaft
Schwangerschaftskategorie B
Es gibt keine ausreichenden und gut kontrollierten Studien bei schwangeren Frauen. Da tierexperimentelle Reproduktionsstudien nicht immer auf die Reaktion beim Menschen schließen lassen, sollte dieses Arzneimittel während der Schwangerschaft nur bei eindeutigem Bedarf angewendet werden.
Reproduktionsstudien wurden an Mäusen und Ratten mit oralen Dosen von Cephalexin-Monohydrat 0.Die Reproduktionsstudien wurden an Mäusen und Ratten mit oralen Dosen von Cephalexin-Monohydrat durchgeführt, die dem 6- und 1,5-fachen der maximalen Tagesdosis für den Menschen (66 mg/kg/Tag) auf Basis der Körperoberfläche entsprachen, und ergaben keine Hinweise auf eine Beeinträchtigung der Fruchtbarkeit oder eine Schädigung des Fötus.
Stillende Mütter
Cephalexin wird in die Muttermilch ausgeschieden. Vorsicht ist geboten, wenn Cephalexin einer stillenden Frau verabreicht wird.
Anwendung in der Pädiatrie
Die Sicherheit und Wirksamkeit von Cephalexin bei pädiatrischen Patienten wurde in klinischen Studien für die im Abschnitt „Dosierung und Verabreichung“ beschriebenen Dosierungen nachgewiesen.
Anwendung in der Geriatrie
Von den 701 Probanden in 3 veröffentlichten klinischen Studien mit Cephalexin waren 433 (62 %) 65 Jahre und älter. Es wurden keine allgemeinen Unterschiede in der Sicherheit oder Wirksamkeit zwischen diesen Probanden und jüngeren Probanden beobachtet, und auch in anderen berichteten klinischen Erfahrungen wurden keine Unterschiede in den Reaktionen zwischen älteren und jüngeren Patienten festgestellt.
Dieses Arzneimittel wird im Wesentlichen über die Nieren ausgeschieden, und das Risiko toxischer Reaktionen auf dieses Arzneimittel kann bei Patienten mit eingeschränkter Nierenfunktion größer sein. Da ältere Patienten eher eine eingeschränkte Nierenfunktion haben, sollte die Dosis mit Vorsicht gewählt werden.
Nierenschwäche
Cephalexin sollte bei eingeschränkter Nierenfunktion (Kreatinin-Clearance < 30 mL/min, mit oder ohne Dialyse) mit Vorsicht verabreicht werden. Unter solchen Bedingungen sollten eine sorgfältige klinische Beobachtung und Laboruntersuchungen zur Überwachung der Nierenfunktion durchgeführt werden, da die sichere Dosierung niedriger sein kann als die üblicherweise empfohlene.
Überdosierung
Symptome einer oralen Überdosierung können Übelkeit, Erbrechen, epigastrisches Unwohlsein, Durchfall und Hämaturie umfassen. Im Falle einer Überdosierung sind allgemeine unterstützende Maßnahmen einzuleiten.
Zwangsdiurese, Peritonealdialyse, Hämodialyse oder Hämoperfusion mit Aktivkohle haben sich bei einer Überdosierung von Cephalexin nicht als nützlich erwiesen.
Cephalexin Suspension Beschreibung
Cephalexin Suspension zum Einnehmen, USP ist ein halbsynthetisches antibakterielles Cephalosporin zur oralen Verabreichung. Es handelt sich um 7-(D-α- Amino-α-phenylacetamido)-3-methyl-3-cephem-4-carboxylsäure-Monohydrat. Cephalexin hat die Summenformel C16H17N3O4S-H2O und das Molekulargewicht beträgt 365,41.
Cephalexin hat die folgende Strukturformel:
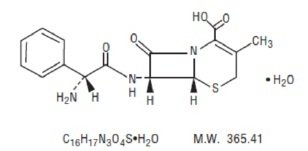
Inaktive Bestandteile: Kolloidales Siliciumdioxid, FD&C Rot # 40, Methylcellulose (15 Premium LV), Methylcellulose (4AC Premium), Natriumbenzoat, Erdbeergeschmack, Saccharose, Xanthan.
Cephalexin Suspension – Klinische Pharmakologie
Wirkmechanismus
Cephalexin ist ein antibakterielles Cephalosporin.
Pharmakokinetik
Absorption:
Cephalexin ist säurestabil und kann unabhängig von den Mahlzeiten gegeben werden. Nach einer Dosis von 250 mg, 500 mg und 1 g wurden nach 1 Stunde durchschnittliche Serumspitzenwerte von etwa 9, 18 bzw. 32 mcg/ml erreicht. Serumspiegel waren 6 Stunden nach der Verabreichung nachweisbar (bei einer Nachweisgrenze von 0,2 mcg/ml).
Verteilung:
Cephalexin ist zu etwa 10 % bis 15 % an Plasmaproteine gebunden.
Ausscheidung:
Cephalexin wird im Urin durch glomeruläre Filtration und tubuläre Sekretion ausgeschieden. Studien zeigten, dass über 90 % des Arzneimittels innerhalb von 8 Stunden unverändert mit dem Urin ausgeschieden werden. Während dieses Zeitraums betrugen die Spitzenkonzentrationen im Urin nach einer Dosis von 250 mg, 500 mg und 1 g etwa 1.000, 2.200 bzw. 5.000 mcg/ml.
Wirkstoffwechselwirkungen:
Bei gesunden Probanden, die eine Einzeldosis von 500 mg Cephalexin und Metformin erhielten, stiegen die mittlere Cmax und AUC von Metformin im Plasma um durchschnittlich 34 % bzw. 24 %, und die mittlere renale Clearance von Metformin verringerte sich um 14 %. Es liegen keine Informationen über die Wechselwirkung von Cephalexin und Metformin nach Mehrfachgabe eines der beiden Arzneimittel vor.
Mikrobiologie
Wirkungsmechanismus
Cephalexin ist ein bakterizides Mittel, das durch Hemmung der bakteriellen Zellwandsynthese wirkt.
Resistenz
Methicillin-resistente Staphylokokken und die meisten Isolate von Enterokokken sind resistent gegen Cephalexin. Cephalexin ist gegen die meisten Isolate von Enterobacter spp., Morganella morganii und Proteus vulgaris nicht wirksam. Cephalexin ist nicht wirksam gegen Pseudomonas spp. oder Acinetobacter calcoaceticus. Penicillin-resistenter Streptococcus pneumoniae ist in der Regel kreuzresistent gegen Beta-Lactam-Antibiotika.
Antimikrobielle Aktivität
Cephalexin hat sich gegen die meisten Isolate der folgenden Bakterien sowohl in vitro als auch bei klinischen Infektionen als wirksam erwiesen.
Gramm-positive Bakterien
Staphylococcus aureus (nur Methicillin-empfängliche Isolate) Streptococcus pneumoniae (Penicillin-empfängliche Isolate) Streptococcus pyogenes
Gramm-negative Bakterien Escherichia coli Haemophilus influenzae Klebsiella pneumoniae Moraxella catarrhalis Proteus mirabilis
Suszeptibilitätstests
Für spezifische Informationen zu den Interpretationskriterien von Suszeptibilitätstests und den damit verbundenen Testmethoden und Qualitätskontrollstandards, die von der FDA für dieses Arzneimittel anerkannt sind, siehe entnehmen Sie bitte: https://www.fda.gov/STIC.
Nonclinical Toxicology
Carcinogenesis & Mutagenesis & Impairment Of Fertility
Lifetime studies in animals have not been performed to evaluate the carcinogenic potential of cephalexin. Tests to determine the mutagenic potential of cephalexin have not been performed. In male and female rats, fertility and reproductive performance were not affected by cephalexin oral doses up to 1.5 times the highest recommended human dose based upon body surface area.
How Supplied/Storage and Handling
Cephalexin for oral suspension* USP (a strawberry flavored formula) is supplied as follows:
125 mg/5 mL:
Bottles of 100 mL (NDC 67877-544-88)
Bottles of 200 mL (NDC 67877-544-68)
250 mg/5 mL:
Bottles of 100 mL (NDC 67877-545-88)
Bottles of 200 mL (NDC 67877-545-68)
Directions for mixing are included on the label.
Lagerung bei 20o bis 25o C (68o bis 77o F).
Vor Gebrauch gut schütteln. Dicht verschlossen halten.
*Nach dem Mischen im Kühlschrank lagern. Die Haltbarkeit beträgt 14 Tage ohne nennenswerten Wirkungsverlust.
Patientenberatung
- Beraten Sie die Patienten, dass allergische Reaktionen, einschließlich schwerer allergischer Reaktionen, auftreten können und dass schwere Reaktionen sofortige Behandlung erfordern. Fragen Sie den Patienten nach früheren Überempfindlichkeitsreaktionen auf Cephalexin, andere Beta-Lactame (einschließlich Cephalosporine) oder andere Allergene (5.1)
- Beraten Sie den Patienten, dass Durchfall ein häufiges Problem ist, das durch antibakterielle Arzneimittel verursacht wird und normalerweise verschwindet, wenn das Arzneimittel abgesetzt wird. Manchmal können häufige wässrige oder blutige Durchfälle auftreten, die ein Anzeichen für eine ernstere Darminfektion sein können. Wenn schwerer wässriger oder blutiger Durchfall auftritt, sollten die Patienten ihren medizinischen Betreuer kontaktieren.
- Beraten Sie die Patienten, dass antibakterielle Medikamente, einschließlich Cephalexin, nur zur Behandlung bakterieller Infektionen verwendet werden sollten. Sie sind nicht zur Behandlung von Virusinfektionen (z. B. Erkältungskrankheiten) geeignet. Wenn Cephalexin zur Behandlung einer bakteriellen Infektion verschrieben wird, weisen Sie die Patienten darauf hin, dass es zwar üblich ist, sich zu Beginn der Therapie besser zu fühlen, das Medikament aber genau nach Anweisung eingenommen werden muss. Das Auslassen von Dosen oder die nicht vollständige Beendigung der Therapie kann (1) die Wirksamkeit der sofortigen Behandlung verringern und (2) die Wahrscheinlichkeit erhöhen, dass Bakterien eine Resistenz entwickeln und in Zukunft nicht mehr mit Cephalexin oder anderen antibakteriellen Medikamenten behandelt werden können.
Hergestellt in Indien von:
Alkem Laboratories Ltd,
Mumbai – 400013, INDIA.
Vertrieben durch:
Ascend Laboratories, LLC
Parsippany, NJ 07054
Revised: Dezember 2018
PT 2851
PACKUNGSKENNZEICHNUNG.HAUPTANZEIGEFELD
NDC 67877-544-88
Cephalexin zum Einnehmen, USP 125 mg pro 5 mL
wenn es gemäß den Anweisungen rekonstituiert wird.
Angemessene pädiatrische Dosis: 25 bis 50 mg pro kg pro Tag in vier geteilten Dosen. Bei schwereren Infektionen kann die Dosis verdoppelt werden. Siehe beiliegende Literatur.
Rx only
For Oral Use only
100 mL (wenn gemischt)
Ascend Laboratories, LLC

NDC 67877-545-88
Cephalexin for Oral Suspension, USP 250 mg pro 5 mL
wenn gemäß den Anweisungen rekonstituiert.
Gebräuchliche pädiatrische Dosis: 25 bis 50 mg pro kg pro Tag in vier geteilten Dosen. Bei schwereren Infektionen kann die Dosis verdoppelt werden.
Siehe Begleitliteratur.
Nur auf Rezept
Nur zum Einnehmen
100 ml (gemischt)
Ascend Laboratories, LLC

| CEPHALEXIN Cephalexin zur Suspension |
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
| CEPHALEXIN cephalexin for suspension |
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
Labeler – Ascend Laboratories, LLC (141250469)
| Establishment | |||
| Name | Address | ID/FEI | Operations |
| Alkem Laboratories Limited | 915628612 | MANUFACTURE(67877-544, 67877-545) | |
Frequently asked questions
- What are the best antibiotics for a tooth infection?
- Cephalexin – can this be used to treat an abscess in the mouth or gum infection?
- If people are allergic to amoxicillin can they take cephalexin?
- What is the best antibiotic to treat strep throat?
- Can you take cephalexin for a spider bite?
- Can you take antibiotics while pregnant?
- Cephalexin – is this a drug that can be abused by teens?
More about cephalexin
- Side Effects
- During Pregnancy or Breastfeeding
- Dosage Information
- Patient Tips
- Drug Images
- Drug Interactions
- Compare Alternatives
- Support Group
- Pricing & Coupons
- En Español
- 415 Reviews
- Drug class: first generation cephalosporins
Consumer resources
- Patient Information
- Cephalexin (Advanced Reading)
Professional resources
- Prescribing Information
- Cephalexin (Professional Patient Advice)
- Cephalexin (FDA)
- Cephalexin Tablets (FDA)
Other brands Keflex, Daxbia, Panixine
Related treatment guides
- Bacterial Infection
- Bladder Infection
- Bacterial Endocarditis Prevention
- Acne
- … +7 more
Medical Disclaimer