US Pharm. 2016;41(12):HS16-HS19.
ABSTRACT: Van marihuana, of cannabis, wordt over het algemeen gedacht dat het een goedaardige stof is zonder nadelige effecten; het cannabinoïde hyperemesis syndroom (CHS) is echter een sequela van chronisch cannabisgebruik. Artsen moeten CHS sterk vermoeden bij langdurige cannabisgebruikers die zich presenteren met hardnekkige misselijkheid en braken en bij wie de symptomen worden verlicht door baden in heet water. Het uitblijven van een reactie op anti-emetica zou moeten helpen bij het stellen van de diagnose CHS. De enige behandeling die CHS met succes kan oplossen, is onthouding van cannabis, hoewel haloperidol wordt onderzocht als een mogelijke behandelingsoptie. Een patiënt die CHS ervaart, moet worden geadviseerd om cannabis te vermijden, omdat verder gebruik verdere symptomen zal triggeren.
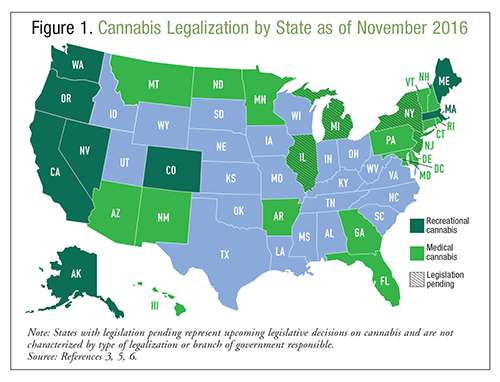
Marijuana, of cannabis, is een natuurlijk product dat is afgeleid van een hennepplant die bekend staat als Cannabis sativa; het wordt algemeen beschouwd als een goedaardige stof zonder nadelige effecten.1 Cannabis kan worden gerookt, verdampt of ingenomen voor intoxicatie of therapeutisch voordeel, en het wordt al eeuwenlang voor deze doeleinden gebruikt. Volgens de 2014 National Survey on Drug Use and Health, >22 miljoen Amerikanen gebruikten cannabis in de voorafgaande maand, waarmee deze stof de meest gebruikte illegale drug is.2 Verwacht wordt dat het cannabisgebruik in de Verenigde Staten zal blijven toenemen vanwege de toenemende legalisatiegraad.3 Volgens het National Epidemiologic Survey on Alcohol and Related Conditions hebben inwoners van staten die medicinale cannabis hebben gelegaliseerd twee keer zoveel kans om cannabisgebruik te onderschrijven als inwoners van staten zonder legalisering.4 Op dit moment mag cannabis in 28 staten voor medicinale doeleinden worden gebruikt, en in acht staten ook voor recreatieve doeleinden. Zie FIGUUR 1 voor informatie over de legaliteit van cannabis in de VS op dit moment.3,5,6 Naast legalisering hebben 21 staten en het District of Columbia het bezit van kleine hoeveelheden cannabis gedecriminaliseerd. Medische noodgevallen in verband met cannabisgebruik zijn tussen 2009 en 2011 met 29% toegenomen; het is onbekend of deze toename te wijten is aan de potentie van de cannabis, toegenomen legalisering of andere factoren.1
Het menselijk lichaam heeft een intrinsiek cannabinoïdesysteem, bekend als het endocannabinoïdesysteem, dat neurotransmitters (d.w.z. anandamide) bevat die eetlust, slaap, pijn, emotie en beweging reguleren.7,8 Cannabinoïde verwijst naar elke verbinding die cannabinoïde-receptoren in het lichaam beïnvloedt. Receptoren die therapeutische doeleinden dienen, zijn onder meer cannabinoïde type 1 en 2 (CB1, CB2). CB1 wordt in grote hoeveelheden aangetroffen in de hersenen en in mindere hoeveelheden in spinaal en perifeer zenuwweefsel, terwijl CB2 in grote hoeveelheden wordt aangetroffen in perifere weefsels en het immuunsysteem.8
Cannabis bevat >100 chemische stoffen, waarvan delta-9-tetrahydrocannabinol (THC) de actiefste verbinding is. Omdat het zich bindt aan CB1, is THC verantwoordelijk voor het bedwelmende effect van cannabis.1 Andere cannabinoïden in cannabis zijn cannabidiol en cannabigerol, die niet psychoactief zijn. Vanwege het brede scala aan activiteiten die het intrinsieke systeem beïnvloedt, hebben veel mensen cannabinoïden gebruikt voor bedwelming en voor therapeutische doeleinden.
Cannabinoïd Hyperemesis Syndrome
Cannabis is gebruikt om de eetlust te bevorderen bij de behandeling van HIV/AIDS-geassocieerde anorexia en verspilling en om door chemotherapie veroorzaakte misselijkheid en braken te verlichten. Hoewel cannabis kan worden gebruikt om misselijkheid en braken te behandelen, kan het ook een paradoxaal syndroom van misselijkheid en braken veroorzaken dat bekend staat als cannabinoïd hyperemesis syndroom (CHS). CHS is een klinische diagnose die wordt gekenmerkt door chronisch cannabisgebruik.9 Een uniek kenmerk van CHS is cyclische misselijkheid en braken die niet reageren op standaard anti-emetische therapie, maar wel op dwangmatig warm baden.3,9 Het eerste gedocumenteerde casusverslag over CHS (2004) beschreef negen patiënten in Australië. Voorafgaand aan de presentatie was er sprake van chronisch cannabisgebruik, en de symptomen bestonden uit misselijkheid en braken. De meeste patiënten meldden dat ze baden in heet water om de symptomen te verlichten. Stoppen met cannabisgebruik leidde tot oplossing van de ziekte, terwijl patiënten die cannabis bleven gebruiken ziek bleven.10 Sindsdien zijn er meer casusrapporten en series gepubliceerd die CHS verder beschrijven; er zijn echter geen gerandomiseerde, gecontroleerde studies geweest die CHS hebben geëvalueerd of gedefinieerd.
In Colorado is het aantal gevallen van CHS verdubbeld sinds 2009, toen cannabis daar werd gelegaliseerd.3 Het is echter belangrijk op te merken dat CHS vaak niet wordt herkend door artsen, wat kan leiden tot een uitgebreid en kostbaar onderzoek van de patiënt. De diagnose kan een uitdaging zijn, en CHS kan verkeerd worden gediagnosticeerd als vele andere aandoeningen, waaronder cyclisch braaksyndroom (CVS). Hoewel sommige marihuanagebruikers CVS hebben, zijn er een aantal onderscheidende factoren tussen CVS en CHS. Bij CVS is er meestal sprake van een persoonlijke of familiegeschiedenis van migraine, een voorgeschiedenis van psychiatrische stoornissen, en een gebrek aan dwangmatig warm baden.11 Patiënten met CHS presenteren zich vaak op de spoedeisende hulp (ED) vanwege de symptomen. Een case report van Soriano-Co en collega’s toonde aan dat patiënten met de diagnose CHS meer kans hadden op frequente bezoeken aan een arts, bezoeken aan de ED en ziekenhuisopnames.12 Gemiddeld had een patiënt vijf bezoeken aan een arts, zeven bezoeken aan de ED en drie ziekenhuisopnames voordat de diagnose werd gesteld, wat aangeeft dat patiënten met CHS in elke zorgsetting kunnen worden gezien.12 De diagnose wordt verder bemoeilijkt door het gebruik van synthetische cannabinoïden, zoals K2, ook bekend als Spice, die niet kunnen worden opgespoord met urineonderzoek naar drugs.13 CHS moet worden onderscheiden van andere aandoeningen die misselijkheid en braken veroorzaken, en de diagnose is er over het algemeen een van uitsluiting.
Pathofysiologie
Er zijn meerdere hypothesen met betrekking tot de pathofysiologie van CHS; maar vanwege de veelheid aan actieve chemicaliën in cannabis en het bestaan van verschillende werkingsplaatsen, is het definitieve pathofysiologische proces nog onbekend. Bovendien ontwikkelen niet alle cannabisgebruikers CHS, waardoor het nog moeilijker wordt het syndroom te beschrijven.
Het is bekend dat THC bij lage doses een anti-emetisch effect heeft, maar bij zwaar en chronisch cannabisgebruik wordt het tegenovergestelde gezien. Er is gesuggereerd dat THC zich in de loop van de tijd ophoopt vanwege het grote distributievolume. THC kan CB1-receptoren in het enterische zenuwstelsel direct activeren en de motiliteit van de maag verminderen, waardoor het risico op misselijkheid en braken bij overmatige activering toeneemt.9 Van synthetische cannabinoïden, die zowel het effect als de structuur van THC nabootsen, wordt verondersteld dat ze overstimulatie van de CB1-receptor veroorzaken vanwege hun krachtige agonistische effecten.14 Deze CB1-receptoren worden ook aangetroffen in de hypothalamus en kunnen emesis veroorzaken door de thermoregulatie te belemmeren, wat kan leiden tot verlichting van de symptomen door middel van een warm bad.9,11
Risicofactoren, klinisch beloop en diagnose
Chronisch cannabisgebruik is de belangrijkste risicofactor voor het ontstaan van CHS. Het risico van een patiënt op CHS neemt toe naarmate het gebruik van cannabis langer aanhoudt.9 Dagelijks cannabisgebruik lijkt een grotere kans op CHS te hebben dan minder frequent gebruik, maar elke hoeveelheid cannabis kan tot CHS leiden.15
CHS kent verschillende fasen, die zijn geclassificeerd als preemetisch, hyperemetisch en herstel.9,16 De preemetische fase, die maanden tot jaren kan duren, wordt gekenmerkt door misselijkheid, angst om te braken en buikpijn. Gewoonlijk verhogen cannabisgebruikers hun cannabisinname tijdens de preemetische fase in een poging de misselijkheid te verlichten.11 Tijdens de hyperemetische fase, die meestal 24 tot 48 uur duurt, ervaart de patiënt frequente misselijkheid en braken die ernstig van aard zijn. Dit kan leiden tot gewichtsverlies en acute dehydratie, mogelijk resulterend in prerenaal falen.17,18 De aanhoudende misselijkheid en braken kunnen leiden tot het ontstaan van afwijkingen in de elektrolyten.
Om de symptomen te verlichten, kunnen patiënten beginnen met warm baden, d.w.z. urenlang in een warm bad of douche blijven.11 Dit is een zelf aangeleerd gedrag dat dwangmatig wordt zodra de patiënt het voordeel ervan inziet. Warm baden kan helpen bij de thermoregulatie en de vermindering van de bloedstroom naar de maag door perifere vasodilatatie en herverdeling vanuit de splanchnische circulatie, wat leidt tot minder braken.11 Helaas kan warm baden het risico op uitdroging en acuut nierfalen vergroten.17 Warm baden moet worden beschouwd als een pathognomonisch kenmerk, omdat het niet wordt gezien bij andere aandoeningen die een verder vergelijkbare presentatie kunnen hebben. Patiënten stoppen meestal met heet baden wanneer de symptomen niet aanwezig zijn en beginnen er weer mee zodra misselijkheid en braken terugkeren na toekomstig cannabisgebruik.
Veel patiënten zoeken medische hulp voor hun symptomen tijdens de hyperemetische fase. Als gevolg daarvan kunnen patiënten uitgebreide negatieve onderzoeken ondergaan voor verschillende andere aandoeningen, zoals CVS, pancreatitis en gastroparese, die sommige symptomen van CHS kunnen nabootsen. Zodra de misselijkheid en het braken zijn verdwenen, meestal binnen 48 uur, komt de patiënt in de herstelfase. Het herstel kan variëren van dagen tot maanden en wordt geassocieerd met het stoppen van het cannabisgebruik. Als de patiënt weer begint met cannabis, keren de symptomen meestal terug.11
Het is belangrijk om de invloed van CHS op de andere ziektes van een patiënt in ogenschouw te nemen. Er zijn casusbeschrijvingen van patiënten met CHS die andere aan CHS gerelateerde medische problemen ontwikkelden dan nierfalen. Gregoire en collega’s beschreven een patiënt met een voorgeschiedenis van bipolaire manie en cannabisgebruik die CHS ontwikkelde.19 De patiënt schreef het hardnekkige braken toe aan lithium en stopte met het innemen van de lithium, waarna een manische episode optrad. Herinjectie van lithium in het ziekenhuis veroorzaakte geen extra braken, wat erop wijst dat cannabis de waarschijnlijke oorzaak was.19
Diagnostische criteria voor CHS zijn voorgesteld. Langdurig cannabisgebruik is essentieel voor de diagnose. De tijd die nodig is om CHS te ontwikkelen varieert; de meeste patiënten presenteren zich echter 1 tot 5 jaar na chronisch cannabisgebruik. Wanneer de symptomen lijken op die van CHS vóór 1 jaar chronisch cannabisgebruik, mag de diagnose niet worden uitgesloten. De belangrijkste kenmerken van CHS zijn ernstige cyclische misselijkheid en braken, het verdwijnen van de symptomen na het staken van het cannabisgebruik, verlichting door baden in heet water, epigastrische of periumbilicale buikpijn, en wekelijks cannabisgebruik. Ondersteunende kenmerken die leiden tot de diagnose CHS zijn leeftijd <50 jaar, gewichtsverlies >5 kg, ’s ochtends optreden van de symptomen, normale darmgewoonten, en normale bevindingen bij andere onderzoeken.15 TABEL 1 geeft een overzicht van veel voorkomende bevindingen die de diagnose CHS ondersteunen.14

Potentiële behandelingen
Ondersteunende zorg is geïndiceerd voor alle patiënten die zich in de hyperemetische fase van CHS presenteren. Als de patiënt dit kan verdragen, wordt orale inname van vocht aanbevolen voor hydratatie. Sommige patiënten kunnen orale vochtinname niet verdragen vanwege overmatig braken, zodat intraveneuze vochtinname geïndiceerd kan zijn voor volumedepletie die gepaard gaat met dehydratie.11 Omdat bij braken elektrolytstoornissen kunnen optreden, is controle en vervanging van elektrolyten geïndiceerd.
Compulsief warm baden is een kenmerkend aangeleerd gedrag dat patiënten kunnen gebruiken om de symptomen die gepaard gaan met CHS te minimaliseren. Zoals eerder is besproken, kan warm baden helpen bij de thermoregulatie. Een andere theorie is dat perifere vasodilatatie en herverdeling vanuit de splanchnische circulatie de bloedtoevoer naar de maag kan verminderen, wat resulteert in minder braken.11 In een enkel geval is gemeld dat de verlichting van de symptomen door warm baden na verloop van tijd kan afnemen; dit verschijnsel lijkt echter niet vaak voor te komen.20
Antiemetica zijn zonder succes gebruikt om de symptomen van CHS te verlichten. Het uitblijven van een reactie op anti-emetica zou de clinicus moeten aanzetten tot het vermoeden van CHS. In case reports, patients have had no therapeutic relief from nausea and vomiting with ondansetron, promethazine, chlorpromazine, or metoclopramide.21 In a small case series, 87.5% of patients did not respond to standard antiemetic therapy.12
Haloperidol exerts antipsychotic effects by antagonizing dopamine D2 receptors in the mesolimbic and mesocortical pathways. Haloperidol wordt van oudsher gebruikt om agitatie te behandelen; het is echter met succes gebruikt als anti-emeticum in de algemene chirurgie en oncologie. D2-receptoren zijn ook aanwezig in de chemoreceptor-triggerzone, wat deze anti-emetische eigenschappen zou kunnen verklaren. Dierstudies suggereren dat CB1 kan worden beïnvloed door haloperidol, waardoor dit middel een potentiële behandelingsoptie wordt.22,23 Witsil en Mycyk evalueerden deze hypothese retrospectief bij vier patiënten met misselijkheid en braken die refractair waren aan standaard anti-emetische therapie.21 Alle patiënten vonden verlichting binnen 1 tot 2 uur na IV-introductie van haloperidol 5 mg.21,24 Deze kleine casestudie toont aan dat haloperidol CHS-gerelateerde misselijkheid en braken voldoende kan verlichten om ziekenhuisopname te voorkomen, wat kan leiden tot kostenbesparingen voor het gezondheidszorgsysteem.19 Het risico van QTc-verlenging met haloperidol moet worden overwogen, vooral bij patiënten met elektrolytstoornissen als gevolg van overmatig braken. Aanvullende studies zijn gerechtvaardigd om de plaats van haloperidol in de therapie en de optimale dosering vast te stellen.
Stoppen met cannabis is de enige behandeling die de symptomen geassocieerd met CHS verlicht en voorkomt. In het onderzoek dat CHS voor het eerst beschreef, resulteerde onthouding van cannabis in het stoppen van misselijkheid en braken bij zeven van de tien patiënten, terwijl de anderen bleven lijden aan aanhoudende ziekte. Drie van de zeven patiënten gebruikten later weer cannabis, en de symptomen keerden binnen enkele maanden terug.10 Deze bevindingen zijn herhaald in recente case reports.12,25 Patiënten moeten worden voorgelicht over het stoppen met cannabis als symptoombestrijding, en er moeten middelen worden verstrekt om te helpen bij het stoppen.
Conclusie
Naarmate cannabis in meer staten wordt gelegaliseerd, zal het gebruik ervan waarschijnlijk toenemen en zullen er meer gevallen van CHS worden gemeld. Artsen moeten CHS vermoeden bij patiënten met een voorgeschiedenis van cannabis- of synthetisch cannabinoïdengebruik en symptomen als hardnekkige misselijkheid en braken, samen met meldingen van het gebruik van warm baden voor symptoombestrijding. Dit vermoeden zou uitgebreide en kostbare onderzoeken naar andere aandoeningen kunnen voorkomen. Apothekers hebben een rol bij het adviseren van patiënten over de risico’s van cannabisgebruik en bij het doorverwijzen van patiënten met CHS-symptomen voor passende vervolgzorg. Casusrapporten in de literatuur hebben risicofactoren voor CHS geïdentificeerd. Helaas wordt CHS relatief weinig gerapporteerd en is het exacte mechanisme onbekend. Diagnose en behandeling van CHS zijn momenteel gebaseerd op kleine meldingen van gevallen. Informatie moet geëvalueerd blijven worden naarmate deze beschikbaar komt, om een juiste behandeling te garanderen.
1. Nationaal Instituut voor Drugsmisbruik (NIDA). Wat is marihuana? www.drugabuse.gov/publications/research-reports/marijuana/what-marijuana. Accessed August 25, 2016.
2. NIDA. What is the scope of marijuana use in the United States? www.drugabuse.gov/publications/research-reports/marijuana/what-scope-marijuana-use-in-united-states. Accessed August 25, 2016.
3. Kim HS, Monte AA. Colorado cannabis legalization and its effect on emergency care. Ann Emerg Med. 2016;68:71-75.
4. Cerdá M, Wall M, Keyes KM, et al. Medical marijuana laws in 50 states: investigating the relationship between state legalization of medical marijuana and marijuana use, abuse and dependence. Drug Alcohol Depend. 2012;120:22-27.
5. CNN Money. Waar wiet legaal is. http://money.cnn.com/interactive/news/economy/marijuana-legalization-map/index.html. Accessed August 25, 2016.
6. Marijuana Policy Project. 2016 marihuana policy reform legislation. www.mpp.org/states/key-marijuana-policy-reform. Accessed November 13, 2016.
7. NIDA. Hoe veroorzaakt marihuana zijn effecten? www.drugabuse.gov/publications/research-reports/marijuana/how-does-marijuana-produce-its-effects. Accessed August 2016.
8. Manzanares J, Julian MD, Carrascosa A. Rol van het cannabinoïde systeem in pijncontrole en therapeutische implicaties voor het beheer van acute en chronische pijn episodes. Curr Neuropharmacol. 2006;4:239-257.
9. Galli JA, Sawaya RA, Friedenberg FK. Cannabinoïde hyperemesis syndroom. Curr Drug Abuse Rev. 2011;4:
241-249.
10. Allen JH, de Moore GM, Heddle R, Twartz JC. Cannabinoid hyperemesis: cyclische hyperemesis in associatie met chronisch cannabis misbruik. Gut. 2004;53:1566-1570.
11. Ruffle JK, Bajgoric S, Samra K, et al. Cannabinoid hyperemesis syndrome: an important differential diagnosis of persistent unexplained vomiting. Eur J Gastroenterol Hepatol. 2015;27:1403-1408.
12. Soriano-Co M, Batke M, Cappell MS. The cannabis hyperemesis syndrome characterized by persistent nausea and vomiting, abdominal pain, and compulsive bathing associated with chronic marijuana use: a report of eight cases in the United States. Dig Dis Sci. 2010;55:3113-3119.
13. Ukaigwe A, Karmacharya P, Donato A. A gut gone to pot: a case of cannabinoid hyperemesis syndrome due to K2, a synthetic cannabinoid. Case Rep Emerg Med. 2014;2014:167098.
14. Hopkins CY, Gilchrist BL. Een geval van cannabinoïde hyperemesis syndroom veroorzaakt door synthetische cannabinoïden. J Emerg Med. 2013;45:544-546.
15. Simonetto DA, Oxentenko AS, Herman ML, Szostek JH. Cannabinoïde hyperemesis: een case serie van 98 patiënten. Mayo Clin Proc. 2012;87:114-119.
16. Lu ML, Agito MD. Cannabinoïd hyperemesis syndroom: marihuana is zowel antiemetisch als proemetisch. Cleve Clin J Med. 2015;82:429-434.
17. Habboushe J, Sedor J. Cannabinoïd hyperemesis acuut nierfalen: een veelvoorkomend sequela van het cannabinoïd hyperemesis syndroom. Am J Emerg Med. 2014;32:690.e1-e2.
18. Srihari P, Liu M, Punzell S, et al. Cannabinoïd hyperemesis syndroom geassocieerd met dwangmatig douchen en acuut nierletsel. Prim Care Companion CNS Disord. 2016;18(1).
19. Gregoire P, Tau M, Robertson D. Cannabinoïd hyperemesis syndroom en het begin van een manische episode. BMJ Case Rep. 2016;2016.
20. Bagdure S, Smalligan RD, Sharifi H, Khandheria B. Afnemend effect van dwangmatig baden bij cannabinoïde hyperemesis. Am J Addict. 2012;21:184-185.
21. Witsil JC, Mycyk MB. Haloperidol, een nieuwe behandeling voor het cannabinoïd hyperemesis syndroom. Am J Ther. 2014 Nov 12 .
22. Schulze DR, Carroll FI, McMahon LR. Interacties tussen dopamine transporter en cannabinoïde receptor liganden in rhesus apen. Psychopharmacology (Berl). 2012;222:425-438.
23. Desai RI, Thakur GA, Vemuri VK, et al. Analyse van tolerantie en gedragsmatige/fysieke afhankelijkheid tijdens chronische CB1 agonist behandeling: effecten van CB1 agonisten, antagonisten, en niet-cannabinoïde geneesmiddelen. J Pharmacol Exp Ther. 2013;344:319-328.
24. Hickey JL, Witsil JC, Mycyk MB. Haloperidol voor de behandeling van het cannabinoïde hyperemesis syndroom. Am J Emerg Med. 2013;31:1003.e5-e6.
25. Pélissier F, Claudet I, Gandia-Mailly P, et al. Cannabis hyperemesis syndroom op de spoedeisende hulp: hoe kan een gespecialiseerd verslavingsteam nuttig zijn? Een pilootstudie. J Emerg Med. 2016;51:544-551.