


Spis treści
Patofizjologia PCOS
Kryteria diagnostyczne
Oporność na insulinę i leptynę
Autorzy
Wielu z nas nie zdaje sobie sprawy z tego, jak dobrze działa skomplikowany system pętli sprzężenia zwrotnego w naszym układzie hormonalnym układu rozrodczego, dopóki nie zostanie on w jakiś sposób zakłócony. Zespół policystycznych jajników (Polycystic ovarian syndrome – PCOS) jest tego przykładem. Jest to zaburzenie charakteryzujące się szeregiem objawów, występujące powszechnie u pacjentek zgłaszających się do klinik leczenia niepłodności, dotykające 5-10% kobiet w wieku rozrodczym. Szacuje się, że 90% przypadków anowulacyjnych jest związanych z PCOS. Oprócz negatywnego wpływu na parametry metaboliczne i owulację, zespół ten wiąże się również z wieloma problemami natury psychicznej (takimi jak depresja i lęk) u kobiet, które go mają. W części 1 omówimy patofizjologię PCOS, jego kryteria diagnostyczne oraz insulino- i leptynooporność. W części 2 zajmiemy się postępowaniem w PCOS, implikacjami psychologicznymi oraz wyjątkową rolą klinicysty we wspieraniu pacjentki z PCOS.
Patofizjologia PCOS
U kobiet owulacyjnych, pod wpływem prawidłowo funkcjonującej osi podwzgórze-przysadka-jajnik (HPO), cykl menstruacyjny charakteryzuje się wzrostem i rozwojem (zwykle) pojedynczego pęcherzyka, który jest wyodrębniany z kohorty (grupy pęcherzyków) danego miesiąca. W odpowiedzi na stymulację GnRH, przednia część przysadki mózgowej wydziela dwie ważne gonadotropiny: Follicle Stimulating Hormone (FSH) i Luteinizing Hormone (LH). FSH działa na jajnik, wspomagając wzrost i dojrzewanie małych pęcherzyków. Dominującym pęcherzykiem w danym miesiącu jest ten, który nabył najwięcej receptorów FSH. Pęcherzyk ten będzie nadal wzrastał i dojrzewał kosztem pozostałych małych pęcherzyków, które następnie zostają wchłonięte przez organizm (ale nadal są odliczane od całkowitej ilości komórek jajowych kobiety). Wzrost dominuj±cego pęcherzyka generuje produkcję estradiolu, a podwyższony poziom estrogenu sygnalizuje zaprzestanie produkcji FSH poprzez system ujemnego sprzężenia zwrotnego, jednak wysoki i trwały poziom estrogenu wywoła jednorazowy przypływ LH, który powoduje wyst±pienie owulacji.
W przypadku kobiety z PCOS oś HPO nie przejawia normalnej funkcjonalności. Pulsacyjny hormon GnRH jest zmieniony, co skutkuje zwiększoną aktywnością LH przez przysadkę mózgową. Ten wzrost LH zwiększa stymulację komórek theca (patrz Ryc. 1), które wytwarzają androstenedion i testosteron, dwa androgeny, a wynikające z tego hiperandrogenne środowisko jajnika wyklucza normalny wzrost pęcherzyków, ich dojrzewanie i owulację. Jajnik staje się wówczas złożony z wielu małych, antralnych pęcherzyków, które nigdy nie stają się dominujące. Gromadzenie się tych pęcherzyków może powodować zwiększenie rozmiarów jajników i generować nieznacznie podwyższone podstawowe stężenie estrogenów w surowicy. Nadal nie wiadomo, dlaczego PCOS występuje i kogo dotyka, ale uważa się, że czynniki genetyczne i środowiskowe mają złożony wpływ na jego pojawienie się i objawy kliniczne.
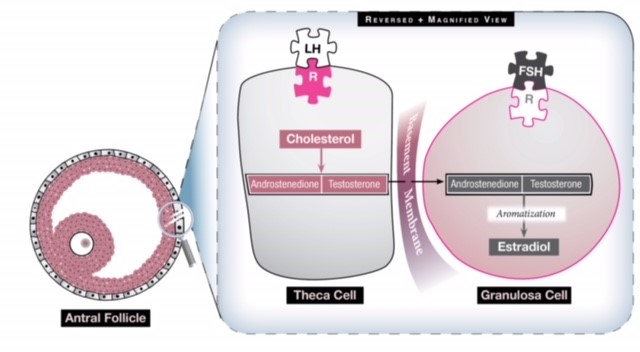
Fig 1: W jajniku znajdują się dwie komórki, które przyczyniają się do produkcji estrogenu i działają synergicznie. Komórka theca konwertuje cholesterol na dwa androgeny (androstenedion i testosteron) pod wpływem LH. Te androgeny następnie przechodzą przez błonę podstawną do komórki ziarnistej, która pod wpływem FSH przekształca je w estrogeny w procesie zwanym aromatyzacją. Nadmierna stymulacja LH generuje więc więcej androgenów, niż może być przekształconych w estrogeny, tak że poziom estrogenów nigdy nie staje się na tyle wysoki, by wygenerować przypływ LH, a jajnik znajduje się w środowisku hiperandrogenicznym.
Kryteria diagnostyczne
PCOS nie jest definiowany ani diagnozowany przez jeden prosty objaw i jest często diagnozą z wykluczenia dla kobiet, które mają oligo-owulację i dowody na hiperandrogenizm (takie jak łysienie trądzikowe i hirsutyzm (wzrost i tekstura włosów o męskim wzorze) po wykluczeniu innych zaburzeń. Dotyka to kobiet o różnych kształtach, rozmiarach i pochodzeniu. Chociaż objawy mogą pojawić się w momencie menarche, większość lekarzy niechętnie diagnozuje PCOS u stosunkowo świeżo miesiączkujących nastolatek, ponieważ nieregularność cyklu miesiączkowego jest normalna w pierwszym roku po menarche i może ustąpić z czasem. Najczęściej stosowane obecnie kryteria diagnostyczne zostały zweryfikowane podczas międzynarodowych warsztatów ekspertów w Rotterdamie, w Holandii, w 2003 r. i są nazywane Kryteriami Rotterdamskimi, gdzie ustalono, co następuje: PCOS może być rozpoznany tylko wtedy, gdy u pacjentki występują co najmniej dwie z trzech cech: oligo/owulacja, hiperandrogenizm (biochemiczny lub kliniczny) oraz obecność policystycznych jajników w badaniu ultrasonograficznym.Hiperandrogenizm jest rozpoznawany klinicznie (przez klinicystę obserwującego objawy androgenne) lub biochemicznie (np. podwyższony poziom wolnego testosteronu w surowicy).
Kryteria te zostały zweryfikowane w 2018 roku przez międzynarodowy komitet, który wprowadził kilka zmian. Po pierwsze, ze względu na dostępność czułych przezpochwowych aparatów ultrasonograficznych, polipowatość jajników (PCOM) charakteryzuje się obecnością 20 lub więcej pęcherzyków (<10 mm) w którymkolwiek z jajników lub objętością jajnika ≥ 10 ml w którymkolwiek z jajników, widoczną w przezpochwowym badaniu ultrasonograficznym, często zlokalizowaną na obrzeżach jajnika (lub jajników). W wytycznych z 2018 roku stwierdzono również, że jeśli u kobiety występują nieregularne cykle miesiączkowe i hiperandrogenizm, badanie ultrasonograficzne nie jest konieczne do postawienia rozpoznania, choć wielu klinicystów nadal preferuje jego wykonanie. Poziom hormonu anty-mullerowskiego (AMH) jest często podwyższony u pacjentek z PCOS, chociaż nie jest to specyficzne dla PCOS, ponieważ podwyższony poziom można znaleźć u kobiet bez tego schorzenia. U kobiet dotkniętych PCOS podwyższony poziom AMH odzwierciedla większą liczbę pęcherzyków zatrzymanych w fazie przedantralnej i antralnej, którym nie udaje się wywołać owulacji.
Inne schorzenia, które mogą powodować nieregularne cykle miesiączkowe (ciąża, niedoczynność i nadczynność tarczycy, niewydolność jajników i hiperprolaktynemia) oraz hiperandrogenizm (wrodzony przerost nadnerczy, guz nadnerczy i guz wydzielający androgeny) muszą być najpierw wykluczone, Dlatego też oprócz stężenia bHCG w surowicy krwi oznacza się podstawowe stężenia FSH i LH, hormonu tyreotropowego (TSH), prolaktyny, testosteronu całkowitego i wolnego, 17hydroksyprogesteronu (17OHP) oraz siarczanu dehydroepiandrosteronu (DHEAS). Jedną z najtrudniejszych diagnoz różnicowych jest odróżnienie kobiety z funkcjonalną amenorrhea hypothalamic (FHA) od szczupłej kobiety z PCOS. Klasycznie kobiety z FHA mają niskie BMI, ale może być ono również w zakresie niskim/normalnym. Oba schorzenia charakteryzują się anowulacją i jajnikami, które wydają się mieć wiele małych pęcherzyków w stanie spoczynku. Chociaż hiperandrogenizm nie jest składnikiem FHA, kobiety z tym schorzeniem mogą mieć hirsutyzm ze względu na pochodzenie etniczne, co dodatkowo gmatwa obraz kliniczny. Jednym ze sposobów na odróżnienie FHA od PCOS jest badanie krwi i badanie ultrasonograficzne. Kobiety z FHA często mają niskie lub prawidłowe podstawowe stężenie FSH i LH (z powodu niedostatecznej stymulacji jajników) oraz niski poziom estrogenów, podczas gdy kobiety z PCOS typowo mają podwyższone stężenie LH w surowicy i niskie lub prawidłowe stężenie FSH. W badaniu ultrasonograficznym macica i jajniki kobiet z FHA są małe lub małe/normalne, podczas gdy kobiety z PCOS mają zwykle zwiększoną objętość jajników (>10 ml).Pojawiają się badania dotyczące możliwego związku pomiędzy FHA i PCOS, ponieważ nie wszystkie kobiety prezentują cechy charakterystyczne dla obu tych schorzeń, a FHA i PCOS mają pewne nakładające się cechy.
Oporność na insulinę i leptynę
Chociaż diagnoza insulinooporności (IR) nie jest częścią Kryteriów Rotterdamskich, jest ona bardzo rozpowszechniona u kobiet z PCOS. Podwyższony wskaźnik BMI zwiększa szansę, że kobieta z PCOS ma IR, ale nawet kobiety bez otyłości z PCOS są znacznie bardziej narażone na rozwój insulinooporności niż ich rówieśniczki bez PCOS. Oprócz konsekwencji zdrowotnych IR (takich jak zespół metaboliczny i cukrzyca typu 2), zaostrza ona również i przyczynia się do hiperandrogenizmu w populacji pacjentów, którzy już z nim cierpią.
Złotym standardem diagnozowania insulinooporności jest stosowanie hiperinsulinemicznej klamry euglikemicznej, która musi być wykonywana w warunkach szpitalnych. Dla większości z nich jest to nierozsądne, dlatego wykonuje się pośrednie badania w kierunku IR. U kobiet z PCOS w warunkach klinicznych przedkoncepcyjnych sugeruje się wykonanie doustnego testu tolerancji glukozy (OGTT) ze względu na wysokie ryzyko rozwoju upośledzonej tolerancji glukozy i cukrzycy ciążowej u kobiet z PCOS w ciąży. Mimo, że jest to badanie czasochłonne, jest ono preferowane w stosunku do oznaczania stężenia glukozy i insuliny na czczo, ponieważ pozwala zdiagnozować upośledzoną tolerancję glukozy na wcześniejszym etapie.U kobiet z PCOS, które nie należą do kategorii wysokiego ryzyka (tj, BMI<25 kg/m2, nie starają się zajść w ciążę, brak osobistej lub rodzinnej historii upośledzonej tolerancji glukozy) uzyskanie przynajmniej wyjściowych poziomów glukozy, insuliny i hemoglobinyA1c na czczo może być pomocne w celu uzyskania „migawkowego” obrazu stanu glikemii tej pacjentki.
Kiedy kobieta ma PCOS, nadwaga lub otyłość nasilają konsekwencje metaboliczne. Białe komórki tłuszczowe są aktywne metabolicznie. Na normalnym poziomie pełnią one funkcję ochronną, ponieważ stanowią bezpieczne schronienie dla lipidów i utrzymują tłuszcz z dala od narządów. Kiedy komórek tłuszczowych jest zbyt wiele, mogą zostać przeciążone i pęknąć, uwalniając kwasy tłuszczowe do krwiobiegu, co może mieć wpływ na wszystkie organy. Te komórki tłuszczowe „utknęły” między komórkami w narządach i powodują ich sztywność, uszkodzenie, mniejszą funkcjonalność i przewlekły stan zapalny. Nierzadko diagnozuje się „stłuszczenie wątroby” u kobiet z PCOS, które są otyłe, ponieważ wątroba jest szczególnie wrażliwa. Ponadto nadmiar tkanki tłuszczowej może utrwalić istniejącą hiperinsulinemię i insulinooporność poprzez zaburzenie delikatnej równowagi cytokin i hormonów produkowanych przez tkankę tłuszczową (patrz Rycina 2), na przykład zmniejszenie produkcji cytokin zwiększających wrażliwość na insulinę, a zwiększenie tych, które promują stan zapalny i insulinooporność. Nadmiar insuliny dodatkowo przyczynia się do otyłości brzusznej i hiperandrogenizmu, tworząc błędne koło u pacjentów z PCOS, które może być trudne do pokonania.
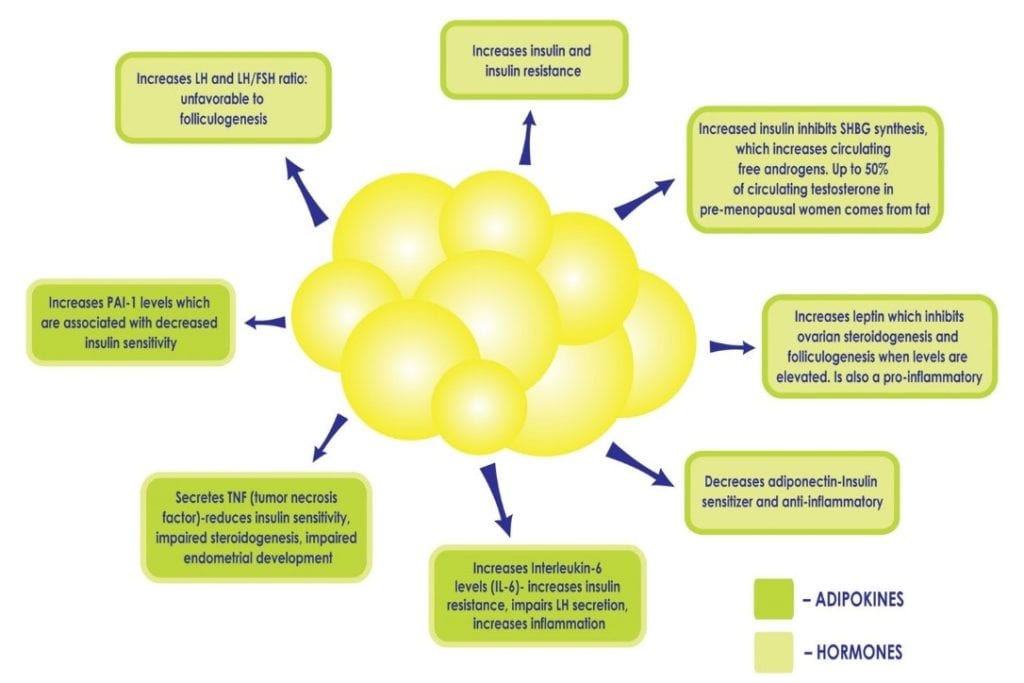
Figura 2: Zwiększona otyłość, a następnie wzrost komórek tłuszczowych, może utrwalić hiperinsulinemię i insulinooporność poprzez zakłócenie delikatnej równowagi hormonów produkowanych przez tkankę tłuszczową, takich jak zmniejszenie produkcji adiponektyny, cytokiny, która zwiększa wrażliwość na insulinę i zwiększenie innych, które promują stan zapalny.
Oprócz insulinooporności, pacjenci z PCOS i otyłością mogą również cierpieć z powodu tego, co niektórzy określają jako oporność na leptynę. Niektóre badania wykazały, że poziom leptyny jest wyższy u otyłych pacjentek z PCOS w porównaniu z pacjentkami szczupłymi. Leptyna jest białkiem produkowanym przez tkankę tłuszczową, które reguluje równowagę energetyczną organizmu i apetyt. Przy prawidłowym funkcjonowaniu, wzrost leptyny sygnalizuje mózgowi zmniejszenie apetytu danej osoby, a spadek leptyny działa odwrotnie, sygnalizuje mózgowi zwiększenie apetytu w celu dostarczenia paliwa potrzebnego do uzyskania energii. U wielu pacjentek z PCOS i otyłością system ten jest jednak wadliwy i pomimo zwiększonego stężenia leptyny wtórnie do wzrostu tkanki tłuszczowej, skuteczność leptyny spada, co prowadzi do leptynooporności. Leptynooporność jest uważana za ważny czynnik ryzyka w patogenezie nadwagi i otyłości, ponieważ organizm pozostaje niewrażliwy na podwyższone stężenie leptyny i sygnalizuje kobiecie, że nawet po jedzeniu jest nadal głodna/nie najedzona. Wiele kobiet z PCOS skarży się, że „nigdy nie czuje się syta” z powodu tej oporności i kontynuuje jedzenie, co prowadzi do wzrostu tkanki tłuszczowej, która powoduje zwiększoną oporność na leptynę i utrwala ten szkodliwy cykl. W rezultacie nadwaga i otyłość są powszechne u kobiet z PCOS, a utrata wagi może wydawać się niemożliwa, ponieważ intuicyjne jedzenie nie jest skuteczne, kiedy wskazówki dotyczące głodu i sytości są niewiarygodne.
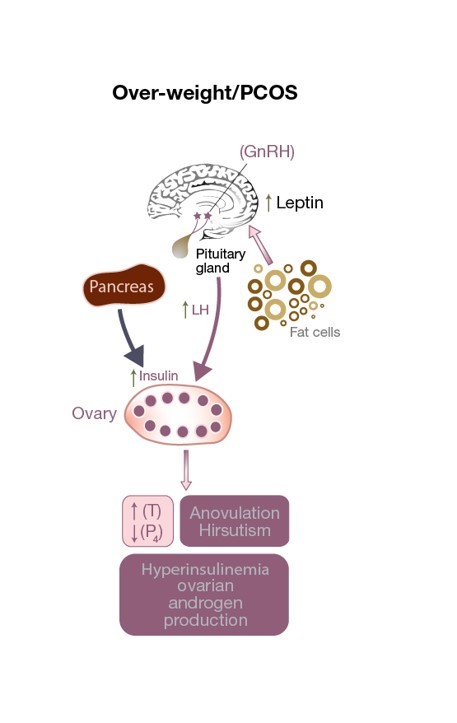
Figura 3: Zaburzenia osi HPO u pacjentki z PCOS. Nadmiar LH stymuluje komórki theca, powodując wzrost poziomu testosteronu, androgenne środowisko jajników oraz anowulację (skutkującą niskim poziomem progesteronu). Podwyższony poziom leptyny, spowodowany nadmiarem komórek tłuszczowych, wpływa na wydzielanie GnRH. Podwyższony poziom insuliny przyczynia się do hiperandrogenizmu.
Zaburzone wydzielanie leptyny nie tylko wpływa na masę ciała, ale może mieć szkodliwy wpływ na owulację (patrz Ryc. 3), a nawet na zapłodnienie u pacjentek z PCOS o prawidłowej masie ciała. Zmienia ona uwalnianie GnRH z podwzgórza, zmniejszając stymulację przedniej części przysadki mózgowej (a tym samym wydzielanie FSH i LH) oraz uniemożliwiając rozwój dojrzałej komórki jajowej. Ponadto, komórki ziarniste przechowują i produkują leptynę, a wysoki poziom leptyny zmniejsza ich zdolność do aromatyzacji, co ostatecznie zaburza zdolność dominującego pęcherzyka do produkcji odpowiedniej ilości estrogenów (patrz Ryc. 1). Niewielkie, obserwacyjne badanie wykazało bezpośrednią korelację pomiędzy stężeniem leptyny w płynie pęcherzykowym (leptyna FF) (która została skorelowana z odsetkiem zapłodnień) u szczupłych kobiet z PCOS, które poddały się IVF, w porównaniu do normalnie owulujących, dobranych wagowo kobiet.
Autorzy
Jaclyn Carr, BSN
Brianna Giannotte, BSN
Monica Moore, MSN, RNC
Szczególne podziękowania dla Neila Chapella, MD za pomoc w edycji tego artykułu.
You can visit the FertilityNurse Newsletter website here
Want to be notified about upcoming Fertility Newsletter posts here at The ObG Project?
Get the ObG Insider e-Newsletter ”



![]()