US Pharm. 2016;41(12):HS16-HS19.
ABSTRACT: Marijuana, sau canabisul, este în mod obișnuit considerată a fi o substanță benignă fără efecte adverse; cu toate acestea, sindromul de hiperemeză canabinoidă (CHS) este o sechelă a consumului cronic de canabis. Clinicienii ar trebui să suspecteze cu tărie CHS la consumatorii de canabis pe termen lung care prezintă greață și vărsături intratabile și ale căror simptome sunt ameliorate prin îmbăiere în apă caldă. O lipsă de răspuns la antiemetice ar trebui să ajute la diagnosticarea CHS. Singurul tratament pentru a rezolva cu succes CHS este abstinența de la canabis, deși haloperidolul este în curs de studiu ca o potențială opțiune de tratament. Un pacient care se confruntă cu CHS ar trebui sfătuit să evite canabisul, deoarece consumul continuu va declanșa simptome suplimentare.
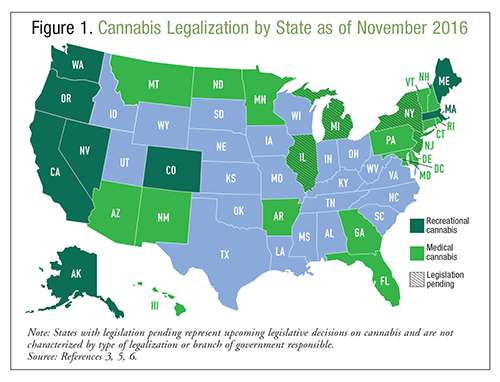
Marijuana, sau canabis, este un produs natural derivat dintr-o plantă de cânepă cunoscută sub numele de Cannabis sativa; este considerat în mod obișnuit o substanță benignă, fără efecte adverse.1 Canabisul poate fi fumat, vaporizat sau ingerat pentru intoxicare sau pentru beneficii terapeutice și este utilizat de secole în aceste scopuri. Potrivit National Survey on Drug Use and Health din 2014, >22 de milioane de americani au consumat canabis în luna precedentă, ceea ce face ca această substanță să fie cel mai frecvent utilizat drog ilicit.2 Se preconizează că utilizarea canabisului în Statele Unite va continua să crească datorită creșterii ratelor de legalizare.3 Potrivit National Epidemiologic Survey on Alcohol and Related Conditions, locuitorii statelor care au legalizat canabisul medical au de două ori mai multe șanse de a aproba consumul de canabis decât locuitorii statelor fără legalizare.4 În prezent, canabisul poate fi utilizat în scopuri medicinale în 28 de state și, de asemenea, poate fi utilizat în scop recreativ în opt dintre acestea. Consultați FIGURA 1 pentru informații privind legalitatea canabisului pe întreg teritoriul SUA în momentul redactării acestui document.3,5,6 În plus față de legalizare, 21 de state și Districtul Columbia au dezincriminat posesia de cantități mici de canabis. Urgențele medicale legate de consumul de canabis au crescut cu 29% din 2009 până în 2011; nu se știe dacă această creștere s-a datorat potenței canabisului, creșterii legalizării sau altor factori.1
Corpul uman are un sistem canabinoidic intrinsec, cunoscut sub numele de sistem endocanabinoid, care conține neurotransmițători (de exemplu, anandamida) care reglează apetitul, somnul, durerea, emoțiile și mișcarea.7,8 Canabinoidul se referă la orice compus care afectează receptorii canabinoizi din organism. Receptorii care servesc în scopuri terapeutice includ canabinoidele de tip 1 și 2 (CB1, CB2). CB1 se găsește în cantități mari în creier și în cantități mai mici în țesuturile nervoase spinale și periferice, în timp ce CB2 se găsește în cantități mari în țesuturile periferice și în sistemul imunitar.8
Cannabisul conține >100 de substanțe chimice, dintre care delta-9-tetrahidrocannabinolul (THC) este cel mai activ compus. Deoarece se leagă de CB1, THC este responsabil pentru efectul intoxicant al canabisului.1 Alte canabinoide prezente în canabis includ canabidiolul și canabigerolul, care nu sunt psihoactive. Datorită gamei largi de activități pe care sistemul intrinsec le afectează, multe persoane au folosit canabinoidele pentru intoxicare și în scopuri terapeutice.
Sindromul de hiperemeză canabinoidă
Canabisul a fost folosit pentru a stimula apetitul în tratamentul anorexiei și epuizării asociate cu HIV/SIDA și pentru a ameliora greața și vărsăturile induse de chimioterapie. Deși canabisul poate fi utilizat pentru a trata greața și vărsăturile, acesta poate provoca, de asemenea, un sindrom paradoxal de greață și vărsături cunoscut sub numele de sindrom de hiperemeză canabinoidă (CHS). CHS este un diagnostic clinic caracterizat de consumul cronic de canabis.9 O trăsătură unică a CHS este greața și vărsăturile ciclice care pot să nu răspundă la terapia antiemetică standard, dar răspund la băile fierbinți compulsive.3,9 Primul raport de caz care documentează CHS (2004) a descris nouă pacienți din Australia. Consumul cronic de canabis a avut loc înainte de prezentare, iar simptomele au inclus greață și vărsături. Majoritatea pacienților au raportat că făceau baie în apă caldă pentru a atenua simptomele. Încetarea consumului de canabis a dus la rezolvarea bolii, în timp ce pacienții care au continuat să consume canabis au rămas bolnavi.10 De atunci, au fost publicate rapoarte de caz și serii suplimentare care descriu în continuare CHS; cu toate acestea, niciun studiu randomizat și controlat nu a evaluat-o sau definit-o.
În Colorado, ratele de CHS s-au dublat din 2009, când canabisul a fost legalizat acolo.3 Cu toate acestea, este important de remarcat faptul că CHS rămâne adesea nerecunoscută de către clinicieni, ceea ce poate duce la un bilanț extins și costisitor al pacientului. Diagnosticul poate fi dificil, iar SHC poate fi diagnosticat greșit ca multe alte tulburări, inclusiv sindromul de vărsături ciclice (CVS). Deși unii pacienți care consumă marijuana prezintă CVS, există mai mulți factori de diferențiere între CVS și CHS. CVS implică, de obicei, un istoric personal sau familial de migrene, un istoric de tulburări psihiatrice și lipsa băilor fierbinți compulsive.11 Pacienții cu CHS se prezintă adesea la departamentul de urgență (ED) din cauza simptomelor. Un raport de caz realizat de Soriano-Co și colegii săi a demonstrat că pacienții diagnosticați cu CHS au avut mai multe șanse de a avea vizite frecvente la un clinician, vizite la Urgențe și spitalizări.12 În medie, un pacient a avut cinci vizite la un clinician, șapte vizite la Urgențe și trei spitalizări înainte de a fi diagnosticat, ceea ce indică faptul că pacienții cu CHS ar putea fi văzuți în orice cadru de îngrijire.12 Un alt factor care complică diagnosticul este utilizarea canabinoizilor sintetici, cum ar fi K2, cunoscut și sub numele de Spice, care nu poate fi detectat în testele de depistare a drogurilor în urină.13 CHS trebuie diferențiată de alte afecțiuni care provoacă greață și vărsături, iar diagnosticul este, în general, unul de excludere.
Fiziopatologie
Există mai multe ipoteze cu privire la fiziopatologia CHS; cu toate acestea, din cauza multitudinii de substanțe chimice active din canabis și a existenței diferitelor locuri de acțiune, procesul fiziopatologic definitiv este necunoscut. În plus, nu toți consumatorii de canabis dezvoltă CHS, ceea ce cauzează dificultăți suplimentare în descrierea sindromului.
La doze mici, se știe că THC exercită un efect antiemetic, dar în cazul consumului intensiv și cronic de canabis, se observă contrariul. S-a sugerat că THC se acumulează în timp din cauza volumului său mare de distribuție. THC poate activa în mod direct receptorii CB1 din sistemul nervos enteric și reduce motilitatea gastrică, crescând riscul de greață și vărsături în cazul unei activări excesive.9 Se presupune că canabinoizii sintetici, care imită atât efectul, cât și structura THC-ului, provoacă o suprastimulare a receptorului CB1 din cauza efectelor lor agoniste puternice.14 Acești receptori CB1 se găsesc, de asemenea, în hipotalamus și pot induce emeză prin afectarea termoreglementării, ceea ce duce la o potențială ameliorare a simptomelor prin băi fierbinți.9,11
Factori de risc, evoluție clinică și diagnostic
Consumul cronic de canabis este principalul factor de risc pentru dezvoltarea SHC. Riscul unui pacient de CHS crește odată cu consumul prelungit de canabis.9 Consumul zilnic de canabis pare să fie mai probabil să provoace CHS decât consumul mai puțin frecvent; cu toate acestea, orice cantitate de canabis poate duce la CHS.15
CHS are mai multe faze, care au fost clasificate ca fiind preemetice, hiperemetice și de recuperare.9,16 Faza preemetică, care poate dura de la luni până la ani, este caracterizată de greață, teamă de vărsături și disconfort abdominal. În mod obișnuit, consumatorii de canabis își măresc consumul de canabis în timpul fazei preemetice în încercarea de a atenua greața.11 În timpul fazei hiperemetice, care durează de obicei între 24 și 48 de ore, pacientul experimentează greață și vărsături frecvente, care sunt de natură severă. Acest lucru poate duce la pierdere în greutate și deshidratare acută, putând duce la insuficiență prerenală.17,18 Greața și vărsăturile persistente pot provoca apariția unor anomalii electrolitice.
Pentru a ameliora simptomele, pacienții pot începe să facă băi fierbinți – adică să rămână într-o baie sau duș fierbinte timp de ore întregi.11 Acesta este un comportament învățat de la sine, care devine compulsiv odată ce pacientul își dă seama de beneficii. Băile fierbinți pot ajuta la termoreglare și la reducerea fluxului sanguin către stomac prin afectarea vasodilatației periferice și redistribuirea din circulația splanhnică, ceea ce duce la scăderea vărsăturilor.11 Din păcate, băile fierbinți pot crește riscul de deshidratare și de insuficiență renală acută.17 Băile fierbinți ar trebui să fie considerate o trăsătură patognomonică, deoarece nu sunt observate în cazul altor afecțiuni care pot avea o prezentare altfel similară. De obicei, pacienții întrerup băile fierbinți atunci când simptomele nu sunt prezente și le încep din nou odată ce greața și vărsăturile reapar după un viitor consum de canabis.
Mulți pacienți caută asistență medicală pentru simptomele lor în timpul fazei hiperemetice. Ca urmare, pacienții pot fi supuși unor analize negative extinse pentru diverse alte afecțiuni, cum ar fi CVS, pancreatită și gastropareză, care pot mima unele simptome ale CHS. Odată ce greața și vărsăturile dispar, de obicei în 48 de ore, pacientul intră în faza de recuperare. Recuperarea poate varia de la câteva zile la câteva luni și este asociată cu încetarea consumului de canabis. Dacă pacientul reia consumul de canabis, simptomele revin de obicei.11
Este important să se ia în considerare impactul SHC asupra altor stări de boală ale pacientului. Există rapoarte de caz de pacienți cu SHC care au dezvoltat probleme medicale legate de SHC, altele decât insuficiența renală. Gregoire și colegii au descris un pacient cu antecedente de manie bipolară și consum de canabis care a dezvoltat CHS.19 Pacientul a atribuit vărsăturile intratabile litiului și a încetat să ia litiu, iar apoi a apărut un episod maniacal. Reinițierea litiului în spital nu a declanșat vărsături suplimentare, ceea ce indică faptul că canabisul a fost cauza probabilă.19
Au fost propuse criterii de diagnostic pentru CHS. Consumul de canabis pe termen lung este esențial pentru diagnostic. Perioada de timp necesară pentru a dezvolta SHC variază; totuși, majoritatea pacienților se prezintă între 1 și 5 ani după consumul cronic de canabis. Prezentarea cu simptome similare cu cele ale CHS înainte de 1 an de consum cronic de canabis nu ar trebui să excludă diagnosticul. Caracteristicile majore ale CHS includ greață și vărsături ciclice severe, rezolvarea simptomelor la încetarea consumului de canabis, ameliorarea obținută prin îmbăiere în apă caldă, dureri abdominale epigastrice sau periombilicale și consumul săptămânal de canabis. Caracteristicile de susținere care conduc la un diagnostic de SHC includ vârsta <50 de ani, pierderea în greutate >5 kg, apariția simptomelor dimineața, obiceiuri intestinale normale și rezultate normale la alte analize.15 TABELUL 1 rezumă constatările comune care susțin diagnosticul de SHC.14

Tratamente potențiale
Îngrijirile de susținere sunt indicate pentru toți pacienții care se prezintă în faza hiperemetică a SHC. Dacă pacientul o poate tolera, se recomandă administrarea orală de lichide pentru hidratare. Unii pacienți nu pot tolera hidratarea pe cale orală din cauza vărsăturilor excesive, astfel încât fluidele intravenoase pot fi indicate pentru depleția de volum asociată cu deshidratarea.11 Deoarece tulburările electrolitice pot apărea odată cu vărsăturile, este indicată monitorizarea și înlocuirea electroliților.
Băile fierbinți compulsive sunt un comportament învățat caracteristic pe care pacienții îl pot folosi pentru a minimiza simptomele asociate cu SHC. După cum s-a discutat anterior, baia caldă poate ajuta la termoreglare. O altă teorie este că vasodilatația periferică și redistribuirea din circulația splanhnică pot reduce fluxul sanguin către stomac, ceea ce duce la diminuarea vărsăturilor.11 Un singur raport de caz a indicat faptul că ameliorarea simptomelor prin baie fierbinte poate scădea în timp; cu toate acestea, acest fenomen pare să fie neobișnuit.20
Antiemeticele au fost utilizate fără succes pentru ameliorarea simptomelor de CHS. Lipsa de răspuns la antiemetice ar trebui să determine clinicianul să suspecteze CHS. În rapoartele de caz, pacienții nu au avut nicio ameliorare terapeutică a grețurilor și vărsăturilor cu ondansetron, prometazină, clorpromazină sau metoclopramidă.21 Într-o serie mică de cazuri, 87,5% dintre pacienți nu au răspuns la terapia antiemetică standard.12
Haloperidolul exercită efecte antipsihotice prin antagonizarea receptorilor de dopamină D2 în căile mezolimbice și mezocorticale. Haloperidolul este utilizat în mod tradițional pentru a trata agitația; cu toate acestea, a fost utilizat cu succes ca antiemetic în chirurgia generală și în oncologie. Receptorii D2 sunt, de asemenea, prezenți în zona de declanșare a chemoreceptorilor, ceea ce poate explica aceste proprietăți antiemetice. Studiile pe animale sugerează că CB1 poate fi afectat de haloperidol, ceea ce face din acest agent o potențială opțiune de tratament.22,23 Witsil și Mycyk au evaluat retrospectiv această ipoteză la patru pacienți cu greață și vărsături refractare la tratamentul antiemetic standard.21 Toți pacienții au găsit ameliorare în decurs de 1 până la 2 ore de la administrarea de haloperidol 5 mg IV.21,24 Acest mic studiu de caz demonstrează că haloperidolul poate ameliora greața și vărsăturile legate de CHS suficient pentru a preveni internarea în spital, ceea ce poate duce la economii de costuri pentru sistemul de sănătate.19 Trebuie luat în considerare riscul de prelungire a QTc cu haloperidol, în special la pacienții cu tulburări electrolitice ca urmare a vărsăturilor excesive. Sunt necesare studii suplimentare pentru a determina locul haloperidolului în terapie și dozajul optim al acestuia.
Întreruperea consumului de canabis este singurul tratament care ameliorează și previne simptomele asociate cu CHS. În studiul care a descris pentru prima dată CHS, abstinența de la canabis a dus la încetarea grețurilor și vărsăturilor la șapte din 10 pacienți, în timp ce ceilalți au continuat să sufere de boală continuă. Trei dintre cei șapte pacienți au reluat ulterior consumul de canabis, iar simptomele au revenit în câteva luni.10 Aceste constatări au fost reproduse în rapoarte de caz recente.12,25 Pacienții ar trebui să fie educați cu privire la încetarea consumului de canabis ca mijloc de ameliorare a simptomelor și ar trebui să li se ofere resurse pentru a ajuta la încetarea consumului.
Concluzie
Pe măsură ce canabisul este legalizat în mai multe state, este probabil că utilizarea sa va crește și vor fi raportate mai multe cazuri de SHC. Clinicienii ar trebui să suspecteze CHS la pacienții care se prezintă cu antecedente de consum de canabis sau canabinoizi sintetici și simptome care includ greață și vărsături intratabile, împreună cu relatări privind utilizarea băilor fierbinți pentru controlul simptomelor. Această conjectură ar putea preveni efectuarea unor analize extinse și costisitoare pentru alte afecțiuni. Farmaciștii au un rol în consilierea pacienților cu privire la riscurile asociate consumului de canabis și în trimiterea pacienților cu simptome de SHC pentru o îngrijire ulterioară adecvată. Rapoartele de caz din literatura de specialitate au identificat factorii de risc pentru CHS. Din păcate, CHS este relativ puțin raportat, iar mecanismul său exact este necunoscut. Diagnosticul și tratamentul CHS se bazează în prezent pe rapoarte de caz mici. Informațiile ar trebui să continue să fie evaluate pe măsură ce devin disponibile, pentru a asigura un tratament adecvat.
1. Institutul Național pentru Abuzul de Droguri (NIDA). Ce este marijuana? www.drugabuse.gov/publications/research-reports/marijuana/what-marijuana. Accesat la 25 august 2016.
2. NIDA. Care este amploarea consumului de marijuana în Statele Unite? www.drugabuse.gov/publications/research-reports/marijuana/what-scope-marijuana-use-in-united-states. Accesat la 25 august 2016.
3. Kim HS, Monte AA. Legalizarea canabisului din Colorado și efectul său asupra asistenței de urgență. Ann Emerg Med. 2016;68:71-75.
4. Cerdá M, Wall M, Keyes KM, et al. Legile privind marijuana medicală în 50 de state: investigarea relației dintre legalizarea de stat a marijuanei medicale și consumul, abuzul și dependența de marijuana. Dependența de droguri și alcool. 2012;120:22-27.
5. CNN Money. Unde iarba este legală. http://money.cnn.com/interactive/news/economy/marijuana-legalization-map/index.html. Accesat la 25 august 2016.
6. Marijuana Policy Project. 2016 marijuana policy reform legislation. www.mpp.org/states/key-marijuana-policy-reform. Accesat la 13 noiembrie 2016.
7. NIDA. Cum își produce efectele marijuana? www.drugabuse.gov/publications/research-reports/marijuana/how-does-marijuana-produce-its-effects. Accesat în august 2016.
8. Manzanares J, Julian MD, Carrascosa A. Rolul sistemului canabinoid în controlul durerii și implicațiile terapeutice pentru gestionarea episoadelor de durere acută și cronică. Curr Neuropharmacol. 2006;4:239-257.
9. Galli JA, Sawaya RA, Friedenberg FK. Sindromul de hiperemeză canabinoidă. Curr Drug Abuse Rev. 2011;4:
241-249.
10. Allen JH, de Moore GM, Heddle R, Twartz JC. Hiperemeza canabinoidă: hiperemeză ciclică în asociere cu abuzul cronic de canabis. Gut. 2004;53:1566-1570.
11. Ruffle JK, Bajgoric S, Samra K, et al. Sindromul de hiperemeză canabinoidă: un diagnostic diferențial important al vărsăturilor persistente și inexplicabile. Eur J Gastroenterol Hepatol. 2015;27:1403-1408.
12. Soriano-Co M, Batke M, Cappell MS. Sindromul hiperemesis de canabis caracterizat prin greață și vărsături persistente, dureri abdominale și băi compulsive asociate cu consumul cronic de marijuana: un raport de opt cazuri în Statele Unite. Dig Dis Sci. 2010;55:3113-3119.
13. Ukaigwe A, Karmacharya P, Donato A. A gut gone to pot: un caz de sindrom de hiperemeză canabinoidă datorat K2, un canabinoid sintetic. Case Rep Emerg Med. 2014;2014:167098.
14. Hopkins CY, Gilchrist BL. Un caz de sindrom de hiperemeză canabinoidă cauzată de canabinoizi sintetici. J Emerg Med. 2013;45:544-546.
15. Simonetto DA, Oxentenko AS, Herman ML, Szostek JH. Hiperemeza canabinoidă: o serie de cazuri de 98 de pacienți. Mayo Clin Proc. 2012;87:114-119.
16. Lu ML, Agito MD. Sindromul de hiperemeză canabinoidă: marijuana este atât antiemetică, cât și proemetică. Cleve Clin J Med. 2015;82:429-434.
17. Habboushe J, Sedor J. Cannabinoid hyperemesis acute renal failure: a common sequela of cannabinoid hyperemesis syndrome. Am J Emerg Med. 2014;32:690.e1-e2.
18. Srihari P, Liu M, Punzell S, et al. Sindromul de hiperemeză canabinoidă asociat cu dușul compulsiv și leziuni renale acute. Prim Care Companion CNS Disord. 2016;18(1).
19. Gregoire P, Tau M, Tau M, Robertson D. Sindromul de hiperemeză canabinoidă și debutul unui episod maniacal. BMJ Case Rep. 2016;2016.
20. Bagdure S, Smalligan RD, Sharifi H, Khandheria B. Efectul descrescător al scăldatului compulsiv în hiperemeza canabinoidă. Am J Addict. 2012;21:184-185.
21. Witsil JC, Mycyk MB. Haloperidol, un tratament nou pentru sindromul de hiperemeză canabinoidă. Am J Ther. 2014 Nov 12 .
22. Schulze DR, Carroll FI, McMahon LR. Interacțiuni între transportatorul de dopamină și liganzii receptorilor canabinoizi la maimuțele rhesus. Psihofarmacologie (Berl). 2012;222:425-438.
23. Desai RI, Thakur GA, Thakur GA, Vemuri VK, et al. Analiza toleranței și a dependenței comportamentale/fizice în timpul tratamentului cronic cu agoniști CB1: efectele agoniștilor CB1, antagoniștilor și ale medicamentelor noncannabinoide. J Pharmacol Exp Ther. 2013;344:319-328.
24. Hickey JL, Witsil JC, Mycyk MB. Haloperidol pentru tratamentul sindromului de hiperemeză canabinoidă. Am J Emerg Med. 2013;31:1003.e5-e6.
25. Pélissier F, Claudet I, Gandia-Mailly P, et al. Sindromul de hiperemeză a canabisului în departamentul de urgență: cum poate fi utilă o echipă specializată în dependență? Un studiu pilot. J Emerg Med. 2016;51:544-551.