 Tzv. „tvrdnutí tepen“ vede ke zvýšení krevního tlaku a v konečném důsledku je významným rizikovým faktorem trombózy a srdečních onemocnění. Proces tvrdnutí je ve skutečnosti kalcifikace cévních tkání stejnou formou minerálu jako v kostech, fosforečnanem vápenatým příbuzným minerálu hydroxyapatitu. Kalcifikace může probíhat na tukových ložiscích (aterosklerotických placích) na vnitřní straně cévy (intimální nebo aterosklerotická kalcifikace) nebo ve střední vrstvě cévní stěny (mediální kalcifikace), přičemž druhá jmenovaná kalcifikace je typicky spojena se stárnutím, cukrovkou a onemocněním ledvin.
Tzv. „tvrdnutí tepen“ vede ke zvýšení krevního tlaku a v konečném důsledku je významným rizikovým faktorem trombózy a srdečních onemocnění. Proces tvrdnutí je ve skutečnosti kalcifikace cévních tkání stejnou formou minerálu jako v kostech, fosforečnanem vápenatým příbuzným minerálu hydroxyapatitu. Kalcifikace může probíhat na tukových ložiscích (aterosklerotických placích) na vnitřní straně cévy (intimální nebo aterosklerotická kalcifikace) nebo ve střední vrstvě cévní stěny (mediální kalcifikace), přičemž druhá jmenovaná kalcifikace je typicky spojena se stárnutím, cukrovkou a onemocněním ledvin.
Existují významné důkazy o tom, že buňky v cévní stěně (buňky hladkého svalstva cév) se při zátěži mění směrem k buňkám více podobným kostem a začínají exprimovat proteiny typicky spojené s kalcifikací kostí. Existuje zde mnoho otázek: co spouští proces kalcifikace v cévách; jak se částice fosforečnanu vápenatého vážou na cévní tkáň nebo tukové usazeniny; proč jsou některé kalcifikované plaky v cévách stabilní, zatímco u jiných se odlamují kusy, které způsobují ucpání cévy?
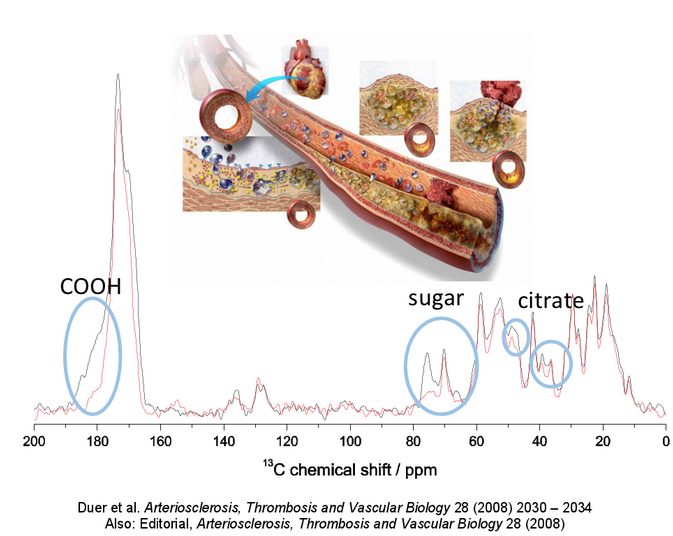
Naše původní práce v této oblasti (Arteriosclerosis, Thrombosis and Vascular Biology, 2008) ukázala, že stejné molekuly, které jsou zodpovědné za vazbu částic fosforečnanu vápenatého do kostí – funkcionalizované cukry – jsou zodpovědné za stejný proces při kalcifikaci cév. V současné době pracujeme na identifikaci toho, co jsou tyto cukry zač, v naději, že pak bude možné navrhnout inhibitory jejich funkce v cévní kalcifikaci.
V naší nejnovější práci jsme ukázali, že to, zda je do cévních kalciumfosfátových částic začleněn citrát, má obrovský vliv jak na velikost a formu částic, tak na to, jak jsou toxické pro buňky (Biomaterials, 2013). Citrát je totiž běžně inkorporován do kalcifikovaných tkání včetně kostí (Calcified Tissue International, 2013), nejspíše proto, že vápník je do míst kalcifikace transportován ve formě citrátových komplexů a malé póry nanoskopických rozměrů, ve kterých kalcifikace často probíhá, neumožňují transportovanému citrátu „uniknout“. Nyní se zabýváme možností, že citrát výrazně ovlivňuje mechanické vlastnosti kalciumfosfátových částic a může vysvětlit, proč jsou některé kalcifikované cévní pláty stabilní a jiné výrazně méně.
Dalším rysem cévní kalcifikace je, že jí vždy bezprostředně předchází nekróza buněk, a proto zkoumáme, jaké buněčné molekuly se v důsledku tohoto procesu ukládají v cévní stěně. Doufáme, že právě to nám umožní určit, jaké by mohly být funkcionalizované cukry, které vážou částice fosforečnanu vápenatého na tkáň.
Spolupracovníci: Cathy Shanahan (Kings College London), Dr. Jeremy Skepper (PDN, University of Cambridge), Dr. Karin Muller (PDN, University of Cambridge)
Financování: Britská kardiologická nadace