Teoría MO y enlaces pi conjugados
La ventaja de utilizar la teoría MO para entender el enlace en las moléculas orgánicas se hace más evidente cuando pensamos en los enlaces pi. Consideremos primero el enlace pi en el eteno desde el punto de vista de la teoría MO (en este ejemplo prescindiremos de los enlaces s en la molécula, y pensaremos sólo en el enlace π). Empezamos con dos orbitales atómicos: un orbital 2p no hibridado de cada carbono. Cada uno contiene un solo electrón. En la teoría de la MO, los dos atómicos se combinan matemáticamente para formar dos orbitales moleculares pi, uno de baja energía de enlace pi y otro de alta energía de antienlace pi*.
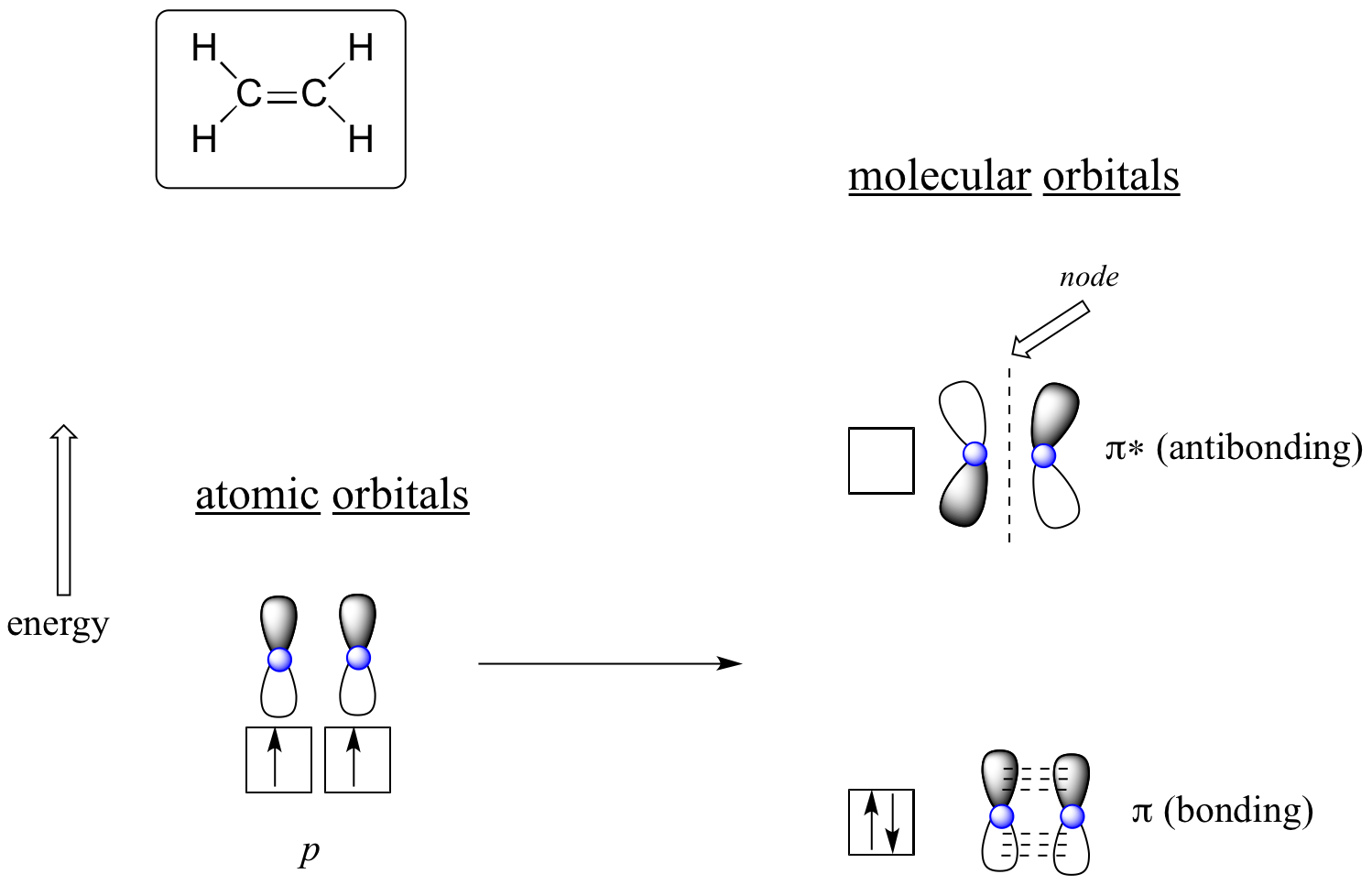
Orbitales moleculares del eteno (etileno)
En el orbital pi de enlace, los dos lóbulos sombreados de los orbitales p interactúan constructivamente entre sí, al igual que los dos lóbulos no sombreados (recuerde que la elección arbitraria del sombreado representa los signos matemáticos (+) y (-) para la función de onda matemática que describe el orbital). Hay una mayor densidad de electrones entre los dos núcleos de carbono en el orbital molecular – es una interacción de enlace.
En el orbital pi* antienlace de mayor energía, el lóbulo sombreado de un orbital p interactúa destructivamente con el lóbulo no sombreado del segundo orbital p, dando lugar a un nodo entre los dos núcleos y a una repulsión general entre los núcleos de carbono.
Utilizando de nuevo el principio de «acumulación», colocamos los dos electrones en el orbital molecular pi de menor energía y de enlace. El orbital pi* antienlace permanece vacío.
A continuación, consideraremos la molécula de 1,3-butadieno. A partir de la teoría del orbital de valencia, podríamos esperar que el enlace C2-C3 de esta molécula, al ser un enlace sigma, pudiera rotar libremente.

Sin embargo, experimentalmente se observa que hay una barrera significativa a la rotación sobre el enlace C2-C3, y que toda la molécula es plana. Además, el enlace C2-C3 tiene una longitud de 148 pm, más corto que un enlace simple carbono-carbono típico (alrededor de 154 pm), aunque más largo que un enlace doble típico (alrededor de 134 pm).
La teoría de orbitales moleculares explica estas observaciones con el concepto de enlaces pi deslocalizados. En esta imagen, los cuatro orbitales atómicos 2p se combinan matemáticamente para formar cuatro orbitales moleculares pi de energía creciente. Dos de ellos -los orbitales pi de enlace- son más bajos en energía que los orbitales atómicos p de los que se forman, mientras que dos -los orbitales pi* de antienlace- son más altos en energía.

El orbital molecular de menor energía, pi1, sólo tiene interacción constructiva y cero nodos. Más alto en energía, pero aún más bajo que los orbitales p aislados, el orbital pi2 tiene un nodo pero dos interacciones constructivas – por lo que sigue siendo un orbital de enlace en general. Observando los dos orbitales antienlazados, pi3* tiene dos nodos y una interacción constructiva, mientras que pi4* tiene tres nodos y cero interacciones constructivas.
Por el principio de aufbau, los cuatro electrones de los orbitales atómicos 2pz aislados se colocan en las MO de pi1 y pi2 enlazadas. Debido a que pi1 incluye la interacción constructiva entre C2 y C3, existe un grado, en la molécula de 1,3-butadieno, de interacción de enlace pi entre estos dos carbonos, lo que explica su menor longitud y la barrera a la rotación. La imagen del enlace de valencia del 1,3-butadieno muestra los dos enlaces pi como aislados entre sí, con cada par de electrones pi «atrapados» en su propio enlace pi. Sin embargo, la teoría del orbital molecular predice (con exactitud) que los cuatro electrones pi están hasta cierto punto deslocalizados, o «repartidos», por todo el sistema pi.
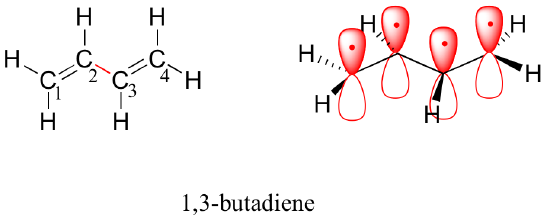
Vista de relleno del espacio
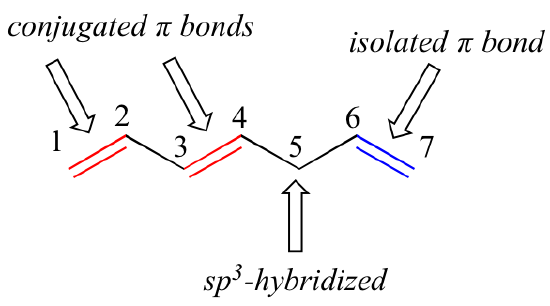
El 1,3-butadieno es el ejemplo más simple de un sistema de enlaces pi conjugados. Para que se considere conjugado, dos o más enlaces pi deben estar separados por un solo enlace -en otras palabras, no puede haber un carbono sp3-hibridado intermedio, porque esto rompería el sistema superpuesto de orbitales p paralelos. En el compuesto de abajo, por ejemplo, los dobles enlaces C1-C2 y C3-C4 están conjugados, mientras que el doble enlace C6-C7 está aislado de los otros dos enlaces pi por el C5 hibridado sp3.
Un concepto muy importante a tener en cuenta es que hay una estabilidad termodinámica inherente asociada a la conjugación. Esta estabilidad se puede medir experimentalmente comparando el calor de hidrogenación de dos dienos diferentes. (La hidrogenación es un tipo de reacción del que aprenderemos mucho más en el capítulo 15: esencialmente, es el proceso de añadir una molécula de hidrógeno -dos protones y dos electrones- a un enlace p). Cuando los dos dobles enlaces conjugados del 1,3-pentadieno se «hidrogenan» para producir pentano, se liberan unos 225 kJ por mol de pentano formado. Compárese con los aproximadamente 250 kJ/mol liberados cuando los dos dobles enlaces aislados del 1,4-pentadieno se hidrogenan, formando también pentano.
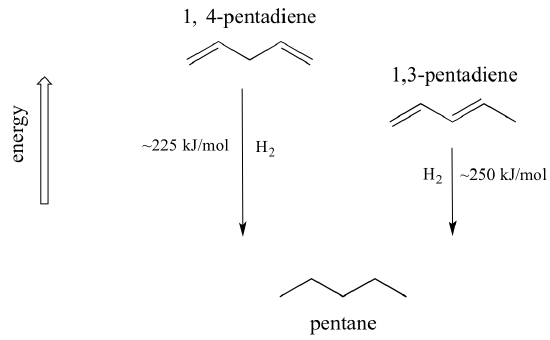
El dieno conjugado tiene menor energía: en otras palabras, es más estable. En general, los enlaces pi conjugados son más estables que los enlaces pi aislados.
En los sistemas pi conjugados pueden intervenir átomos de oxígeno y nitrógeno, además del carbono. En el metabolismo de las moléculas de grasa, algunas de las reacciones clave implican alquenos conjugados con grupos carbonilo.

En el capítulo 4, veremos que la teoría MO es muy útil para explicar por qué las moléculas orgánicas que contienen sistemas extendidos de enlaces pi conjugados suelen tener colores distintivos. El beta-caroteno, el compuesto responsable del color naranja de las zanahorias, tiene un sistema extendido de 11 enlaces pi conjugados.
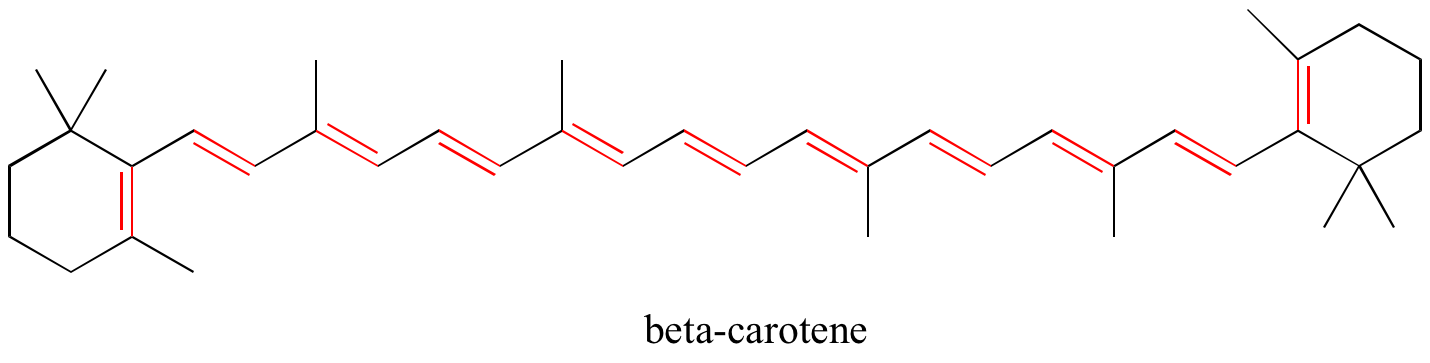
Ejercicio: Identifique todos los dobles enlaces conjugados y aislados en las estructuras siguientes. Para cada sistema pi conjugado, especifique el número de orbitales p superpuestos y cuántos electrones pi se comparten entre ellos.
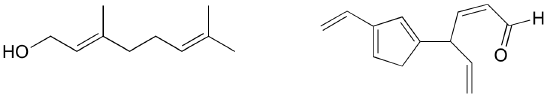
Ejercicio: Identifica todos los enlaces pi aislados y conjugados en el licopeno, el compuesto de color rojo de los tomates. ¿Cuántos electrones pi contiene el sistema pi conjugado?
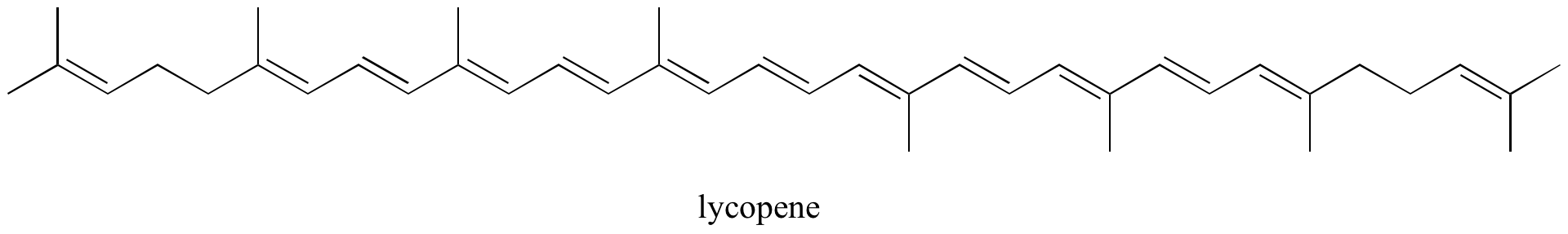
Soluciones a los ejercicios
Aromaticidad – El sistema conjugado definitivo
La teoría de los orbitales moleculares es especialmente útil para explicar las propiedades únicas de los compuestos aromáticos como el benceno:
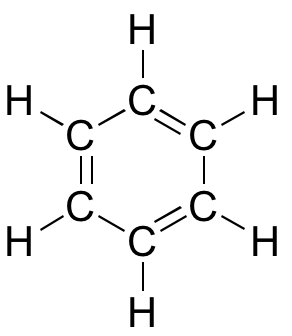
Modelo interactivo en 3D del benceno
Aunque el benceno se suele dibujar con tres enlaces dobles y tres enlaces simples, en realidad todos los enlaces carbono-carbono tienen exactamente la misma longitud (138 pm). Además, los enlaces pi del benceno son significativamente menos reactivos que los enlaces pi «normales», ya sean aislados o conjugados. Algo en la estructura del benceno hace que su disposición de enlaces pi sea especialmente estable. Este «algo» tiene un nombre: se llama «aromaticidad».
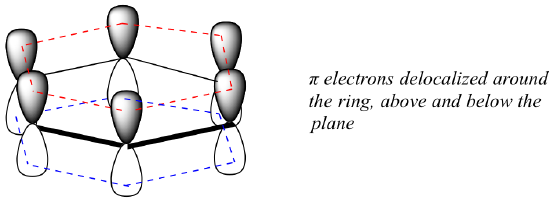
¿Qué es exactamente esta propiedad «aromática» que hace que los enlaces pi del benceno sean tan estables? En gran parte, la respuesta a esta pregunta radica en el hecho de que el benceno es una molécula cíclica en la que todos los átomos del anillo están hibridados sp2. Esto permite que los electrones pi se deslocalicen en orbitales moleculares que se extienden por todo el anillo, por encima y por debajo del plano. Para que esto ocurra, por supuesto, el anillo debe ser plano, de lo contrario los orbitales p no podrían solaparse adecuadamente. En efecto, se sabe que el benceno es una molécula plana.
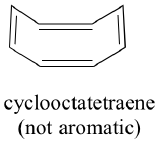
¿Tienen todas las moléculas cíclicas con alternancia de enlaces simples y dobles esta misma estabilidad aromática? La respuesta, de hecho, es «no». El anillo de ciclooctatetraeno de ocho miembros que se muestra a continuación no es plano, y sus enlaces π reaccionan como los alquenos «normales».
Está claro que hace falta algo más para ser aromático, y esto se puede explicar mejor con la teoría de orbitales moleculares. Veamos un diagrama de energía de los orbitales moleculares pi del benceno.
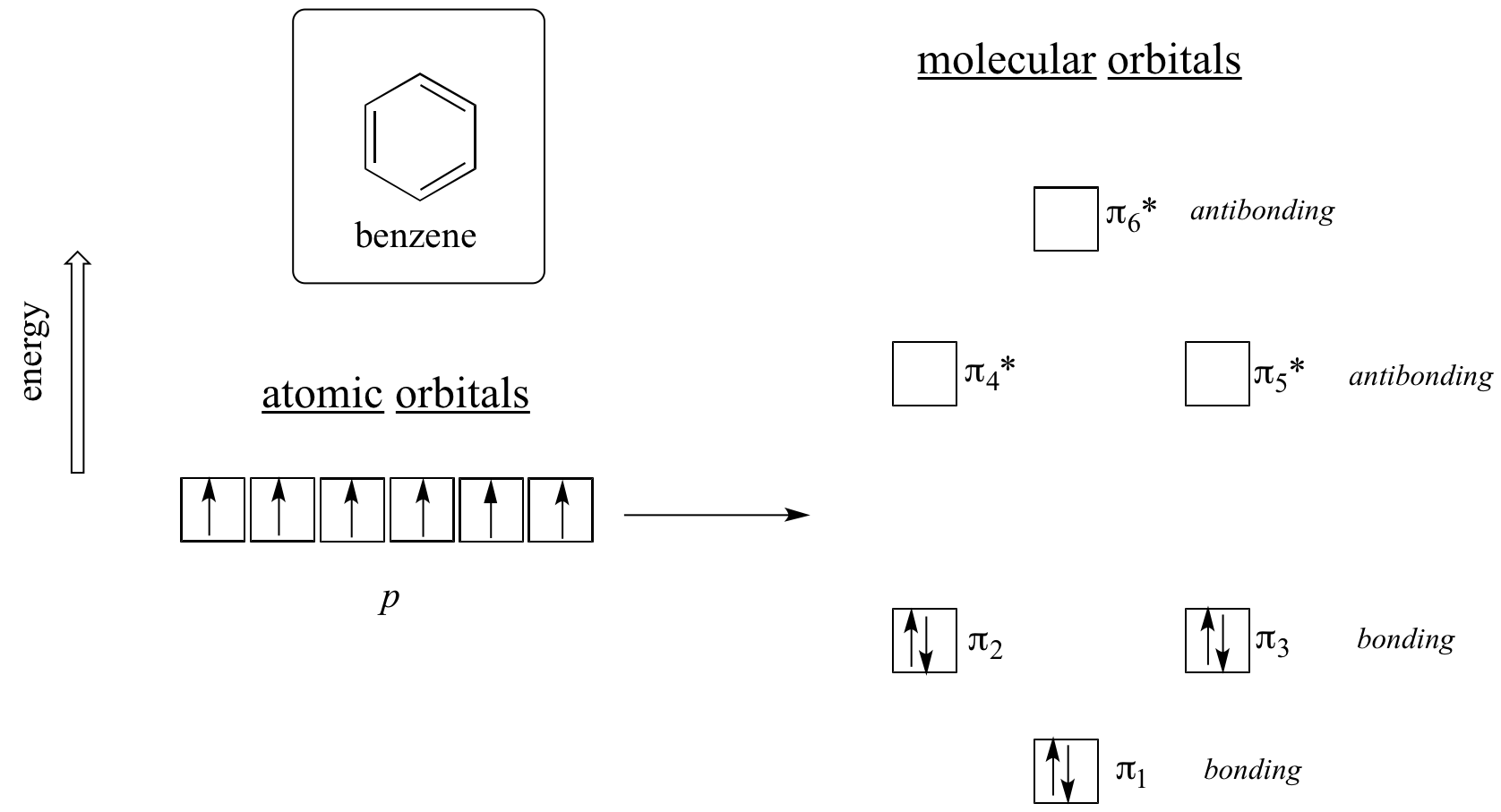
Los cálculos de mecánica cuántica nos dicen que los seis orbitales moleculares pi del benceno, formados a partir de seis orbitales atómicos p, ocupan cuatro niveles de energía distintos. pi1 y pi6* tienen niveles de energía únicos, mientras que los pares pi2 – pi3 y pi4*- pi5* son degenerados, lo que significa que están en el mismo nivel de energía. Cuando utilizamos el principio de aufbau para rellenar estos orbitales con los seis electrones pi del benceno, vemos que los orbitales de enlace están completamente llenos, y los orbitales de antienlace están vacíos. Esto nos da una buena pista sobre el origen de la especial estabilidad del benceno: un conjunto completo de MO de enlace es similar en muchos aspectos a la «cáscara completa» de electrones en los orbitales atómicos de los gases nobles estables helio, neón y argón.
Ahora, hagamos lo mismo para el ciclooctatetraeno, que ya hemos aprendido que no es aromático.
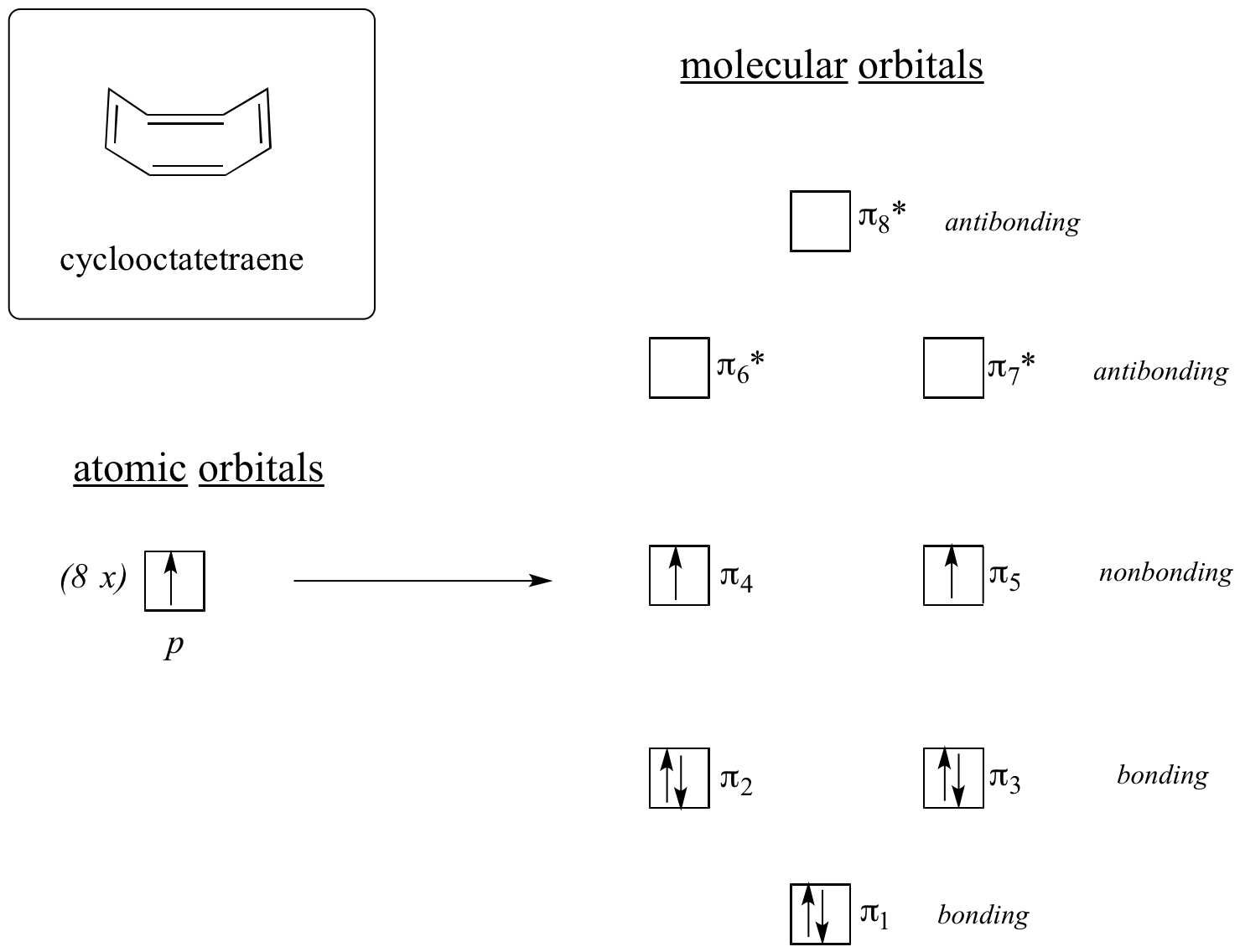
El resultado de los cálculos de los orbitales moleculares nos dice que los MO de menor y mayor energía (pi1 y pi8*) tienen niveles de energía únicos, mientras que los otros seis forman pares degenerados. Obsérvese que pi4 y pi5 están en el mismo nivel de energía que los orbitales atómicos aislados 2pz: por lo tanto, no son ni enlazantes ni antienlazantes, sino que se denominan MOs no enlazantes. Al rellenar los MOs con los ocho electrones pi de la molécula, encontramos que los dos últimos electrones no están apareados y caen en los dos orbitales degenerados no enlazantes. Como no tenemos una cáscara perfectamente llena de MOs de enlace, nuestra molécula no es aromática. Como consecuencia, cada uno de los dobles enlaces en el ciclooctatetraeno actúa más como un doble enlace aislado.
Por ahora, el objetivo de aprendizaje importante es reconocer los sistemas de enlaces pi conjugados y entender que el benceno es excepcionalmente estable exhibiendo una propiedad llamada aromaticidad. La aromaticidad y la química de los compuestos aromáticos es relativamente compleja y se discute en mayor detalle en los capítulos posteriores de este texto.
Química orgánica con énfasis biológico por Tim Soderberg (Universidad de Minnesota, Morris)