El elemento metálico aluminio es el tercer elemento más abundante en la corteza terrestre, comprendiendo el 8% del suelo y las rocas del planeta (el oxígeno y el silicio constituyen el 47% y el 28%, respectivamente). En la naturaleza, el aluminio sólo se encuentra en compuestos químicos con otros elementos como el azufre, el silicio y el oxígeno. El aluminio puro y metálico sólo puede producirse económicamente a partir del mineral de óxido de aluminio.
El aluminio metálico tiene muchas propiedades que lo hacen útil en una amplia gama de aplicaciones. Es ligero, fuerte, no magnético y no tóxico. Conduce el calor y la electricidad y refleja el calor y la luz. Es fuerte, pero fácil de trabajar, y conserva su resistencia en condiciones de frío extremo sin volverse frágil. La superficie del aluminio se oxida rápidamente para formar una barrera invisible contra la corrosión. Además, el aluminio puede reciclarse fácil y económicamente en nuevos productos.
Antecedentes
Los compuestos de aluminio han resultado útiles durante miles de años. Alrededor del año 5000 a.C., los alfareros persas fabricaban sus recipientes más resistentes con arcilla que contenía óxido de aluminio. Los antiguos egipcios y babilonios utilizaban compuestos de aluminio en tintes para tejidos, cosméticos y medicamentos. Sin embargo, no fue hasta principios del siglo XIX cuando se identificó el aluminio como elemento y se aisló como metal puro. La dificultad de extraer el aluminio de sus compuestos naturales hizo que el metal siguiera siendo raro durante muchos años; medio siglo después de su descubrimiento, seguía siendo tan raro y valioso como la plata.
En 1886, dos científicos de 22 años desarrollaron de forma independiente un proceso de fundición que hizo posible la producción económica en masa de aluminio. Conocido como el proceso Hall-Heroult en honor a sus inventores estadounidenses y franceses, el proceso sigue siendo el principal método de producción de aluminio en la actualidad. El proceso Bayer para refinar el mineral de aluminio, desarrollado en 1888 por un químico austriaco, también contribuyó significativamente a la producción económica en masa de aluminio.
En 1884, se produjeron 125 libras (60 kg) de aluminio en Estados Unidos, y se vendió por el mismo precio unitario que la plata. En 1995, las plantas estadounidenses produjeron 3,6 millones de toneladas de aluminio y el precio de la plata era setenta y cinco veces superior al del aluminio.
Materias primas
Los compuestos de aluminio se encuentran en todos los tipos de arcilla, pero el mineral más útil para producir aluminio puro es la bauxita. La bauxita está compuesta por un 45-60% de óxido de aluminio, junto con varias impurezas como arena, hierro y otros metales. Aunque algunos depósitos de bauxita son de roca dura, la mayoría consiste en tierra relativamente blanda que se extrae fácilmente en minas a cielo abierto. Australia produce más de un tercio del suministro mundial de bauxita. Se necesitan unas 4 libras (2 kg) de bauxita para producir 1 libra (0,5 kg) de aluminio metálico.
La sosa cáustica (hidróxido de sodio) se utiliza para disolver los compuestos de aluminio que se encuentran en la bauxita, separándolos de las impurezas. Dependiendo de la composición del mineral de bauxita, pueden utilizarse cantidades relativamente pequeñas de otros productos químicos en la extracción
de aluminio. El almidón, la cal y el sulfuro de sodio son algunos ejemplos.
La criolita, un compuesto químico formado por sodio, aluminio y flúor, se utiliza como electrolito (medio conductor de corriente) en la operación de fundición. La criolita se extraía de forma natural en Groenlandia, pero ahora el compuesto se produce de forma sintética para su uso en la producción de aluminio. Se añade fluoruro de aluminio para reducir el punto de fusión de la solución electrolítica.
El otro ingrediente principal utilizado en la operación de fundición es el carbono. Los electrodos de carbono transmiten la corriente eléctrica a través del electrolito. Durante la operación de fundición, parte del carbono se consume al combinarse con el oxígeno para formar dióxido de carbono. De hecho, se utiliza aproximadamente media libra (0,2 kg) de carbono por cada libra (2,2 kg) de aluminio producido. Parte del carbono utilizado en la fundición del aluminio es un subproducto del refinado del petróleo; el carbono adicional se obtiene del carbón.
Debido a que la fundición de aluminio implica el paso de una corriente eléctrica a través de un electrolito fundido, requiere grandes cantidades de energía eléctrica. En promedio, la producción de 2 libras (1 kg) de aluminio requiere 15 kilovatios-hora (kWh) de energía. El coste de la electricidad representa aproximadamente un tercio del coste de la fundición de aluminio.
El proceso de fabricación
La fabricación del aluminio se realiza en dos fases: el proceso Bayer de refinado del mineral de bauxita para obtener el óxido de aluminio, y el proceso Hall-Heroult de fundición del óxido de aluminio para liberar el aluminio puro.
El proceso Bayer
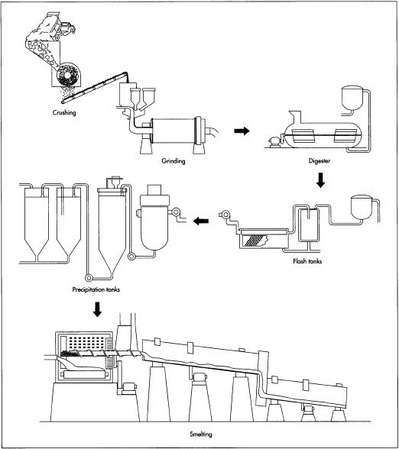
- 1 Primero, el mineral de bauxita se tritura mecánicamente. A continuación, el mineral triturado se mezcla con sosa cáustica y se procesa en un molino para producir una lechada (una suspensión acuosa) que contiene partículas muy finas de mineral.
- 2 La lechada se bombea a un digestor, un tanque que funciona como una olla a presión. El lodo se calienta a 230-520°F (110-270°C) bajo una presión de 50 lb/pulg 2 (340 kPa). Estas condiciones se mantienen durante un tiempo que va de media hora a varias horas. Puede añadirse sosa cáustica adicional para asegurar que se disuelven todos los compuestos que contienen aluminio.
- 3 La lechada caliente, que ahora es una solución de aluminato de sodio, pasa a través de una serie de tanques de flash que reducen la presión y recuperan el calor que puede reutilizarse en el proceso de refinado.
- 4 La lechada se bombea a un tanque de sedimentación. A medida que la pulpa descansa en este tanque, las impurezas que no se disuelven en la sosa cáustica se depositan en el fondo del recipiente. Un fabricante compara este proceso con la arena fina que se deposita en el fondo de un vaso de agua azucarada; el azúcar no se deposita porque está disuelto en el agua, al igual que el aluminio en el tanque de sedimentación permanece disuelto en la sosa cáustica. El residuo (llamado «lodo rojo») que se acumula en el fondo del tanque está formado por arena fina, óxido de hierro y óxidos de oligoelementos como el titanio.
- 5 Una vez que las impurezas se han asentado, el líquido restante, que tiene un aspecto similar al del café, se bombea a través de una serie de filtros de tela. Las partículas finas de impurezas que quedan en la solución son atrapadas por los filtros. Este material se lava para recuperar la alúmina y la sosa cáustica que pueden reutilizarse.
- 6 El líquido filtrado se bombea a través de una serie de tanques de precipitación de seis pisos de altura. Se añaden cristales semilla de hidrato de alúmina (alúmina unida a moléculas de agua) a través de la parte superior de cada tanque. Los cristales semilla crecen a medida que se asientan en el líquido y la alúmina disuelta se adhiere a ellos.
- 7 Los cristales precipitan (se depositan en el fondo del tanque) y se retiran. Tras el lavado, se transfieren a un horno para su calcinación (calentamiento para liberar las moléculas de agua que están químicamente unidas a las moléculas de alúmina). Un transportador de tornillo mueve un flujo continuo de cristales hacia un horno cilíndrico giratorio que está inclinado para permitir que la gravedad mueva el material a través de él. Una temperatura de 1.100 °C (2.000 °F) expulsa las moléculas de agua, dejando cristales de alúmina anhidra (sin agua). Tras salir del horno, los cristales pasan por un enfriador.
El proceso Hall-Heroult
La fundición de la alúmina en aluminio metálico tiene lugar en una cuba de acero llamada olla de reducción. El fondo de la olla está revestido de carbón, que actúa como un electrodo (conductor de la corriente eléctrica) del sistema. Los electrodos opuestos consisten en un conjunto de varillas de carbono suspendidas por encima de la olla; se introducen en una solución electrolítica y se mantienen a unos 3,8 cm por encima de la superficie del aluminio fundido que se acumula en el suelo de la olla. Las ollas de reducción se organizan en filas (potlines) compuestas por 50-200 ollas que se conectan en serie para formar un circuito eléctrico. Cada línea de ollas puede producir entre 66.000 y 110.000 toneladas (60.000-100.000 toneladas métricas) de aluminio al año. Una planta de fundición típica consta de dos o tres potlines.
- 8 Dentro de la olla de reducción, los cristales de alúmina se disuelven en criolita fundida a una temperatura de 1.760-1.780° F (960-970° C) para formar una solución electrolítica que conducirá la electricidad desde las varillas de carbono hasta el lecho revestido de carbono de la olla. Se hace pasar una corriente continua (4-6 voltios y 100.000-230.000 amperios) a través de la solución. La reacción resultante rompe los enlaces entre los átomos de aluminio y oxígeno de las moléculas de alúmina. El oxígeno liberado es atraído por las barras de carbono, donde forma dióxido de carbono. Los átomos de aluminio liberados se depositan en el fondo de la olla como metal fundido.
El proceso de fundición es continuo, ya que se añade más alúmina a la solución de criolita para sustituir el compuesto descompuesto. Se mantiene una corriente eléctrica constante. El calor generado por el flujo de electricidad en el electrodo inferior mantiene el contenido de la olla en estado líquido, pero tiende a formarse una costra sobre el electrolito fundido. Periódicamente, la corteza se rompe para permitir que se añada más alúmina para su procesamiento. El aluminio puro fundido se acumula en el fondo de la olla y se sifonea. Las ollas funcionan las 24 horas del día, los siete días de la semana.
- 9 Un crisol se desplaza por la línea de ollas, recogiendo 4.000 kg (9.000 lb) de aluminio fundido, que tiene una pureza del 99,8%. El metal se transfiere a un horno de retención y luego se funde (se vierte en moldes) como lingotes. Una técnica habitual es verter el aluminio fundido en un molde largo y horizontal. A medida que el metal se desplaza por el molde, el exterior se enfría con agua, lo que hace que el aluminio se solidifique. El eje sólido sale por el extremo del molde, donde se sierra a intervalos adecuados para formar lingotes de la longitud deseada. Al igual que el propio proceso de fundición, este proceso de colada también es continuo.
Subproductos/Residuos
La alúmina, la sustancia intermedia que se produce en el proceso Bayer y que constituye la materia prima del proceso Hall-Heroult, es también un producto final útil. Es una sustancia blanca, en forma de polvo, con una consistencia que oscila entre la del talco y la del azúcar granulado. Puede utilizarse en una amplia gama de productos, como detergentes para la ropa, pasta de dientes y bombillas fluorescentes. Es un ingrediente importante en los materiales cerámicos; por ejemplo, se utiliza para fabricar dientes postizos, bujías y parabrisas cerámicos transparentes para aviones militares. Es un eficaz compuesto de pulido que se utiliza, entre otros productos, para el acabado de los discos duros de los ordenadores. Sus propiedades químicas lo hacen eficaz en muchas otras aplicaciones, como los convertidores catalíticos y los explosivos. Incluso se utiliza como combustible para cohetes: en cada lanzamiento del transbordador espacial se consumen 180.000 kg. Aproximadamente el 10% de la alúmina producida cada año se utiliza para aplicaciones distintas a la fabricación de aluminio.
El mayor producto de desecho que se genera en el refinado de la bauxita son los residuos (desechos del mineral) llamados «lodo rojo». Una refinería produce aproximadamente la misma cantidad de lodo rojo que de alúmina (en términos de peso seco). Contiene algunas sustancias útiles, como el hierro, el titanio, la sosa y la alúmina, pero nadie ha sido capaz de desarrollar un proceso económico para recuperarlas. Aparte de una pequeña cantidad de lodo rojo que se utiliza comercialmente para colorear la mampostería, se trata realmente de un producto de desecho. La mayoría de las refinerías se limitan a recoger el lodo rojo en un estanque abierto que permite que se evapore parte de su humedad; cuando el lodo se ha secado hasta alcanzar una consistencia suficientemente sólida, lo que puede llevar varios años, se cubre con tierra o se mezcla con ella.
La descomposición de los electrodos de carbono durante la operación de fundición genera varios tipos de residuos. Las plantas de aluminio de Estados Unidos crean cantidades significativas de gases de efecto invernadero, generando unos 5,5 millones de toneladas (5 millones de toneladas métricas) de dióxido de carbono y 3.300 toneladas (3.000 toneladas métricas) de perfluorocarbonos (compuestos de carbono y flúor) cada año.
Aproximadamente 120.000 toneladas (110.000 toneladas métricas) de material de revestimiento de ollas gastado (SPL) se retira cada año de las ollas de reducción de aluminio. Declarado material peligroso por la Agencia de Protección Medioambiental (EPA), el SPL ha supuesto un importante problema de eliminación para la industria. En 1996, se inauguró la primera de una serie de plantas de reciclaje previstas; estas plantas transforman los SPL en frita de vidrio, un producto intermedio con el que se puede fabricar vidrio y cerámica. En última instancia, los SPL reciclados aparecen en productos como baldosas de cerámica, fibras de vidrio y gránulos de tejas de asfalto.
El futuro
Prácticamente todos los productores de aluminio de Estados Unidos son miembros de la Asociación Industrial Voluntaria del Aluminio (VAIP), una organización que colabora estrechamente con la EPA para encontrar soluciones a los problemas de contaminación a los que se enfrenta la industria. Uno de los principales focos de investigación es el esfuerzo por desarrollar un material de electrodo inerte (químicamente inactivo) para las ollas de reducción de aluminio. Un compuesto de titanio-diboruro-grafito es muy prometedor. Entre los beneficios que se espera obtener cuando se perfeccione esta nueva tecnología están la eliminación de las emisiones de gases de efecto invernadero y una reducción del 25% en el uso de energía durante la operación de fundición.
– Loretta Hall