Play media
EcocardiografíaEditar
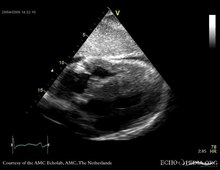
La ecocardiografía es un método seguro y no invasivo que puede utilizarse para evaluar la enfermedad estructural y funcional del corazón. La amiloidosis se presenta con engrosamiento ventricular y valvular, agrandamiento biatrial, patrón de llenado restrictivo, con función sistólica normal a levemente reducida y llenado diastólico disminuido. Se puede utilizar un eco para evaluar el pronóstico de la enfermedad, midiendo las diferentes tensiones dentro del corazón. La amiloidosis cardíaca produce alteraciones específicas en la funcionalidad del corazón. La ecocardiografía puede utilizarse para detectar este patrón específico (preservación relativa del miocardio apical con disminución de la deformación longitudinal en las secciones media y basal), que tiene una sensibilidad del 90-95% y una especificidad del 80-85% para la amiloidosis cardíaca. La ecocardiografía puede utilizarse para ayudar a los médicos con el diagnóstico, sin embargo, sólo puede utilizarse para la sugerencia de la enfermedad, no para la confirmación, a menos que se trate de una amiloidosis en fase tardía.
ECG/EKGEdit
Los ECG de los pacientes con amiloidosis cardíaca suelen mostrar un bajo voltaje en las derivaciones de las extremidades, con un eje derecho extremo inusual. Suele haber una onda P normal, sin embargo, puede estar ligeramente prolongada. En el caso de los pacientes con amiloidosis de cadena ligera, el patrón del complejo QRS está sesgado, con ondas R pobres de las derivaciones torácicas.
Los ECG de Holter pueden utilizarse para identificar arritmias asintomáticas.
Pueden estar presentes cambios en el electrocardiograma, mostrando bajo voltaje y anomalías de conducción como el bloqueo auriculoventricular o la disfunción del nódulo sinusal.
Pruebas de laboratorioEditar
Las pruebas de laboratorio incluyen los niveles de urea y creatinina, las enzimas hepáticas, la glucosa, la función tiroidea, el recuento sanguíneo completo y las pruebas de coagulación. El análisis de suero y orina para detectar la presencia de inmunoglobulina monoclonal también se realiza mediante inmunofijación para la detección de la banda monoclonal. La presencia de la banda monoclonal sería consistente con la amiloidosis de cadena ligera. En el caso de la amiloidosis de cadena ligera, se puede utilizar el ensayo de inmunoglobulina libre de cadena ligera en suero para el diagnóstico y el seguimiento de la amiloidosis. En la amiloidosis de cadena ligera, puede estar presente un nivel bajo de paraproteínas.
Biomarcadores cardíacosEditar
Hay 2 biomarcadores cardíacos principales utilizados en la evaluación de la amiloidosis cardíaca, la troponina y el proBNP N-terminal. Como es de esperar, con el daño y la disfunción cardíaca, puede haber una elevación de estos marcadores en pacientes con amiloidosis cardíaca. Estos marcadores se han incorporado a los diversos sistemas de estadificación/puntuación utilizados por los médicos para determinar la gravedad de la enfermedad y el pronóstico.

Biopsias
Las biopsias extracardíacas de tejidos del riñón, el hígado, el nervio periférico o la grasa abdominal pueden utilizarse para confirmar la presencia de depósitos amiloides. Los depósitos de amiloide en las muestras de biopsia se confirman mediante el uso del colorante rojo Congo, que produce una birrefringencia verde cuando se observa bajo luz polarizada. También puede realizarse una tinción con rojo Sirio o un examen por microscopía electrónica. La determinación del tipo de amiloide puede realizarse mediante técnicas de inmunohistoetiquetado, así como tinciones de inmunofluorescencia.
En el caso de los pacientes con amiloidosis de cadena ligera, podrían realizarse biopsias de médula ósea para determinar el porcentaje basal de células plasmáticas y para descartar un mieloma múltiple.
Cateterización
El cateterismo cardíaco derecho es la prueba que se utiliza para comprobar la existencia de presiones ventriculares diastólicas elevadas. Esta prueba es más invasiva y se realizaría tras muestras de biopsia endomiocárdica no concluyentes.
Resonancia magnética cardiacaEditar
La resonancia magnética cardiaca (RMC) es capaz de medir el grosor de diferentes zonas del corazón. Esto puede utilizarse para la cuantificación de los depósitos en el corazón. La RMC también muestra la caracterización del tejido miocárdico a través de los patrones de realce del gadolinio. Sin embargo, ninguna de las técnicas de RMC es capaz de diferenciar definitivamente la ATTR-CM y la AL-CM.
En el caso de la AL-CM, el 68% de ellos presentan hipertrofia ventricular izquierda simétrica y concéntrica. Por otro lado, para la ATTR-CM, el 79% de ellos tienen hipertrofia ventricular izquierda asimétrica y el 18% de ellos tienen hipertrofia ventricular izquierda simétrica y concéntrica.
En las imágenes ponderadas en T1, se puede detectar edema en el corazón con una señal T1 alta. Mientras tanto, el agrandamiento de las células del corazón reducirá la señal T1. Utilizando la señal T1, el volumen extracelular (ECV) es útil para determinar el grado de deposición de amiloide alrededor de las células del corazón y detectar la regresión de los depósitos de amiloide después del tratamiento. El VEC es mayor en la ATTR-CM que en la AL-CM.
En las imágenes ponderadas en T2, la señal T2 está aumentada en la miocarditis aguda (inflamación de los músculos del corazón), y en el infarto de miocardio (ataque al corazón). La señal T2 también está aumentada en la AL-CM y en la ATTR-CM, pero la señal es mayor en la AL-CM antes de iniciar la quimioterapia.
El realce tardío del gadolinio (LGE) puede determinar la gravedad del depósito de amiloide en el tejido cardíaco. Cuanto mayor sea la señal de LGE, más grave será la afectación del corazón. Puede dividirse en tres etapas: ausencia de RTG, RTG subendocárdico y RTG de espesor total (transmural).
Escintigrafía/imagen de radionúclidos
La escintigrafía puede utilizarse para medir la extensión y la distribución del amiloide en todo el cuerpo, incluidos el hígado, el riñón, el bazo y el corazón. Se puede administrar a un paciente un componente P amiloide sérico radiomarcado por vía intravenosa y el componente P se acumula en el depósito amiloide de forma proporcional al tamaño del depósito. El etiquetado del componente P puede entonces ser fotografiado por una cámara gamma.
Las exploraciones con radionúclidos de tecnecio pueden ahora diagnosticar de forma fiable la amiloidosis cardíaca, con ciertos métodos de exploración que tienen una sensibilidad superior al 99% (pero sólo un 91% de especificidad para la amiloidosis). En este método de obtención de imágenes, se inyecta tecnecio radiomarcado en el cuerpo, donde se une a los depósitos de amiloide cardíaco. A continuación, se realiza un escáner para determinar dónde permanece el trazador, lo que pone de manifiesto la deposición de amiloide en el corazón. Este método permite un diagnóstico definitivo no invasivo de la amiloidosis cardíaca (ya que en el pasado se requería una biopsia endomiocárdica)
Espectrometría de masasEditar
La espectrometría de masas puede utilizarse para determinar si la proteína es de cadena ligera o amiloidosis familiar mediante la identificación de la subunidad de la proteína.