Calcular grados de insaturación (DoU)
El grado de insaturación (DoU) también se conoce como equivalente de doble enlace. Si se da la fórmula molecular, introduzca los números en esta fórmula:
- (C\) es el número de carbonos
- (N\) es el número de nitrógenos
- (X\) es el número de halógenos (F, Cl, Br, I)
- (H\) es el número de hidrógenos
- One degree of unsaturation is equivalent to 1 ring or 1 double bond (1 \( \pi \) bond).
- Two degrees of unsaturation is equivalent to 2 double bonds, 1 ring and 1 double bond, 2 rings, or 1 triple bond (2 \( \pi \) bonds).
Como se ha dicho antes, una molécula saturada sólo contiene enlaces simples y no anillos. Otra forma de interpretar esto es que una molécula saturada tiene el máximo número de átomos de hidrógeno posible para ser un alcano acíclico. Así, el número de hidrógenos puede representarse por 2C+2, que es la representación molecular general de un alcano. Como ejemplo, para la fórmula molecular C3H4 el número de hidrógenos reales necesarios para que el compuesto esté saturado es 8 . El compuesto necesita 4 hidrógenos más para estar completamente saturado (número esperado de hidrógenos-número observado de hidrógenos=8-4=4). El grado de insaturación es igual a 2, es decir, la mitad del número de hidrógenos que necesita la molécula para ser clasificada como saturada. Por lo tanto, la fórmula DoB se divide por 2. La fórmula resta el número de X porque un halógeno (X) sustituye a un hidrógeno en un compuesto. Por ejemplo, en el cloroetano, C2H5Cl, hay un hidrógeno menos en comparación con el etano, C2H6.
Para que un compuesto esté saturado, hay un hidrógeno más en una molécula cuando el nitrógeno está presente. Por lo tanto, añadimos el número de nitrógenos (N). Esto se puede ver con el C3H9N en comparación con el C3H8. El oxígeno y el azufre no se incluyen en la fórmula porque la saturación no se ve afectada por estos elementos. As seen in alcohols, the same number of hydrogens in ethanol, C2H5OH, matches the number of hydrogens in ethane, C2H6.
The following chart illustrates the possible combinations of the number of double bond(s), triple bond(s), and/or ring(s) for a given degree of unsaturation. Each row corresponds to a different combination.
|
DoU
|
Possible combinations of rings/ bonds
|
||
|---|---|---|---|
|
|
# of rings
|
# of double bonds
|
# of triple bonds
|
|
1
|
1
|
0
|
0
|
|
|
0
|
1
|
0
|
|
2
|
2
|
0
|
0
|
|
|
0
|
2
|
0
|
|
|
0
|
0
|
1
|
|
|
1
|
1
|
0
|
| 3 | 3 | 0 | 0 |
| 2 | 1 | 0 | |
| 1 | 2 | 0 | |
| 0 | 1 | 1 | |
| 0 | 3 | 0 | |
| 1 | 0 | 1 | |
Remember, los grados de insaturación sólo dan la suma de dobles enlaces, triples enlaces y/o anillos. Por ejemplo, un grado de insaturación de 3 puede contener 3 anillos, 2 anillos+1 doble enlace, 1 anillo+2 dobles enlaces, 1 anillo+1 triple enlace, 1 doble enlace+1 triple enlace o 3 dobles enlaces.
Ejemplo: Benceno
¿Cuál es el grado de insaturación del benceno?
SOLUCIÓN
La fórmula molecular del benceno es C6H6. Por tanto,
DoU= 4, donde C=6, N=0,X=0, y H=6. 1 DoB puede ser igual a 1 anillo o 1 doble enlace. Esto corresponde al benceno que contiene 1 anillo y 3 dobles enlaces.
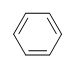
Sin embargo, cuando se da la fórmula molecular C6H6, el benceno es sólo una de las muchas estructuras posibles (isómeros). Las siguientes estructuras tienen todas DoB de 4 y tienen la misma fórmula molecular que el benceno.