- Objetivos de aprendizaje
- Producción y maduración de los linfocitos B
- Piensa en ello
- Receptores de células B
- Piénsalo
- Activación de las células B independiente de las células T
- Piensa en ello
- Activación de las células B dependiente de las células T
- Piénsalo
- Respuestas primarias y secundarias
- Piensa en ello
- Conceptos clave y resumen
- Múltiples opciones
- Fill in the Blank
- Think about It
Objetivos de aprendizaje
- Describir la producción y maduración de los linfocitos B
- Comparar la estructura de los receptores de los linfocitos B y los receptores de los linfocitos T
- Comparar la activación de los linfocitos B dependiente e independiente de T
- Comparar las respuestas de anticuerpos primarias y secundarias.dependiente y T-independiente de la activación de los linfocitos B
- Comparar las respuestas de anticuerpos primarias y secundarias
La inmunidad humoral se refiere a los mecanismos de las defensas inmunitarias adaptativas que están mediadas por los anticuerpos secretados por los linfocitos B o células B. Esta sección se centrará en los linfocitos B y analizará su producción y maduración, sus receptores y sus mecanismos de activación.
Producción y maduración de los linfocitos B
Al igual que los linfocitos T, los linfocitos B se forman a partir de células madre hematopoyéticas (HSC) multipotentes en la médula ósea y siguen una vía que pasa por la célula madre linfoide y el linfoblasto (véase la Figura 1 en Defensas celulares). Sin embargo, a diferencia de las células T, los linfoblastos destinados a convertirse en células B no abandonan la médula ósea y viajan al timo para su maduración. Más bien, las células B eventuales continúan madurando en la médula ósea.
El primer paso de la maduración de las células B es una evaluación de la funcionalidad de sus receptores de unión a antígenos. Esto ocurre a través de la selección positiva de las células B con receptores funcionales normales. A continuación, se utiliza un mecanismo de selección negativa para eliminar las células B autorreactivas y minimizar el riesgo de autoinmunidad. La selección negativa de las células B autorreactivas puede implicar la eliminación por apoptosis, la edición o modificación de los receptores para que dejen de ser autorreactivos, o la inducción de anergia en la célula B. Los linfocitos B inmaduros que superan la selección en la médula ósea se desplazan al bazo para sus etapas finales de maduración. Allí se convierten en células B maduras ingenuas, es decir células B maduras que aún no han sido activadas.
Piensa en ello
- Compara la maduración de las células B con la maduración de las células T.
Receptores de células B
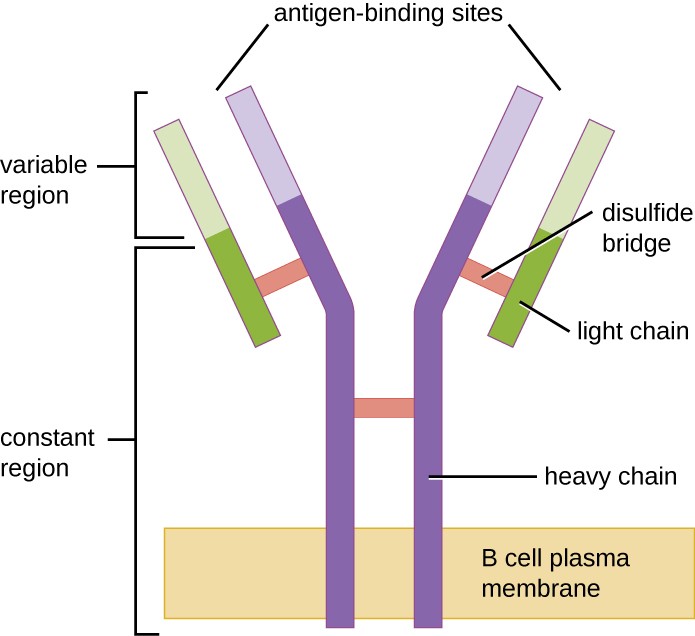
Figura 1. Los receptores de células B están incrustados en las membranas de las células B. Las regiones variables de todos los receptores de una misma célula se unen al mismo antígeno específico.
Al igual que las células T, las células B poseen receptores específicos de antígeno con diversas especificidades. Aunque dependen de las células T para un funcionamiento óptimo, las células B pueden activarse sin ayuda de las células T. Los receptores de células B (BCR) para las células B maduras ingenuas son formas monoméricas de IgD e IgM unidas a la membrana. Tienen dos cadenas pesadas idénticas y dos cadenas ligeras idénticas conectadas por enlaces disulfuro en una forma básica de «Y» (Figura 1). El tronco de la molécula en forma de Y, la región constante de las dos cadenas pesadas, abarca la membrana de las células B. Los dos sitios de unión al antígeno expuestos al exterior de la célula B participan en la unión de epítopos patógenos específicos para iniciar el proceso de activación. Se calcula que cada célula B madura ingenua tiene más de 100.000 BCR en su membrana, y cada uno de estos BCR tiene una especificidad de unión a epítopos idéntica.
Con el fin de estar preparadas para reaccionar a una amplia gama de epítopos microbianos, las células B, al igual que las células T, utilizan el reordenamiento genético de cientos de segmentos de genes para proporcionar la diversidad necesaria de especificidades del receptor. La región variable de la cadena pesada del BCR está formada por los segmentos V, D y J, similar a la cadena β del TCR. La región variable de la cadena ligera del BCR está formada por segmentos V y J, similares a la cadena α del TCR. El reordenamiento genético de todas las combinaciones posibles de V-J-D (cadena pesada) y V-J (cadena ligera) proporciona millones de sitios únicos de unión a antígenos para el BCR y para los anticuerpos secretados tras la activación.
Una diferencia importante entre los BCR y los TCR es la forma en que pueden interactuar con los epítopos antigénicos. Mientras que los TCRs sólo pueden interactuar con epítopos antigénicos que se presentan dentro de la hendidura de unión al antígeno del MHC I o MHC II, los BCRs no requieren la presentación del antígeno con el MHC; pueden interactuar con epítopos en antígenos libres o con epítopos mostrados en la superficie de patógenos intactos. Otra diferencia importante es que los TCR sólo reconocen epítopos de proteínas, mientras que los BCR pueden reconocer epítopos asociados a diferentes clases moleculares (por ejemplo, proteínas, polisacáridos, lipopolisacáridos).
La activación de las células B se produce a través de diferentes mecanismos dependiendo de la clase molecular del antígeno. La activación de un linfocito B por un antígeno proteico requiere que el linfocito B funcione como APC, presentando los epítopos proteicos con MHC II a las células T auxiliares. Debido a su dependencia de las células T para la activación de las células B, los antígenos proteicos se clasifican como antígenos T-dependientes. Por el contrario, los polisacáridos, los lipopolisacáridos y otros antígenos no proteicos se consideran antígenos T-independientes porque pueden activar las células B sin el procesamiento y la presentación del antígeno a las células T.
Piénsalo
- ¿Qué tipos de moléculas sirven como BCR?
- ¿Cuáles son las diferencias entre los TCR y los BCR con respecto al reconocimiento del antígeno?
- ¿Qué clases de moléculas son antígenos T-dependientes y cuáles son antígenos T-independientes?
Activación de las células B independiente de las células T
La activación de las células B sin la cooperación de las células T ayudantes se denomina activación independiente de las células T y se produce cuando los BCR interactúan con antígenos T-independientes. Los antígenos independientes de T (por ejemplo, cápsulas de polisacáridos, lipopolisacáridos) tienen unidades epitópicas repetitivas dentro de su estructura, y esta repetición permite el entrecruzamiento de múltiples BCR, proporcionando la primera señal para la activación (Figura 2). Dado que las células T no están implicadas, la segunda señal tiene que proceder de otras fuentes, como las interacciones de los receptores tipo Toll con los PAMP o las interacciones con factores del sistema del complemento.
Una vez que se activa una célula B, ésta experimenta una proliferación clonal y las células hijas se diferencian en células plasmáticas. Las células plasmáticas son fábricas de anticuerpos que secretan grandes cantidades de éstos. Tras la diferenciación, los BCR de superficie desaparecen y la célula plasmática secreta moléculas IgM pentaméricas que tienen la misma especificidad de antígeno que los BCR (Figura 2).
La respuesta independiente de las células T es de corta duración y no da lugar a la producción de células B de memoria. Por tanto, no dará lugar a una respuesta secundaria ante posteriores exposiciones a antígenos independientes de las células T.

Figura 2. Los antígenos independientes de T tienen epítopos repetidos que pueden inducir el reconocimiento y la activación de las células B sin la participación de las células T. También se requiere una segunda señal, como la interacción de los TLR con los PAMP (no se muestra), para la activación de la célula B. Una vez activada, la célula B prolifera y se diferencia en células plasmáticas secretoras de anticuerpos.
Piensa en ello
- ¿Cuáles son las dos señales necesarias para la activación de las células B independiente de las células T?
- ¿Cuál es la función de una célula plasmática?
Activación de las células B dependiente de las células T

Figura 3. Haga clic para ampliar la imagen. En la activación de los linfocitos B dependiente de las células T, el linfocito B reconoce e internaliza un antígeno y lo presenta a un linfocito T ayudante que es específico para el mismo antígeno. La célula T colaboradora interactúa con el antígeno presentado por la célula B, que activa la célula T y estimula la liberación de citoquinas que luego activan la célula B. La activación de la célula B desencadena la proliferación y la diferenciación en células B y células plasmáticas.
Una vez activadas por el reconocimiento vinculado, las células TH2 producen y secretan citoquinas que activan la célula B y provocan la proliferación en células hijas clonales. Tras varias rondas de proliferación, las citocinas adicionales proporcionadas por las células TH2 estimulan la diferenciación de los clones de células B activadas en células B de memoria, que responderán rápidamente a posteriores exposiciones al mismo epítopo proteico, y en células plasmáticas que pierden sus BCR de membrana y secretan inicialmente IgM pentamérica (Figura 3).
Después de la secreción inicial de IgM, las citocinas secretadas por las células TH2 estimulan a las células plasmáticas para que pasen de producir IgM a producir IgG, IgA o IgE. Este proceso, denominado cambio de clase o cambio de isotipo, permite que las células plasmáticas clonadas a partir de la misma célula B activada produzcan una variedad de clases de anticuerpos con la misma especificidad epitópica. El cambio de clase se lleva a cabo mediante la reordenación genética de los segmentos del gen que codifica la región constante, que determina la clase de un anticuerpo. La región variable no se modifica, por lo que la nueva clase de anticuerpo conserva la especificidad epitópica original.
Piénsalo
- ¿Qué pasos son necesarios para la activación de las células B dependiente de las células T?
- ¿Qué es el cambio de clase de anticuerpos y por qué es importante?
Respuestas primarias y secundarias
La activación de las células B dependiente de las células T desempeña un papel importante en las respuestas primarias y secundarias asociadas a la inmunidad adaptativa. Con la primera exposición a un antígeno proteico, se produce una respuesta primaria de anticuerpos dependiente de células T. La etapa inicial de la respuesta primaria es un periodo de retardo, o periodo latente, de aproximadamente 10 días, durante el cual no se puede detectar ningún anticuerpo en el suero. Este periodo de latencia es el tiempo necesario para todos los pasos de la respuesta primaria, incluyendo la unión del antígeno con los BCR por parte de los linfocitos B maduros ingenuos, el procesamiento y la presentación del antígeno, la activación de los linfocitos T auxiliares, la activación de los linfocitos B y la proliferación clonal. El final del periodo de retardo se caracteriza por un aumento de los niveles de IgM en el suero, ya que las células TH2 estimulan la diferenciación de las células B en células plasmáticas. Los niveles de IgM alcanzan su máximo alrededor de 14 días después de la exposición al antígeno primario; aproximadamente en este mismo momento, el TH2 estimula el cambio de clase de anticuerpos, y los niveles de IgM en el suero comienzan a disminuir. Mientras tanto, los niveles de IgG aumentan hasta que alcanzan un pico unas tres semanas después de la respuesta primaria (Figura 4).
Durante la respuesta primaria, algunas de las células B clonadas se diferencian en células B de memoria programadas para responder a exposiciones posteriores. Esta respuesta secundaria se produce de forma más rápida y contundente que la respuesta primaria. El periodo de retardo se reduce a sólo unos días y la producción de IgG es significativamente mayor que la observada en la respuesta primaria (Figura 4). Además, los anticuerpos producidos durante la respuesta secundaria son más eficaces y se unen con mayor afinidad a los epítopos objetivo. Las células plasmáticas producidas durante las respuestas secundarias viven más tiempo que las producidas durante la respuesta primaria, por lo que los niveles de anticuerpos específicos permanecen elevados durante un periodo de tiempo más largo.

Figura 4. En comparación con la respuesta primaria, la respuesta secundaria de anticuerpos ocurre más rápidamente y produce niveles de anticuerpos que son más altos y más sostenidos. La respuesta secundaria implica principalmente a las IgG.
Piensa en ello
- ¿Qué acontecimientos ocurren durante el periodo de retraso de la respuesta primaria de anticuerpos?
- ¿Por qué los niveles de anticuerpos permanecen elevados durante más tiempo durante la respuesta secundaria de anticuerpos?
Conceptos clave y resumen
- Los linfocitos B o células B producen anticuerpos que participan en la inmunidad humoral. Los linfocitos B se producen en la médula ósea, donde se producen las etapas iniciales de maduración, y viajan al bazo para los pasos finales de maduración hasta convertirse en linfocitos B maduros ingenuos.
- Los receptores de células B (BCR) son formas monoméricas de IgD e IgM unidas a la membrana que se unen a epítopos de antígenos específicos con sus regiones de unión al antígeno Fab. La diversidad de la especificidad de unión al antígeno se crea mediante el reordenamiento genético de los segmentos V, D y J, de forma similar al mecanismo utilizado para la diversidad del TCR.
- Los antígenos proteicos se denominan antígenos T-dependientes porque sólo pueden activar las células B con la cooperación de las células T auxiliares. Otras clases de moléculas no requieren la cooperación de las células T y se denominan antígenos T-independientes.
- La activación de las células B independiente de las células T implica el entrecruzamiento de los BCR por epítopos repetitivos de antígenos no proteicos. Se caracteriza por la producción de IgM por parte de las células plasmáticas y no produce células B de memoria.
- La activación de las células B dependiente de las células T implica el procesamiento y la presentación de antígenos proteicos a las células T auxiliares, la activación de las células B por las citocinas secretadas por las células TH2 activadas y las células plasmáticas que producen diferentes clases de anticuerpos como resultado del cambio de clase. También se producen células B de memoria.
- Las exposiciones secundarias a antígenos dependientes de T dan lugar a una respuesta de anticuerpos secundaria iniciada por las células B de memoria. La respuesta secundaria se desarrolla más rápidamente y produce niveles más altos y sostenidos de anticuerpos con mayor afinidad por el antígeno específico.
Múltiples opciones
¿Cuál de los siguientes sería un antígeno dependiente de T?
- lipopolysaccharide
- glycolipid
- protein
- carbohydrate
Which of the following would be a BCR?
- CD4
- MHC II
- MHC I
- IgD
Which of the following does not occur during the lag period of the primary antibody response?
- activation of helper T cells
- class switching to IgG
- presentation of antigen with MHC II
- binding of antigen to BCRs
Fill in the Blank
________ antigens can stimulate B cells to become activated but require cytokine assistance delivered by helper T cells.
T-independent antigens can stimulate B cells to become activated and secrete antibodies without assistance from helper T cells. These antigens possess ________ antigenic epitopes that cross-link BCRs.
Think about It
A patient lacks the ability to make functioning T cells because of a genetic disorder. Would this patient’s B cells be able to produce antibodies in response to an infection? Explain your answer.