L’élément métallique aluminium est le troisième élément le plus abondant dans la croûte terrestre, constituant 8% du sol et des roches de la planète (l’oxygène et le silicium en constituent respectivement 47% et 28%). Dans la nature, l’aluminium ne se trouve que dans des composés chimiques avec d’autres éléments comme le soufre, le silicium et l’oxygène. L’aluminium pur et métallique ne peut être produit économiquement qu’à partir du minerai d’oxyde d’aluminium.
L’aluminium métallique possède de nombreuses propriétés qui le rendent utile dans un large éventail d’applications. Il est léger, solide, non magnétique et non toxique. Il conduit la chaleur et l’électricité et reflète la chaleur et la lumière. Il est solide mais facile à travailler, et il conserve sa force par grand froid sans devenir cassant. La surface de l’aluminium s’oxyde rapidement pour former une barrière invisible contre la corrosion. En outre, l’aluminium peut être recyclé facilement et économiquement en nouveaux produits.
Contexte
Les composés d’aluminium se sont révélés utiles depuis des milliers d’années. Vers 5000 av. J.-C. , les potiers perses ont fabriqué leurs récipients les plus solides à partir d’argile contenant de l’oxyde d’aluminium. Les anciens Égyptiens et Babyloniens utilisaient les composés d’aluminium dans les teintures pour tissus, les cosmétiques et les médicaments. Toutefois, ce n’est qu’au début du XIXe siècle que l’aluminium a été identifié comme un élément et isolé comme un métal pur. La difficulté d’extraire l’aluminium de ses composés naturels a maintenu le métal rare pendant de nombreuses années ; un demi-siècle après sa découverte, il était encore aussi rare et précieux que l’argent.
En 1886, deux scientifiques de 22 ans ont développé indépendamment un procédé de fusion qui a rendu possible la production économique de masse de l’aluminium. Connu sous le nom de procédé Hall-Heroult, du nom de ses inventeurs américain et français, ce procédé est encore aujourd’hui la principale méthode de production d’aluminium. Le procédé Bayer de raffinage du minerai d’aluminium, développé en 1888 par un chimiste autrichien, a également contribué de manière significative à la production économique de masse de l’aluminium.
En 1884, 125 lb (60 kg) d’aluminium ont été produites aux États-Unis, et elles se sont vendues à peu près au même prix unitaire que l’argent. En 1995, les usines américaines ont produit 7,8 milliards de lb (3,6 millions de tonnes métriques) d’aluminium, et le prix de l’argent était soixante-quinze fois supérieur à celui de l’aluminium.
Matières premières
Les composés de l’aluminium se trouvent dans tous les types d’argile, mais le minerai le plus utile pour produire de l’aluminium pur est la bauxite. La bauxite est composée de 45 à 60 % d’oxyde d’aluminium, ainsi que de diverses impuretés telles que du sable, du fer et d’autres métaux. Bien que certains gisements de bauxite soient constitués de roches dures, la plupart consistent en une terre relativement molle qui est facilement extraite de mines à ciel ouvert. L’Australie produit plus d’un tiers de l’approvisionnement mondial en bauxite. Il faut environ 4 lb (2 kg) de bauxite pour produire 1 lb (0,5 kg) d’aluminium métallique.
La soude caustique (hydroxyde de sodium) est utilisée pour dissoudre les composés d’aluminium présents dans la bauxite, en les séparant des impuretés. Selon la composition du minerai de bauxite, des quantités relativement faibles d’autres produits chimiques peuvent être utilisées dans l’extraction
d’aluminium. L’amidon, la chaux et le sulfure de sodium en sont quelques exemples.
La cryolite, un composé chimique constitué de sodium, d’aluminium et de fluor, est utilisée comme électrolyte (milieu conducteur de courant) dans l’opération de fusion. La cryolite naturelle était autrefois exploitée au Groenland, mais le composé est maintenant produit synthétiquement pour être utilisé dans la production d’aluminium. Du fluorure d’aluminium est ajouté pour abaisser le point de fusion de la solution électrolytique.
L’autre ingrédient majeur utilisé dans l’opération de fusion est le carbone. Les électrodes de carbone transmettent le courant électrique à travers l’électrolyte. Pendant l’opération de fusion, une partie du carbone est consommée car il se combine avec l’oxygène pour former du dioxyde de carbone. En fait, environ une demi-livre (0,2 kg) de carbone est utilisée pour chaque livre (2,2 kg) d’aluminium produite. Une partie du carbone utilisé dans la fusion de l’aluminium est un sous-produit du raffinage du pétrole ; le carbone supplémentaire est obtenu à partir du charbon.
Comme la fusion de l’aluminium implique le passage d’un courant électrique dans un électrolyte fondu, elle nécessite de grandes quantités d’énergie électrique. En moyenne, la production de 1 kg (2 lb) d’aluminium nécessite 15 kilowattheures (kWh) d’énergie. Le coût de l’électricité représente environ un tiers du coût de la fusion de l’aluminium.
Le processus de fabrication
La fabrication de l’aluminium s’effectue en deux phases : le procédé Bayer, qui consiste à raffiner le minerai de bauxite pour obtenir de l’oxyde d’aluminium, et le procédé Hall-Heroult, qui consiste à fondre l’oxyde d’aluminium pour libérer de l’aluminium pur.
Le procédé Bayer
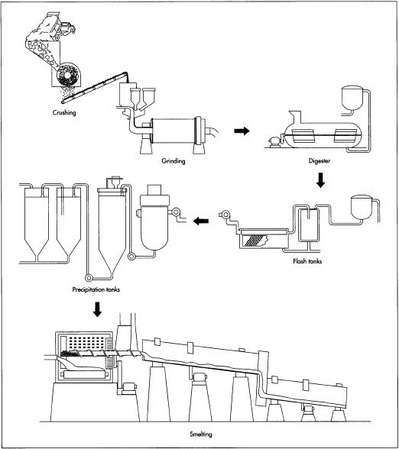
- 1 Tout d’abord, le minerai de bauxite est broyé mécaniquement. Ensuite, le minerai concassé est mélangé à de la soude caustique et traité dans un broyeur pour produire une boue (une suspension aqueuse) contenant de très fines particules de minerai.
- 2 La boue est pompée dans un digesteur, un réservoir qui fonctionne comme une cocotte-minute. La boue est chauffée à 230-520°F (110-270°C) sous une pression de 50 lb/in 2 (340 kPa). Ces conditions sont maintenues pendant une durée allant d’une demi-heure à plusieurs heures. De la soude caustique supplémentaire peut être ajoutée pour s’assurer que tous les composés contenant de l’aluminium sont dissous.
- 3 La boue chaude, qui est maintenant une solution d’aluminate de sodium, passe par une série de réservoirs de flash qui réduisent la pression et récupèrent la chaleur qui peut être réutilisée dans le processus de raffinage.
- 4 La boue est pompée dans un réservoir de décantation. Lorsque la boue repose dans cette cuve, les impuretés qui ne se dissolvent pas dans la soude caustique se déposent au fond de la cuve. Un fabricant compare ce processus au sable fin qui se dépose au fond d’un verre d’eau sucrée ; le sucre ne se dépose pas parce qu’il est dissous dans l’eau, tout comme l’aluminium dans le réservoir de décantation reste dissous dans la soude caustique. Le résidu (appelé « boue rouge ») qui s’accumule au fond du réservoir est constitué de sable fin, d’oxyde de fer et d’oxydes d’oligo-éléments comme le titane.
- 5 Une fois les impuretés décantées, le liquide restant, qui ressemble un peu à du café, est pompé à travers une série de filtres en tissu. Toutes les fines particules d’impuretés qui restent dans la solution sont piégées par les filtres. Cette matière est lavée pour récupérer l’alumine et la soude caustique qui peuvent être réutilisées.
- 6 Le liquide filtré est pompé à travers une série de cuves de précipitation hautes de six étages. Des cristaux d’amorçage d’hydrate d’alumine (alumine liée à des molécules d’eau) sont ajoutés par le haut de chaque réservoir. Les cristaux d’ensemencement grandissent à mesure qu’ils se déposent dans le liquide et que l’alumine dissoute s’y attache.
- 7 Les cristaux précipitent (se déposent au fond du réservoir) et sont retirés. Après le lavage, ils sont transférés dans un four pour la calcination (chauffage pour libérer les molécules d’eau qui sont chimiquement liées aux molécules d’alumine). Un convoyeur à vis déplace un flux continu de cristaux dans un four cylindrique rotatif incliné pour permettre à la gravité de déplacer le matériau. Une température de 1 100 °C (2 000 °F) chasse les molécules d’eau, laissant des cristaux d’alumine anhydres (sans eau). Après avoir quitté le four, les cristaux passent par un refroidisseur.
Le procédé Hall-Heroult
La fusion de l’alumine en aluminium métallique a lieu dans une cuve en acier appelée cuve de réduction. Le fond de la cuve est tapissé de carbone, qui joue le rôle d’une électrode (conducteur du courant électrique) du système. Les électrodes opposées sont constituées d’un ensemble de tiges de carbone suspendues au-dessus de la cuve ; elles sont plongées dans une solution électrolytique et maintenues à environ 3,8 cm (1,5 po) au-dessus de la surface de l’aluminium fondu qui s’accumule sur le fond de la cuve. Les cuves de réduction sont disposées en rangées (potlines) composées de 50 à 200 cuves qui sont connectées en série pour former un circuit électrique. Chaque potline peut produire 66 000 à 110 000 tonnes (60 000 à 100 000 tonnes métriques) d’aluminium par an. Une usine d’électrolyse typique est constituée de deux ou trois séries de cuves.
- 8 Dans la cuve de réduction, les cristaux d’alumine sont dissous dans de la cryolite fondue à une température de 1 760 à 1 780° F (960 à 970° C) pour former une solution électrolytique qui conduira l’électricité des tiges de carbone au lit revêtu de carbone de la cuve. Un courant continu (4-6 volts et 100 000-230 000 ampères) est passé dans la solution. La réaction qui en résulte brise les liaisons entre les atomes d’aluminium et d’oxygène des molécules d’alumine. L’oxygène libéré est attiré par les tiges de carbone, où il forme du dioxyde de carbone. Les atomes d’aluminium libérés se déposent au fond de la marmite sous forme de métal fondu.
Le processus de fusion est continu, de l’alumine étant ajoutée à la solution de cryolite pour remplacer le composé décomposé. Un courant électrique constant est maintenu. La chaleur générée par le flux d’électricité à l’électrode inférieure maintient le contenu du pot à l’état liquide, mais une croûte a tendance à se former au-dessus de l’électrolyte fondu. Périodiquement, la croûte est brisée pour permettre d’ajouter de l’alumine pour le traitement. L’aluminium pur fondu s’accumule au fond de la cuve et est évacué par siphonage. Les cuves fonctionnent 24 heures sur 24, sept jours sur sept.
- 9 Un creuset est déplacé le long de la ligne de cuves, recueillant 4 000 kg (9 000 lb) d’aluminium fondu, qui est pur à 99,8 %. Le métal est transféré dans un four de maintien, puis coulé (versé dans des moules) sous forme de lingots. Une technique courante consiste à verser l’aluminium en fusion dans un long moule horizontal. À mesure que le métal se déplace dans le moule, l’extérieur est refroidi à l’eau, ce qui entraîne la solidification de l’aluminium. L’arbre solide émerge de l’extrémité du moule, où il est scié à intervalles appropriés pour former des lingots de la longueur souhaitée. Comme le processus de fusion lui-même, ce processus de coulée est également continu.
Sous-produits/déchets
L’alumine, la substance intermédiaire qui est produite par le procédé Bayer et qui constitue la matière première du procédé Hall-Heroult, est également un produit final utile. Il s’agit d’une substance blanche, pulvérulente, dont la consistance varie entre celle du talc et celle du sucre cristallisé. Il peut être utilisé dans une large gamme de produits tels que les détergents à lessive, le dentifrice et les ampoules fluorescentes. C’est un ingrédient important des matériaux céramiques ; par exemple, il est utilisé pour fabriquer des fausses dents, des bougies d’allumage et des pare-brise en céramique transparente pour les avions militaires. Un composé de polissage efficace, il est utilisé pour la finition des disques durs d’ordinateurs, entre autres produits. Ses propriétés chimiques le rendent efficace dans de nombreuses autres applications, notamment les convertisseurs catalytiques et les explosifs. Il est même utilisé dans le carburant pour fusées – 180 000 kg (400 000 lb) sont consommés lors de chaque lancement de navette spatiale. Environ 10% de l’alumine produite chaque année est utilisée pour des applications autres que la fabrication d’aluminium.
Le plus grand déchet généré par le raffinage de la bauxite est constitué par les résidus (déchets de minerai) appelés « boue rouge ». Une raffinerie produit environ la même quantité de boue rouge que d’alumine (en termes de poids sec). Ces boues contiennent des substances utiles, comme du fer, du titane, de la soude et de l’alumine, mais personne n’a réussi à mettre au point un procédé économique pour les récupérer. À l’exception d’une petite quantité de boue rouge qui est utilisée commercialement pour colorer la maçonnerie, il s’agit véritablement d’un déchet. La plupart des raffineries se contentent de recueillir la boue rouge dans un bassin ouvert qui permet à une partie de son humidité de s’évaporer ; lorsque la boue a séché jusqu’à atteindre une consistance suffisamment solide, ce qui peut prendre plusieurs années, elle est recouverte de terre ou mélangée à de la terre.
Plusieurs types de déchets sont générés par la décomposition des électrodes de carbone pendant l’opération de fusion. Les usines d’aluminium aux États-Unis créent des quantités importantes de gaz à effet de serre, générant chaque année environ 5,5 millions de tonnes (5 millions de tonnes métriques) de dioxyde de carbone et 3 300 tonnes (3 000 tonnes métriques) de perfluorocarbones (composés de carbone et de fluor).
Environ 120 000 tonnes (110 000 tonnes métriques) de matériaux de revêtement de poterie usagé (SPL) sont retirés des pots de réduction en aluminium chaque année. Désigné comme une matière dangereuse par l’Agence de protection de l’environnement (EPA), le SPL a posé un problème d’élimination important pour l’industrie. En 1996, la première d’une série planifiée d’usines de recyclage a été ouverte ; ces usines transforment le SPL en fritte de verre, un produit intermédiaire à partir duquel le verre et la céramique peuvent être fabriqués. En fin de compte, le SPL recyclé apparaît dans des produits tels que les carreaux de céramique, les fibres de verre et les granules de bardeaux d’asphalte.
L’avenir
La quasi-totalité des producteurs d’aluminium des États-Unis sont membres du Voluntary Aluminum Industrial Partnership (VAIP), une organisation qui travaille en étroite collaboration avec l’EPA pour trouver des solutions aux problèmes de pollution auxquels l’industrie est confrontée. L’un des principaux axes de recherche consiste à développer un matériau d’électrode inerte (chimiquement inactif) pour les cuves de réduction de l’aluminium. Un composé titane-diborure-graphite est très prometteur. Parmi les avantages attendus lorsque cette nouvelle technologie sera perfectionnée figurent l’élimination des émissions de gaz à effet de serre et une réduction de 25 % de la consommation d’énergie pendant l’opération de fusion.
– Loretta Hall