Retrouver les sources : « Isotopes du béryllium » – actualités – journaux – livres – savant – JSTOR (mai 2018) (Learn how and when to remove this template message)
Le béryllium (4Be) possède 11 isotopes et 3 isomères connus, mais un seul de ces isotopes (9
Be
) est stable et constitue un nucléide primordial. En tant que tel, le béryllium est considéré comme un élément monoisotopique. C’est également un élément mono-isotopique, car ses autres isotopes ont des demi-vies si courtes qu’aucun n’est primordial et que leur abondance est très faible (le poids atomique standard est de 9,0122). Le béryllium a la particularité d’être le seul élément monoisotopique possédant à la fois un nombre pair de protons et un nombre impair de neutrons. Il existe 25 autres éléments monoisotopes mais tous ont un numéro atomique impair, et un nombre pair de neutrons.
|
||||||||||||||||||||||||||||||
| Standard atomic weight Ar, standard(Be) |
|
|||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
Of the 10 radioisotopes of beryllium, the most stable are 10
Be
with a half-life of 1.39 million years and 7
Be
with a half-life of 53.22 days. All other radioisotopes have half-lives under 15 seconds, most under 0.03 seconds. The least stable isotope is 16
Be
, with a half-life measured as 6.5 × 10−22 seconds.
The 1:1 neutron–proton ratio seen in stable isotopes of many light elements (up to oxygen, and in elements with even atomic number up to calcium) is prevented in beryllium by the extreme instability of 8
Be
toward alpha decay, which is favored due to the extremely tight binding of 4
He
nuclei. La demi-vie de la désintégration de 8
Be
n’est que de 8,19(37)×10-17 secondes.
Le béryllium est empêché d’avoir un isotope stable à 4 protons et 6 neutrons par la très grande discordance du rapport neutrons-protons pour un élément aussi léger. Néanmoins, cet isotope, 10
Be
, a une demi-vie de 1,39 million d’années, ce qui indique une stabilité inhabituelle pour un isotope léger présentant un déséquilibre neutrons/protons aussi important. D’autres isotopes de béryllium encore possibles présentent des déséquilibres encore plus graves dans le nombre de neutrons et de protons, et sont donc encore moins stables.
La plupart des 9
Be
dans l’univers seraient formés par nucléosynthèse à partir de la spallation des rayons cosmiques dans la période comprise entre le Big Bang et la formation du système solaire. Les isotopes 7
Be
, dont la demi-vie est de 53,22 jours, et 10
Be
sont tous deux des nucléides cosmogéniques car ils sont produits à une échelle de temps récente dans le système solaire par spallation, comme le 14
C
. Ces deux radio-isotopes du béryllium présents dans l’atmosphère suivent le cycle des taches solaires et l’activité solaire, car celle-ci affecte le champ magnétique qui protège la Terre des rayons cosmiques. La vitesse à laquelle le 7
Be
à vie courte est transféré de l’air au sol est contrôlée en partie par la météo. La désintégration du 7
Be
dans le soleil est l’une des sources de neutrinos solaires, et le premier type jamais détecté à l’aide de l’expérience Homestake. La présence de 7
Be
dans les sédiments est souvent utilisée pour établir qu’ils sont frais, c’est-à-dire qu’ils ont moins d’environ 3-4 mois, soit environ deux demi-vies de 7
Be
.
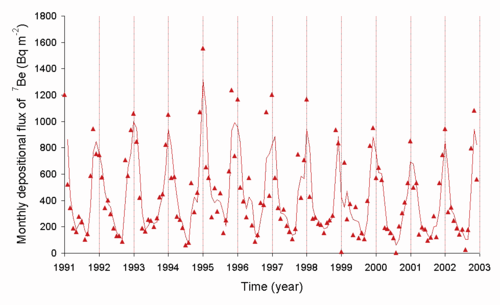
Be
de l’air au sol au Japon (source M. Yamamoto et al, Journal of Environmental Radioactivity, 2006, 8, 110-131)
.