Contrairement aux kinases, les enzymes phosphatases reconnaissent et catalysent un plus large éventail de substrats et de réactions. Par exemple, chez l’homme, les Ser/Thr kinases sont dix fois plus nombreuses que les Ser/Thr phosphatases. Dans une certaine mesure, cette disparité résulte d’une connaissance incomplète du phosphatome humain, c’est-à-dire de l’ensemble des phosphatases exprimées dans une cellule, un tissu ou un organisme. De nombreuses phosphatases n’ont pas encore été découvertes, et pour de nombreuses phosphatases connues, un substrat n’a pas encore été identifié. Cependant, parmi les paires phosphatase/kinase bien étudiées, les phosphatases présentent une plus grande variété que leurs homologues kinases, tant au niveau de la forme que de la fonction ; cela peut résulter du moindre degré de conservation parmi les phosphatases.

Phosphatases protéiquesModifier
Une protéine phosphatase est une enzyme qui déphosphoryle un résidu d’acide aminé de son substrat protéique. Alors que les protéines kinases agissent comme des molécules de signalisation en phosphorylant les protéines, les phosphatases éliminent le groupe phosphate, ce qui est essentiel pour que le système de signalisation intracellulaire puisse être réinitialisé pour une utilisation future. Le travail en tandem des kinases et des phosphatases constitue un élément important du réseau de régulation de la cellule. La phosphorylation (et la déphosphorylation) est l’un des modes les plus courants de modification post-traductionnelle des protéines, et l’on estime qu’à tout moment, jusqu’à 30 % de toutes les protéines sont phosphorylées.Deux phosphatases protéiques notables sont PP2A et PP2B. La PP2A est impliquée dans de multiples processus de régulation, tels que la réplication de l’ADN, le métabolisme, la transcription et le développement. La PP2B, également appelée calcineurine, est impliquée dans la prolifération des cellules T ; pour cette raison, elle est la cible de certains médicaments qui cherchent à supprimer le système immunitaire.
NucléotidasesEdit
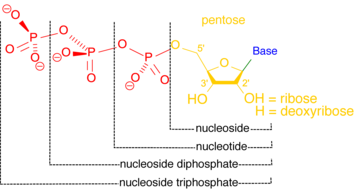
Une nucléotidase est une enzyme qui catalyse l’hydrolyse d’un nucléotide, formant un nucléoside et un ion phosphate. Les nucléotidases sont essentielles à l’homéostasie cellulaire, car elles sont partiellement responsables du maintien d’un rapport équilibré entre nucléotides et nucléosides. Certaines nucléotidases fonctionnent à l’extérieur de la cellule, créant des nucléosides qui peuvent être transportés dans la cellule et utilisés pour régénérer les nucléotides par des voies de récupération. À l’intérieur de la cellule, les nucléotidases peuvent contribuer à maintenir les niveaux d’énergie dans des conditions de stress. Une cellule privée d’oxygène et de nutriments peut cataboliser davantage de nucléotides pour augmenter les niveaux de nucléosides triphosphates tels que l’ATP, la principale monnaie d’énergie de la cellule.
Dans la gluconéogenèse
Les phosphatases peuvent également agir sur les glucides, tels que les intermédiaires de la gluconéogenèse. La gluconéogenèse est une voie de biosynthèse dans laquelle le glucose est créé à partir de précurseurs non glucidiques ; cette voie est essentielle car de nombreux tissus ne peuvent tirer de l’énergie que du glucose. Deux phosphatases, la glucose-6-phosphatase et la fructose-1,6-bisphosphatase, catalysent les étapes irréversibles de la gluconéogenèse. Chacune d’elles clive un groupe phosphate d’un intermédiaire sucre phosphate à six carbones.