USA Pharm. 2016;41(12):HS16-HS19.
ABSTRACT: A marihuánát vagy kannabiszt általában jóindulatú, káros hatások nélküli anyagnak tartják; a cannabinoid hyperemesis szindróma (CHS) azonban a krónikus kannabiszhasználat egyik következménye. A klinikusoknak erősen gyanakodniuk kell a CHS-re azoknál a hosszú távú kannabisz-használóknál, akiknél csillapíthatatlan hányinger és hányás jelentkezik, és akiknek tünetei forró vízben való fürdéssel enyhülnek. Az antiemetikumokra adott válasz hiánya segíthet a CHS diagnózisának felállításában. A CHS sikeres megoldására az egyetlen kezelés a kannabisztól való tartózkodás, bár a haloperidolt mint lehetséges kezelési lehetőséget jelenleg is vizsgálják. A CHS-t tapasztaló betegnek azt kell tanácsolni, hogy kerülje a kannabiszt, mert a további használat további tüneteket vált ki.
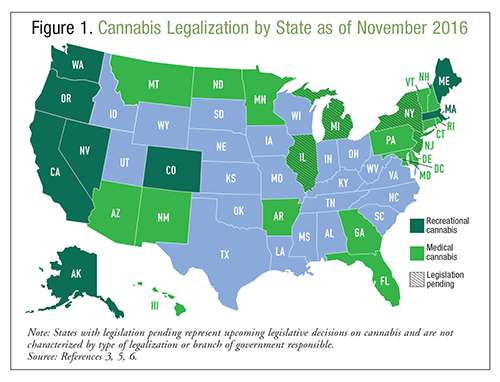
A marihuána vagy kannabisz a Cannabis sativa néven ismert kender növényből származó természetes termék; általában jóindulatú, káros hatások nélküli anyagnak tartják.1 A kannabiszt lehet elszívni, elpárologtatni vagy lenyelni mérgezés vagy terápiás céllal, és évszázadok óta használják ezekre a célokra. A 2014-es National Survey on Drug Use and Health szerint >22 millió amerikai használt kannabiszt az előző hónapban, így ez az anyag a leggyakrabban használt tiltott kábítószer.2 Várhatóan a kannabiszhasználat az Egyesült Államokban tovább fog nőni a növekvő legalizálási arányok miatt.3 A National Epidemiologic Survey on Alcohol and Related Conditions szerint az orvosi kannabiszt legalizáló államok lakói kétszer nagyobb valószínűséggel támogatják a kannabiszhasználatot, mint a legalizálás nélküli államok lakói.4 Jelenleg a kannabisz 28 államban használható gyógyászati célokra, és nyolc államban szabadidős célokra is. A kannabisz jogszerűségéről az Egyesült Államokban jelenleg az 1. ÁBRÁT lásd.3,5,6 A legalizálás mellett 21 állam és a Columbia körzet dekriminalizálta a kis mennyiségű kannabisz birtoklását. A kannabiszhasználattal kapcsolatos orvosi vészhelyzetek száma 2009 és 2011 között 29%-kal nőtt; nem tudni, hogy ez a növekedés a kannabisz erősségének, a fokozott legalizációnak vagy más tényezőknek köszönhető-e.1
Az emberi szervezetnek van egy belső kannabinoid rendszere, az úgynevezett endokannabinoid rendszer, amely neurotranszmittereket (pl. anandamid) tartalmaz, amelyek az étvágyat, az alvást, a fájdalmat, az érzelmeket és a mozgást szabályozzák.7,8 A kannabinoid bármely olyan vegyületre utal, amely a szervezet kannabinoid receptoraira hat. A terápiás célokat szolgáló receptorok közé tartoznak az 1-es és 2-es típusú kannabinoidok (CB1, CB2). A CB1 nagy mennyiségben az agyban, kisebb mennyiségben a gerincvelői és perifériás idegszövetekben található, míg a CB2 nagy mennyiségben a perifériás szövetekben és az immunrendszerben.8
A kannabisz >100 vegyi anyagot tartalmaz, amelyek közül a delta-9-tetrahidrokannabinol (THC) a legaktívabb vegyület. Mivel a CB1-hez kötődik, a THC felelős a kannabisz bódító hatásáért.1 A kannabiszban található egyéb kannabinoidok közé tartozik a kannabidiol és a kannabigerol, amelyek nem pszichoaktívak. Az intrinsikus rendszer által befolyásolt tevékenységek széles skálája miatt sokan használták a kannabinoidokat mérgezésre és terápiás célokra.
Cannabinoid hiperémiás szindróma
A kannabiszt használták az étvágy fokozására a HIV/AIDS-szel összefüggő anorexia és fogyókúra kezelésében, valamint a kemoterápia okozta hányinger és hányás enyhítésére. Bár a kannabisz alkalmazható az émelygés és hányás kezelésére, a kannabinoid hipermézis szindróma (CHS) néven ismert paradox hányinger és hányás szindrómát is okozhat. A CHS egy klinikai diagnózis, amelyet a krónikus kannabiszhasználat jellemez.9 A CHS egyedi jellemzője a ciklikus hányinger és hányás, amely nem reagál a szokásos hányáscsillapító kezelésre, de reagál a kényszeres forró fürdőzésre.3,9 A CHS-t dokumentáló első esetjelentés (2004) kilenc ausztráliai beteget írt le. A krónikus kannabiszhasználat a betegség megjelenését megelőzően történt, és a tünetek között hányinger és hányás szerepelt. A legtöbb beteg arról számolt be, hogy a tünetek enyhítése érdekében forró vízben fürdött. A kannabiszhasználat abbahagyása a betegség megszűnéséhez vezetett, míg a kannabiszhasználatot folytató betegek továbbra is betegek maradtak.10 Azóta további esetjelentések és sorozatok jelentek meg, amelyek a CHS további leírását adták; randomizált, kontrollált tanulmányok azonban nem értékelték vagy határozták meg.
Coloradóban a CHS aránya 2009 óta, a kannabisz legalizálása óta megduplázódott.3 Fontos azonban megjegyezni, hogy a CHS-t a klinikusok gyakran nem ismerik fel, ami a betegek kiterjedt és költséges kivizsgálásához vezethet. A diagnózis felállítása kihívást jelenthet, és a CHS-t tévesen sok más rendellenességként diagnosztizálhatják, beleértve a ciklikus hányás szindrómát (CVS). Bár a marihuánát használó betegek egy része CVS-t mutat, a CVS és a CHS között számos megkülönböztető tényező van. A CVS általában magában foglalja a migrén személyes vagy családi anamnézisét, a pszichiátriai rendellenességek kórtörténetét és a kényszeres forró fürdőzés hiányát.11 A CHS-ben szenvedő betegek gyakran a tünetek miatt jelentkeznek a sürgősségi osztályon (ED). A Soriano-Co és munkatársai által készített esetjelentés kimutatta, hogy a CHS-szel diagnosztizált betegeknél nagyobb valószínűséggel fordul elő gyakori klinikai látogatás, sürgősségi betegellátás és kórházi kezelés.12 Átlagosan egy betegnek öt klinikai látogatása, hét sürgősségi betegellátás és három kórházi kezelés volt a diagnózis felállítása előtt, ami azt jelzi, hogy a CHS-ben szenvedő betegek bármely ellátási környezetben megjelenhetnek.12 A diagnózist tovább nehezíti a szintetikus kannabinoidok, például a K2, más néven Spice használata, amely nem mutatható ki a vizeletben végzett drogszűrés során.13 A CHS-t meg kell különböztetni más, hányingert és hányást okozó rendellenességektől, és a diagnózis általában kizáró diagnózis.
Patofiziológia
A CHS patofiziológiájára vonatkozóan több hipotézis is létezik; a kannabiszban lévő aktív vegyi anyagok sokasága és a különböző hatáshelyek létezése miatt azonban a végleges patofiziológiai folyamat nem ismert. Ráadásul nem minden kannabiszhasználónál alakul ki CHS, ami további nehézséget okoz a szindróma leírásában.
A THC kis dózisban köztudottan hányáscsillapító hatást fejt ki, de erős és krónikus kannabiszhasználat esetén ennek ellenkezője figyelhető meg. Azt feltételezik, hogy a THC idővel felhalmozódik, mivel nagy az eloszlási mennyisége. A THC közvetlenül aktiválhatja a CB1 receptorokat az enterális idegrendszerben, és csökkentheti a gyomor motilitását, így túlzott aktiválással növelheti a hányinger és hányás kockázatát.9 A szintetikus kannabinoidok, amelyek a THC hatását és szerkezetét is utánozzák, feltételezhetően a CB1 receptor túlstimulációját okozzák, mivel erős agonista hatásuk van14. Ezek a CB1-receptorok a hipotalamuszban is megtalálhatók, és a hőszabályozás károsításával hányást válthatnak ki, ami a tünetek forró fürdőzéssel történő lehetséges enyhítéséhez vezet.9,11
Rizikótényezők, klinikai lefolyás és diagnózis
A CHS kialakulásának fő kockázati tényezője a krónikus kannabiszhasználat. A beteg CHS kockázata a hosszan tartó kannabiszhasználattal nő.9 Úgy tűnik, hogy a napi kannabiszhasználat nagyobb valószínűséggel okoz CHS-t, mint a ritkább használat; azonban bármilyen mennyiségű kannabisz CHS-hez vezethet.15
A CHS-nek több fázisa van, amelyeket preemetikus, hiperemetikus és gyógyulási fázisba soroltak.9,16 A preemetikus fázist, amely hónapoktól évekig is eltarthat, hányinger, hányástól való félelem és hasi panaszok jellemzik. Gyakran előfordul, hogy a kannabiszhasználók a preemetikus fázisban növelik a kannabiszbevitelt, hogy enyhítsék a hányingert.11 A hiperemetikus fázisban, amely jellemzően 24-48 óráig tart, a beteg gyakori hányingert és hányást tapasztal, amely súlyos jellegű. Ez súlyvesztéshez és akut dehidratációhoz vezethet, ami potenciálisan prerenális elégtelenséghez vezethet.17,18 A tartós hányinger és hányás elektrolit-rendellenességek kialakulásához vezethet.
A tünetek enyhítése érdekében a betegek forró fürdőzésbe kezdhetnek – azaz órákon át forró fürdőben vagy zuhanyzóban maradnak.11 Ez egy öntanult viselkedés, amely kényszeressé válik, amint a beteg felismeri az előnyöket. A forró fürdőzés segíthet a hőszabályozásban és a gyomorba áramló vér mennyiségének csökkentésében azáltal, hogy befolyásolja a perifériás értágulatot és a splanchnikus keringésből történő átcsoportosítást, ami a hányás csökkenését eredményezi.11 Sajnos a forró fürdőzés növelheti a dehidratáció és az akut veseelégtelenség kockázatát.17 A forró fürdőzést patognomikus jellemzőnek kell tekinteni, mivel más, egyébként hasonló megjelenésű állapotoknál nem fordul elő. A betegek jellemzően abbahagyják a forró fürdőzést, amikor a tünetek nem jelentkeznek, és újra elkezdik, amint a jövőbeni kannabiszhasználat után a hányinger és a hányás kiújul.
Sok beteg keresi fel orvosát a tünetei miatt a hiperémiás fázisban. Ennek eredményeképpen a betegek kiterjedt negatív vizsgálatoknak vethetik alá magukat különböző egyéb állapotok, például CVS, hasnyálmirigy-gyulladás és gasztroparézis miatt, amelyek utánozhatják a CHS egyes tüneteit. Amint az émelygés és a hányás megszűnik, általában 48 órán belül, a beteg a gyógyulási fázisba lép. A felépülés napoktól hónapokig terjedhet, és a kannabiszhasználat abbahagyásához kapcsolódik. Ha a beteg újra elkezdi a kannabiszhasználatot, a tünetek általában visszatérnek.11
Nagyon fontos figyelembe venni a CHS hatását a beteg egyéb betegségállapotaira. Vannak esetleírások olyan CHS-es betegekről, akiknél a veseelégtelenségen kívül más, CHS-hez kapcsolódó egészségügyi problémák is kialakultak. Gregoire és munkatársai leírtak egy bipoláris mániás és kannabiszhasználó beteget, akinél CHS alakult ki.19 A beteg a csillapíthatatlan hányást a lítiumnak tulajdonította, és abbahagyta a lítium szedését, mire mániás epizód következett be. A kórházban a lítium újraindítása nem váltott ki további hányást, ami arra utal, hogy valószínűleg a kannabisz volt az ok.19
A CHS diagnosztikai kritériumait javasolták. A hosszú távú kannabiszhasználat elengedhetetlen a diagnózishoz. A CHS kialakulásához szükséges idő hossza változó; a legtöbb beteg azonban 1-5 évvel a krónikus kannabiszhasználat után jelentkezik. A CHS-hez hasonló tünetek jelentkezése a krónikus kannabiszhasználat 1 éve előtt nem zárja ki a diagnózist. A CHS fő jellemzői közé tartozik a súlyos, ciklikusan jelentkező hányinger és hányás, a tünetek megszűnése a kannabisz abbahagyásakor, a forró vízben való fürdéssel elért enyhülés, epigasztrikus vagy periumbilikális hasi fájdalom és a heti kannabiszhasználat. A CHS diagnózisát alátámasztó jellemzők közé tartozik az életkor <50 év, testsúlycsökkenés >5 kg, a tünetek reggeli jelentkezése, normális bélműködés és normális leletek más vizsgálatok során.15 Az 1. TÁBLÁZAT összefoglalja a CHS diagnózisát alátámasztó gyakori leleteket.14

Potenciális kezelések
A CHS hyperemetikus fázisában jelentkező valamennyi beteg esetében a támogató kezelés javallt. Ha a beteg elviseli, szájon át történő folyadékbevitel javasolt a hidratálás érdekében. Néhány beteg a túlzott hányás miatt nem tolerálja az orális hidratálást, ezért a dehidratációval járó térfogatcsökkenés miatt intravénás folyadékpótlás javallott lehet.11 Mivel hányással elektrolit-zavarok léphetnek fel, az elektrolitok ellenőrzése és pótlása javallott.
A kényszeres forró fürdőzés egy jellegzetes tanult viselkedés, amelyet a betegek a CHS-sel járó tünetek minimalizálására használhatnak. Amint azt korábban tárgyaltuk, a forró fürdőzés segíthet a hőszabályozásban. Egy másik elmélet szerint a perifériás vazodilatáció és a splanchnikus keringésből történő redisztribúció csökkentheti a gyomorba irányuló véráramlást, ami a hányás csökkenését eredményezi.11 Egyetlen esetjelentés jelezte, hogy a tünetek forró fürdőzés általi enyhülése idővel csökkenhet; ez a jelenség azonban ritkának tűnik.20
Az antiemetikumokat sikertelenül alkalmazták a CHS tüneteinek enyhítésére. Az antiemetikumokra adott válasz hiánya miatt a klinikusnak CHS-re kell gyanakodnia. Esetjelentések szerint a betegeknél az ondansetron, prometazin, klórpromazin vagy metoklopramid nem enyhítette terápiásan a hányingert és hányást.21 Egy kis esetsorozatban a betegek 87,5%-a nem reagált a standard antiemetikus kezelésre.12
A kaloperidol antipszichotikus hatását a dopamin D2-receptorok antagonizálásával fejti ki a mezolimbikus és mezokortikális pályákon. A haloperidolt hagyományosan az agitáció kezelésére használják; azonban az általános sebészetben és az onkológiában is sikeresen alkalmazzák antiemetikumként. A D2-receptorok a kemoreceptorok kiváltó zónájában is jelen vannak, ami magyarázatot adhat ezekre az antiemetikus tulajdonságokra. Állatkísérletek azt sugallják, hogy a CB1-re hatással lehet a haloperidol, ami ezt a szert potenciális kezelési lehetőséggé teszi.22,23 Witsil és Mycyk visszamenőlegesen értékelte ezt a hipotézist négy, a standard antiemetikus terápiára refrakter hányingerben és hányásban szenvedő betegnél.21 Minden betegnél az intravénásan adott 5 mg haloperidol 1-2 órán belül enyhülést tapasztalt.21,24 Ez a kis esettanulmány azt mutatja, hogy a haloperidol eléggé enyhítheti a CHS-hez kapcsolódó hányingert és hányást ahhoz, hogy megelőzze a kórházi felvételt, ami költségmegtakarítást eredményezhet az egészségügyi rendszer számára.19 Figyelembe kell venni a QTc-meghosszabbodás kockázatát haloperidollal, különösen a túlzott hányás következtében elektrolit-zavarban szenvedő betegek esetében. További vizsgálatok indokoltak a haloperidol terápiában elfoglalt helyének és optimális adagolásának meghatározására.
A kannabisz abbahagyása az egyetlen olyan kezelés, amely enyhíti és megelőzi a CHS-hez társuló tüneteket. A CHS-t először leíró tanulmányban a kannabisz absztinenciája 10 betegből hétnél a hányinger és hányás megszűnését eredményezte, míg a többieknél a betegség továbbra is folyamatos volt. A hét beteg közül három később újra kannabiszhoz nyúlt, és a tünetek néhány hónapon belül visszatértek.10 Ezeket az eredményeket a közelmúltbeli esetjelentések is megismételték.12,25 A betegeket fel kell világosítani a kannabiszról mint tünetcsökkentőről való leszokásról, és a leszokást segítő forrásokat kell biztosítani.
Következtetés
Mivel több államban legalizálják a kannabiszt, valószínű, hogy használata növekedni fog, és több CHS-es esetet fognak jelenteni. A klinikusoknak CHS-re kell gyanakodniuk azoknál a betegeknél, akik kannabisz- vagy szintetikus kannabinoid-használatról és olyan tünetekről számolnak be, mint a kezelhetetlen hányinger és hányás, valamint arról számolnak be, hogy a tünetek ellenőrzésére forró fürdőt használnak. Ez a feltételezés megelőzheti az egyéb állapotok miatt végzett kiterjedt és költséges vizsgálatokat. A gyógyszerészeknek szerepük van abban, hogy tanácsot adjanak a betegeknek a kannabiszhasználattal kapcsolatos kockázatokról, és a CHS tüneteit mutató betegeket megfelelő utókezelésre utalják. A szakirodalomban található esetleírások azonosították a CHS kockázati tényezőit. Sajnos a CHS viszonylag kevéssé ismert, és pontos mechanizmusa nem ismert. A CHS diagnózisa és kezelése jelenleg kis esetszámú beszámolókon alapul. Az információkat továbbra is értékelni kell, amint azok rendelkezésre állnak, a megfelelő kezelés biztosítása érdekében.
1. Nemzeti Drogfogyasztási Intézet (NIDA). Mi a marihuána? www.drugabuse.gov/publications/research-reports/marijuana/what-marijuana. Hozzáférés 2016. augusztus 25.
2. NIDA. Milyen mértékű a marihuánafogyasztás az Egyesült Államokban? www.drugabuse.gov/publications/research-reports/marijuana/what-scope-marijuana-use-in-united-states. Hozzáférés 2016. augusztus 25.
3. Kim HS, Monte AA. A coloradói kannabisz legalizációja és annak hatása a sürgősségi ellátásra. Ann Emerg Med. 2016;68:71-75.
4. Cerdá M, Wall M, Keyes KM, et al. Medical marijuana laws in 50 states: investigating the relationship between state legalization of medical marijuana and marijuana use, abuse and dependence. Drug Alcohol Depend. 2012;120:22-27.
5. CNN Money. Ahol legális a fű. http://money.cnn.com/interactive/news/economy/marijuana-legalization-map/index.html. Hozzáférés 2016. augusztus 25.
6. Marijuana Policy Project. 2016-os marihuánapolitikai reformtörvények. www.mpp.org/states/key-marijuana-policy-reform. Hozzáférés 2016. november 13.
7. NIDA. Hogyan fejti ki hatását a marihuána? www.drugabuse.gov/publications/research-reports/marijuana/how-does-marijuana-produce-its-effects. Hozzáférés 2016. augusztus.
8. Manzanares J, Julian MD, Carrascosa A. A kannabinoid rendszer szerepe a fájdalom szabályozásában és terápiás implikációk az akut és krónikus fájdalom epizódok kezelésében. Curr Neuropharmacol. 2006;4:239-257.
9. Galli JA, Sawaya RA, Friedenberg FK. Cannabinoid hyperemesis szindróma. Curr Drug Abuse Rev. 2011;4:
241-249.
10. Allen JH, de Moore GM, Heddle R, Twartz JC. Cannabinoid hyperemesis: ciklikus hyperemesis krónikus kannabiszfogyasztással összefüggésben. Gut. 2004;53:1566-1570.
11. Ruffle JK, Bajgoric S, Samra K, et al. Cannabinoid hyperemesis szindróma: a tartós megmagyarázhatatlan hányás fontos differenciáldiagnózisa. Eur J Gastroenterol Hepatol. 2015;27:1403-1408.
12. Soriano-Co M, Batke M, Cappell MS. A cannabis hyperemesis szindróma, amelyet tartós hányinger és hányás, hasi fájdalom és kényszeres fürdés jellemez, és amely krónikus marihuána használathoz társul: jelentés nyolc esetről az Egyesült Államokban. Dig Dis Sci. 2010;55:3113-3119.
13. Ukaigwe A, Karmacharya P, Donato A. A gut gone to pot: a K2, egy szintetikus kannabinoid okozta cannabinoid hyperemesis szindróma esete. Case Rep Emerg Med. 2014;2014:167098.
14. Hopkins CY, Gilchrist BL. A szintetikus kannabinoidok által okozott kannabinoid-hyperézis-szindróma esete. J Emerg Med. 2013;45:544-546.
15. Simonetto DA, Oxentenko AS, Herman ML, Szostek JH. Cannabinoid hyperemesis: 98 beteg esetsorozata. Mayo Clin Proc. 2012;87:114-119.
16. Lu ML, Agito MD. Cannabinoid hyperemesis szindróma: a marihuána egyszerre antiemetikus és proemetikus. Cleve Clin J Med. 2015;82:429-434.
17. Habboushe J, Sedor J. Cannabinoid hyperemesis akut veseelégtelenség: a cannabinoid hyperemesis szindróma gyakori következménye. Am J Emerg Med. 2014;32:690.e1-e2.
18. Srihari P, Liu M, Punzell S, et al. Cannabinoid hyperemesis szindróma társulva kényszeres zuhanyozással és akut vesekárosodással. Prim Care Companion CNS Disord. 2016;18(1).
19. Gregoire P, Tau M, Robertson D. Cannabinoid hyperemesis szindróma és mániás epizód kialakulása. BMJ Case Rep. 2016;2016.
20. Bagdure S, Smalligan RD, Sharifi H, Khandheria B. A kényszeres fürdés csökkenő hatása cannabinoid hyperemesisben. Am J Addict. 2012;21:184-185.
21. Witsil JC, Mycyk MB. Haloperidol, a cannabinoid hyperemesis szindróma újszerű kezelése. Am J Ther. 2014 Nov 12 .
22. Schulze DR, Carroll FI, McMahon LR. A dopamin transzporter és a kannabinoid receptor ligandumok közötti kölcsönhatások rhesusmajmokban. Psychopharmacology (Berl). 2012;222:425-438.
23. Desai RI, Thakur GA, Vemuri VK, et al. A tolerancia és a viselkedési/fizikai függőség elemzése krónikus CB1 agonista kezelés során: CB1 agonisták, antagonisták és nem kannabinoid gyógyszerek hatása. J Pharmacol Exp Ther. 2013;344:319-328.
24. Hickey JL, Witsil JC, Mycyk MB. Haloperidol a kannabinoid hyperemesis szindróma kezelésére. Am J Emerg Med. 2013;31:1003.e5-e6.
25. Pélissier F, Claudet I, Gandia-Mailly P, et al. Cannabis hyperemesis syndrome in the emergency department: hogyan lehet hasznos egy speciális függőségi csapat? Egy kísérleti tanulmány. J Emerg Med. 2016;51:544-551.