Effetto Fotoelettrico e la Natura Particellare della Luce
Nel 1905, Albert Einstein (1879-1955) propose che la luce fosse descritta come quanti di energia che si comportano come particelle. Un fotone è una particella di radiazione elettromagnetica che ha massa zero e porta un quantum di energia. L’energia dei fotoni di luce è quantizzata secondo l’equazione (E = h \nu). Per molti anni la luce era stata descritta usando solo concetti ondulatori, e gli scienziati formati in fisica classica trovavano questa dualità onda-particella della luce un’idea difficile da accettare. Un concetto chiave che fu spiegato da Einstein usando la natura particellare della luce fu chiamato effetto fotoelettrico.
L’effetto fotoelettrico è un fenomeno che si verifica quando la luce che colpisce una superficie metallica causa l’espulsione di elettroni da quel metallo. È stato osservato che solo certe frequenze di luce sono in grado di causare l’espulsione di elettroni. Se la frequenza della luce incidente era troppo bassa (luce rossa, per esempio), allora non venivano espulsi elettroni, anche se l’intensità della luce era molto alta o se veniva fatta brillare sulla superficie per molto tempo. Se la frequenza della luce era più alta (luce verde, per esempio), allora gli elettroni potevano essere espulsi dalla superficie metallica anche se l’intensità era molto bassa o se veniva illuminata per poco tempo. Questa frequenza minima necessaria per provocare l’espulsione degli elettroni viene chiamata frequenza di soglia.
La fisica classica non era in grado di spiegare l’effetto fotoelettrico. Se la fisica classica fosse stata applicata a questa situazione, l’elettrone nel metallo avrebbe potuto raccogliere abbastanza energia per essere espulso dalla superficie anche se la luce in arrivo era di bassa frequenza. Einstein ha usato la teoria delle particelle della luce per spiegare l’effetto fotoelettrico come mostrato nella figura qui sotto.
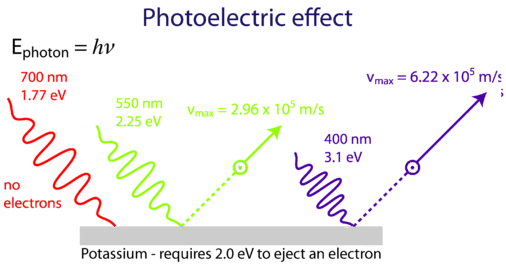
La luce a bassa frequenza (rossa) non è in grado di causare l’espulsione degli elettroni dalla superficie del metallo. A una frequenza pari o superiore alla soglia (verde) gli elettroni vengono espulsi. Anche la luce in entrata a frequenza più alta (blu) causa l’espulsione dello stesso numero di elettroni, ma con maggiore velocità.
Considera l’equazione \(E = h \nu\). Il \(E \) è l’energia minima che è richiesta perché l’elettrone del metallo venga espulso. Se la frequenza della luce in arrivo, \nu\, è inferiore alla frequenza di soglia, non ci sarà mai abbastanza energia per causare l’espulsione degli elettroni. Se la frequenza è uguale o superiore alla frequenza di soglia, gli elettroni saranno espulsi. Quando la frequenza aumenta oltre la soglia, gli elettroni espulsi si muovono semplicemente più velocemente. Un aumento dell’intensità della luce in entrata al di sopra della frequenza di soglia fa aumentare il numero di elettroni espulsi, ma questi non viaggiano più velocemente. L’effetto fotoelettrico è applicato in dispositivi chiamati cellule fotoelettriche, che si trovano comunemente in oggetti di uso quotidiano (come una calcolatrice) che usano l’energia della luce per generare elettricità.

Le cellule fotoelettriche convertono l’energia luminosa in energia elettrica, che alimenta questa calcolatrice.