Dosage Form: powder for oral suspension
Medically reviewed by Drugs.com. Last updated on April 1, 2019.
- Overview
- Side Effects
- Dosage
- Professional
- Tips
- Interactions
- More
- INDICATIONS & USAGE
- Respiratory Tract Infections
- Otitis Media
- Infezioni della pelle e della struttura della pelle
- Infezioni ossee
- Infezioni del tratto genitourinario
- Usage
- DOSAGGIO & AMMINISTRAZIONE
- Adulti e pazienti pediatrici con almeno 15 anni di età
- Pazienti pediatrici (oltre 1 anno di età)
- Regolazioni del dosaggio in pazienti adulti e pediatrici di almeno 15 anni di età con insufficienza renale
- FORME DI DOSAGGIO & Dosi
- Contraindicazioni
- Avvertenze e precauzioni
- Reazioni di ipersensibilità
- Diarrea associata a Clostridium difficile
- Sieroconversione diretta del test di Coombs
- Potenziale di convulsioni
- Tempo di protrombina prolungato
- Sviluppo di batteri farmaco-resistenti
- Reazioni avverse
- Esperienza negli studi clinici
- Interazioni farmacologiche
- Metformina
- Probenecid
- Interazione con laboratorio o test diagnostici
- USO IN POPOLAZIONI SPECIFICHE
- Gravidanza
- Madri che allattano
- Uso pediatrico
- Uso geriatrico
- Depressione renale
- sovradosaggio
- Descrizione della sospensione di cefalexina
- Cefalexina sospensione – Farmacologia clinica
- Meccanismo d’azione
- Farmacocinetica
- Microbiologia
- Nonclinical Toxicology
- Carcinogenesis & Mutagenesis & Impairment Of Fertility
- How Supplied/Storage and Handling
- Informazioni per il paziente
- ETICHETTA DELLA CONFEZIONE.SCHEDA PRINCIPALE
- Frequently asked questions
- More about cephalexin
- Consumer resources
- Professional resources
- Related treatment guides
INDICATIONS & USAGE
Respiratory Tract Infections
Cephalexin is indicated for the treatment of respiratory tract infections caused by susceptible isolates of Streptococcus pneumoniae and Streptococcus pyogenes.
Otitis Media
Cephalexin is indicated for the treatment of otitis media caused by susceptible isolates of Streptococcus pneumoniae, Haemophilus influenzae, Staphylococcus aureus, Streptococcus pyogenes, and Moraxella catarrhalis.
Infezioni della pelle e della struttura della pelle
Cefalexina è indicata per il trattamento di infezioni della pelle e della struttura della pelle causate da isolati sensibili dei seguenti batteri Gram-positivi: Staphylococcus aureus e Streptococcus pyogenes.
Infezioni ossee
Cephalexin è indicato per il trattamento delle infezioni ossee causate da isolati sensibili di Staphylococcus aureus e Proteus mirabilis.
Infezioni del tratto genitourinario
Cefalexina è indicata per il trattamento di infezioni del tratto genitourinario, incluso prostatite acuta, causate da isolati sensibili di Escherichia coli, Proteus mirabilis e Klebsiella pneumoniae.
Usage
Per ridurre lo sviluppo di batteri resistenti ai farmaci e mantenere l’efficacia della cefalexina e di altri farmaci antibatterici, la cefalexina deve essere usata solo per trattare infezioni che sono provate o fortemente sospettate di essere causate da batteri sensibili. Quando sono disponibili informazioni sulla coltura e sulla suscettibilità, queste informazioni dovrebbero essere considerate nella selezione o nella modifica della terapia antibatterica. In assenza di tali dati, l’epidemiologia locale e i modelli di suscettibilità possono contribuire alla selezione empirica della terapia.
DOSAGGIO & AMMINISTRAZIONE
Adulti e pazienti pediatrici con almeno 15 anni di età
La dose usuale di cefalexina orale è 250 mg ogni 6 ore, ma può essere somministrata una dose di 500 mg ogni 12 ore. Il trattamento viene somministrato per 7-14 giorni.
Per infezioni più gravi possono essere necessarie dosi più grandi di cefalexina orale, fino a 4 grammi al giorno in due o quattro dosi equamente divise.
Pazienti pediatrici (oltre 1 anno di età)
La dose giornaliera totale raccomandata di cefalexina orale per i pazienti pediatrici è di 25-50 mg/kg somministrata in dosi equamente divise per 7-14 giorni. Nel trattamento delle infezioni da streptococco β-emolitico, si raccomanda una durata di almeno 10 giorni. In severe infections, a total daily dose of 50 to 100 mg/kg may be administered in equally divided doses.
For the treatment of otitis media, the recommended daily dose is 75 to 100 mg/kg given in equally divided doses.
| Weight 10 kg (22 lb) 20 kg (44 lb) 40 kg (88 lb) |
Cephalexin Suspension 125mg/5mL ½ to 1 tsp q.i.d. 1 to 2 tsp q.i.d. 2 to 4 tsp q.i.d. |
250mg/5mL ¼ to ½ tsp q.i.d. ½ to 1 tsp q.i.d. 1 to 2 tsp q.i.d. |
| Weight 10 kg (22 lb) 20 kg (44 lb) 40 kg (88 lb) |
125mg/5mL 1 to 2 tsp b.i.d. 2 to 4 tsp b.i.d. 4 to 8 tsp b.i.d. |
250mg/5mL ½ to 1 tsp b.i.d 1 to 2 tsp b.i.d. 2 to 4 tsp b.i.d. |
Direzioni per la miscelazione
125 mg per 5 mL (100 mL quando miscelato): Preparare la sospensione al momento dell’erogazione. Aggiungere alla bottiglia un totale di 67 mL di acqua. Per facilitare la preparazione, battere il flacone per allentare la polvere, aggiungere l’acqua in 2 porzioni, agitando bene dopo ogni aggiunta. La sospensione risultante conterrà cefalexina monoidrato equivalente a 125 mg di cefalexina in ogni 5 mL (cucchiaino da tè).
125 mg per 5 mL (200 mL quando mescolato): Preparare la sospensione al momento dell’erogazione. Aggiungere alla bottiglia un totale di 134 mL di acqua. Per facilitare la preparazione, battere la bottiglia per allentare la polvere, aggiungere l’acqua in 2 porzioni, agitando bene dopo ogni aggiunta. La sospensione risultante conterrà cefalexina monoidrato equivalente a 125 mg di cefalexina in ogni 5 mL (cucchiaino da tè).
250 mg per 5 mL (100 mL quando mescolato): Preparare la sospensione al momento dell’erogazione. Aggiungere alla bottiglia un totale di 67 mL di acqua. Per facilitare la preparazione, battere la bottiglia per allentare la polvere, aggiungere l’acqua in 2 porzioni, agitando bene dopo ogni aggiunta. La sospensione risultante conterrà cefalexina monoidrato equivalente a 250 mg di cefalexina in ogni 5 mL (cucchiaino da tè).
250 mg per 5 mL (200 mL quando mescolato): Preparare la sospensione al momento dell’erogazione. Aggiungere alla bottiglia un totale di 134 mL di acqua. Per facilitare la preparazione, battere la bottiglia per allentare la polvere, aggiungere l’acqua in 2 porzioni, agitando bene dopo ogni aggiunta. La sospensione risultante conterrà cefalexina monoidrato equivalente a 250 mg di cefalexina in ogni 5 mL (cucchiaino da tè).
*Dopo la miscelazione, conservare in frigorifero. Può essere conservato per 14 giorni senza perdita significativa di potenza.
Regolazioni del dosaggio in pazienti adulti e pediatrici di almeno 15 anni di età con insufficienza renale
Amministrare i seguenti regimi di dosaggio per cefalexina a pazienti con funzione renale compromessa.
Tabella 1. Recommended Dose Regimen for Patients with Renal Impairment
| Renal function | Dose regimen recommendation |
| Creatinine clearance ≥60 mL/min | No dose adjustment |
| Creatinine clearance 30 to 59 mL/min | No dose adjustment; maximum daily dose should not exceed 1 g |
| Creatinine clearance 15 to 29 mL/min | 250 mg, every 8 hours or every 12 hours |
| Creatinine clearance 5 to 14 mL/min not yet on dialysis* | 250 mg, every 24 hours |
| Creatinine clearance 1 to 4 mL/min not yet on dialysis* | 250 mg, ogni 48 ore o ogni 60 ore |
*Non ci sono informazioni sufficienti per fare raccomandazioni di aggiustamento della dose in pazienti in emodialisi.
FORME DI DOSAGGIO & Dosi
Cefalexina per sospensione orale USP
125 mg/5mL e 250 mg/5mL
Contraindicazioni
Cephalexin è controindicato nei pazienti con ipersensibilità conosciuta a cefalexina o ad altri membri della classe di cefalosporina dei farmaci antibatterici.
Avvertenze e precauzioni
Reazioni di ipersensibilità
Reazioni allergiche nella forma di esantema, orticaria, angioedema, anafilassi, eritema multiforme, sindrome di Stevens-Johnson o necrolisi epidermica tossica sono stati riportati con l’uso di cefalexina. Prima di istituire la terapia con cefalexina, informarsi se il paziente ha una storia di reazioni di ipersensibilità alla cefalexina, cefalosporine, penicilline o altri farmaci. L’ipersensibilità incrociata tra i farmaci antibatterici beta-lattamici può verificarsi fino al 10% dei pazienti con una storia di allergia alla penicillina.
Se si verifica una reazione allergica alla cefalexina, interrompere il farmaco e istituire un trattamento adeguato.
Diarrea associata a Clostridium difficile
Diarrea associata a Clostridium difficile (CDAD) è stata riportata con l’uso di quasi tutti gli agenti antibatterici, incluso cephalexin, e può variare in gravità da diarrea leggera a colite fatale. Il trattamento con agenti antibatterici altera la flora normale del colon portando alla crescita eccessiva di C. difficile.
C. difficile produce tossine A e B, che contribuiscono allo sviluppo di CDAD. I ceppi di C. difficile che producono ipertossine causano una maggiore morbilità e mortalità, poiché queste infezioni possono essere refrattarie alla terapia antimicrobica e possono richiedere la colectomia. La CDAD deve essere considerata in tutti i pazienti che presentano diarrea dopo l’uso di antibiotici. È necessaria un’attenta anamnesi poiché è stato riportato che la CDAD si verifica più di due mesi dopo la somministrazione di agenti antibatterici.
Se la CDAD è sospettata o confermata, può essere necessario interrompere l’uso di antibiotici in corso non diretti contro il C. difficile. La gestione appropriata dei fluidi e degli elettroliti, l’integrazione proteica, il trattamento antibiotico del C. difficile e la valutazione chirurgica devono essere istituiti come clinicamente indicato.
Sieroconversione diretta del test di Coombs
I test di Coombs diretti positivi sono stati riportati durante il trattamento con i farmaci antibatterici cefalosporici inclusa la cefalexina. È stata riportata un’emolisi intravascolare acuta indotta dalla terapia con cefalexina. Se l’anemia si sviluppa durante o dopo la terapia con cefalexina, eseguire un work-up diagnostico per l’anemia emolitica farmaco-indotta, interrompere la cefalexina e istituire una terapia appropriata.
Potenziale di convulsioni
Diverse cefalosporine sono state implicate nell’innesco di convulsioni, particolarmente in pazienti con insufficienza renale quando il dosaggio non è stato ridotto. Se le convulsioni si verificano, interrompere la cefalexina. Una terapia anticonvulsivante può essere data se clinicamente indicato.
Tempo di protrombina prolungato
Le cefalosporine possono essere associate con tempo di protrombina prolungato. Quelli a rischio includono pazienti con insufficienza renale o epatica, o povero stato nutrizionale, così come pazienti che ricevono un corso prolungato di terapia antibatterica, e pazienti che ricevono terapia anticoagulante. Monitorare il tempo di protrombina nei pazienti a rischio e gestire come indicato.
Sviluppo di batteri farmaco-resistenti
Prescrivere cefalexina in assenza di un’infezione batterica provata o fortemente sospetta è improbabile che fornisca beneficio al paziente e aumenta il rischio di sviluppo di batteri farmaco-resistenti.
L’uso prolungato di cefalexina può causare la crescita eccessiva di organismi non sensibili. Un’attenta osservazione del paziente è essenziale. Se si verifica una superinfezione durante la terapia, devono essere prese misure appropriate.
Reazioni avverse
I seguenti eventi gravi sono descritti più dettagliatamente nella sezione Avvertenze e precauzioni:
– Reazioni di ipersensibilità
– Diarrea associata a Clostridium difficile
– Sieroconversione del test di Coombs diretto
– Potenziale convulsivo
– Effetto sull’attività della protrombina
– Sviluppo di batteri resistenti ai farmaci
Esperienza negli studi clinici
Perché gli studi clinici sono condotti in condizioni molto diverse, i tassi di reazione avversa osservati negli studi clinici di un farmaco non possono essere direttamente confrontati con i tassi negli studi clinici di un altro farmaco e possono non riflettere i tassi osservati nella pratica.
Negli studi clinici, la reazione avversa più frequente è stata la diarrea. Si sono verificati anche nausea e vomito, dispepsia, gastrite e dolore addominale. Come con le penicilline e altre cefalosporine, sono stati riportati epatite transitoria e ittero colestatico.
Altre reazioni hanno incluso reazioni di ipersensibilità, prurito genitale e anale, candidosi genitale, vaginite e perdite vaginali, vertigini, affaticamento, mal di testa, agitazione, confusione, allucinazioni, artralgia, artrite e disturbi articolari. È stata riportata nefrite interstiziale reversibile. Eosinofilia, neutropenia, trombocitopenia, anemia emolitica e lievi aumenti di aspartato transaminasi (AST) e alanina transaminasi (ALT) sono stati riportati.
In aggiunta alle reazioni avverse elencate sopra che sono state osservate in pazienti trattati con cefalexina, le seguenti reazioni avverse e altri test di laboratorio alterati sono stati riportati per farmaci antibatterici della classe cefalosporina:
Altre reazioni avverse: Febbre, colite, anemia aplastica, emorragia, disfunzione renale e nefropatia tossica.
Test di laboratorio alterati: Tempo di protrombina prolungato, aumento dell’azoto ureico nel sangue (BUN), aumento della creatinina, fosfatasi alcalina elevata, bilirubina elevata, lattato deidrogenasi elevata (LDH), pancitopenia, leucopenia e agranulocitosi.
Interazioni farmacologiche
Metformina
Somministrazione di cefalexina con metformina provoca aumento delle concentrazioni plasmatiche di metformina e diminuzione della clearance renale di metformina.
Si raccomanda un attento monitoraggio del paziente e aggiustamento della dose di metformina nei pazienti che assumono contemporaneamente cefalexina e metformina.
Probenecid
L’escrezione renale di cefalexina è inibita da probenecid. La co-somministrazione di probenecid con cefalexina non è raccomandata.
Interazione con laboratorio o test diagnostici
Una reazione falso-positiva può verificarsi quando si testa la presenza di glucosio nelle urine usando la soluzione di Benedict o la soluzione di Fehling.
USO IN POPOLAZIONI SPECIFICHE
Gravidanza
Categoria di gravidanza B
Non ci sono studi adeguati e ben controllati in donne incinte. Poiché gli studi sulla riproduzione animale non sono sempre predittivi della risposta umana, questo farmaco dovrebbe essere usato durante la gravidanza solo se chiaramente necessario.
Sono stati eseguiti studi di riproduzione su topi e ratti utilizzando dosi orali di cefalexina monoidrato 0.6 e 1,5 volte la dose massima giornaliera per l’uomo (66 mg/kg/giorno) sulla base della superficie corporea, e non hanno rivelato alcuna prova di compromissione della fertilità o danno al feto.
Madri che allattano
Cefalexina viene escreta nel latte umano. Cautela deve essere esercitata quando la cefalexina viene somministrata ad una donna che allatta.
Uso pediatrico
La sicurezza e l’efficacia della cefalexina in pazienti pediatrici è stata stabilita in studi clinici per i dosaggi descritti nella sezione dosaggio e somministrazione.
Uso geriatrico
Dei 701 soggetti in 3 studi clinici pubblicati sulla cefalexina, 433 (62%) avevano 65 anni e oltre. Non sono state osservate differenze generali nella sicurezza o nell’efficacia tra questi soggetti e quelli più giovani, e altre esperienze cliniche riportate non hanno identificato differenze nelle risposte tra gli anziani e i pazienti più giovani.
Questo farmaco è sostanzialmente escreto dai reni, e il rischio di reazioni tossiche a questo farmaco può essere maggiore nei pazienti con funzione renale compromessa. Poiché i pazienti anziani hanno più probabilità di avere funzione renale diminuita, la cura deve essere presa nella selezione della dose.
Depressione renale
Cefalexina deve essere somministrata con cautela in presenza di compromissione della funzione renale (clearance della creatinina < 30 mL/min, con o senza dialisi). In tali condizioni, un’attenta osservazione clinica e studi di laboratorio di monitoraggio della funzione renale devono essere condotti perché il dosaggio sicuro può essere inferiore a quello solitamente raccomandato.
sovradosaggio
Sintomi di sovradosaggio orale possono includere nausea, vomito, distress epigastrico, diarrea ed ematuria. In caso di sovradosaggio, istituire misure generali di supporto.
Diuresi forzata, dialisi peritoneale, emodialisi, o emoperfusione con carbone vegetale non sono stati stabiliti come benefici per un sovradosaggio di cefalexina.
Descrizione della sospensione di cefalexina
Cefalexina sospensione orale, USP è un farmaco antibatterico semisintetico cefalosporina destinato alla somministrazione orale. È 7-(D-α- Amino-α-phenylacetamido)-3-methyl-3-cephem-4-carboxylic acid monohydrate. Cephalexin ha la formula molecolare C16H17N3O4S-H2O e il peso molecolare è 365.41.
Cephalexin ha la seguente formula strutturale:
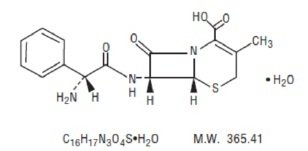
Inactive Ingredients: Diossido di silicio colloidale, FD&C Red # 40, metilcellulosa (15 premium LV), metilcellulosa (4AC premium), sodio benzoato, aroma di fragola, saccarosio, gomma xantano.
Cefalexina sospensione – Farmacologia clinica
Meccanismo d’azione
Cefalexina è un farmaco antibatterico a base di cefalosporina.
Farmacocinetica
Assorbimento:
Cefalexina è stabile agli acidi e può essere somministrata indipendentemente dai pasti. In seguito a dosi di 250 mg, 500 mg e 1 g, i livelli sierici medi di picco di circa 9, 18 e 32 mcg/mL, rispettivamente, sono stati ottenuti a 1 ora. I livelli sierici erano rilevabili 6 ore dopo la somministrazione (ad un livello di rilevazione di 0,2 mcg/mL).
Distribuzione:
Cefalexina è approssimativamente dal 10% al 15% legata alle proteine plasmatiche.
Escrezione:
Cefalexina viene escreta nelle urine per filtrazione glomerulare e secrezione tubulare. Gli studi hanno dimostrato che oltre il 90% del farmaco viene escreto invariato nelle urine entro 8 ore. Durante questo periodo, le concentrazioni di picco nelle urine dopo le dosi di 250 mg, 500 mg e 1 g erano approssimativamente 1.000, 2.200 e 5.000 mcg/mL rispettivamente.
Interazioni farmacologiche:
In soggetti sani a cui sono state somministrate singole dosi da 500 mg di cefalexina e metformina, la Cmax e l’AUC medie della metformina sono aumentate in media del 34% e 24%, rispettivamente, e la clearance renale media della metformina è diminuita del 14%. Non sono disponibili informazioni sull’interazione di cefalexina e metformina in seguito a dosi multiple di entrambi i farmaci.
Microbiologia
Meccanismo d’azione
Cefalexina è un agente battericida che agisce tramite l’inibizione della sintesi della parete cellulare batterica.
Resistenza
Gli stafilococchi resistenti alla meticillina e la maggior parte degli enterococchi sono resistenti alla cefalexina. La cefalexina non è attiva contro la maggior parte degli isolati di Enterobacter spp, Morganella morganii e Proteus vulgaris. La cefalexina non ha attività contro Pseudomonas spp. o Acinetobacter calcoaceticus. Streptococcus pneumoniae resistente alla penicillina è di solito resistente incrociato ai farmaci antibatterici beta-lattamici.
Attività antimicrobica
Cefalexina ha dimostrato di essere attiva contro la maggior parte degli isolati dei seguenti batteri sia in vitro che in infezioni cliniche.
Batteri Gram-positivi
Staphylococcus aureus (solo isolati sensibili alla meticillina) Streptococcus pneumoniae (isolati sensibili alla penicillina) Streptococcus pyogenes
Batteri Gram-Escherichia coli Haemophilus influenzae Klebsiella pneumoniae Moraxella catarrhalis Proteus mirabilis
SusceptibilityTesting
Per informazioni specifiche sui criteri interpretativi dei test di suscettibilità e sui metodi di test associati e sugli standard di controllo della qualità riconosciuti dalla FDA per questo farmaco, si prega di vedere: https://www.fda.gov/STIC.
Nonclinical Toxicology
Carcinogenesis & Mutagenesis & Impairment Of Fertility
Lifetime studies in animals have not been performed to evaluate the carcinogenic potential of cephalexin. Tests to determine the mutagenic potential of cephalexin have not been performed. In male and female rats, fertility and reproductive performance were not affected by cephalexin oral doses up to 1.5 times the highest recommended human dose based upon body surface area.
How Supplied/Storage and Handling
Cephalexin for oral suspension* USP (a strawberry flavored formula) is supplied as follows:
125 mg/5 mL:
Bottles of 100 mL (NDC 67877-544-88)
Bottles of 200 mL (NDC 67877-544-68)
250 mg/5 mL:
Bottles of 100 mL (NDC 67877-545-88)
Bottles of 200 mL (NDC 67877-545-68)
Directions for mixing are included on the label.
Conservare a 20o – 25o C (68o – 77o F). Tenere ben chiuso.
*Dopo la miscelazione, conservare in frigorifero. Può essere conservato per 14 giorni senza perdita significativa di potenza.
Informazioni per il paziente
- Avvisare i pazienti che potrebbero verificarsi reazioni allergiche, incluse reazioni allergiche gravi, e che reazioni gravi richiedono un trattamento immediato. Chiedere al paziente circa eventuali precedenti reazioni di ipersensibilità alla cefalexina, altri beta-lattamici (tra cui cefalosporine) o altri allergeni (5.1)
- Avvisare i pazienti che la diarrea è un problema comune causato da farmaci antibatterici e di solito si risolve quando il farmaco viene interrotto. A volte, può verificarsi frequente diarrea acquosa o sanguinolenta e può essere un segno di una più grave infezione intestinale. Se si sviluppa una grave diarrea acquosa o sanguinolenta, consigliare i pazienti di contattare il loro fornitore di assistenza sanitaria.
- Consigliare i pazienti che i farmaci antibatterici tra cui cefalexina, deve essere utilizzato solo per trattare le infezioni batteriche. Non trattano le infezioni virali (ad esempio, il comune raffreddore). Quando la cefalexina è prescritta per trattare un’infezione batterica, dite ai pazienti che anche se è comune sentirsi meglio all’inizio del corso della terapia, il farmaco deve essere preso esattamente come indicato. Saltare le dosi o non completare il corso completo della terapia può (1) diminuire l’efficacia del trattamento immediato e (2) aumentare la probabilità che i batteri sviluppino resistenza e non saranno trattabili da cefalexina o altri farmaci antibatterici in futuro.
Prodotto in India da:
Alkem Laboratories Ltd.,
Mumbai – 400013, INDIA.
Distribuito da:
Ascend Laboratories, LLC
Parsippany, NJ 07054
Revisionato: Dicembre, 2018
PT 2851
ETICHETTA DELLA CONFEZIONE.SCHEDA PRINCIPALE
NDC 67877-544-88
Cefalexina per sospensione orale, USP 125 mg per 5 mL
quando ricostituita secondo le istruzioni.
Dose pediatrica abituale: 25-50 mg per kg al giorno in quattro dosi divise. Per infezioni più gravi, la dose può essere raddoppiata. Vedere letteratura di accompagnamento.
Rx only
For Oral Use only
100 mL (when mixed)
Ascend Laboratories, LLC

NDC 67877-545-88
Cephalexin for Oral Suspension, USP 250 mg per 5 mL
when reconstituted according to directions.
Dose pediatrica abituale: 25-50 mg per kg al giorno in quattro dosi divise. Per infezioni più gravi, la dose può essere raddoppiata.
Rx only
For Oral Use only
100 mL (when mixed)
Ascend Laboratories, LLC

| CEPHALEXIN cefalexina per sospensione |
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
| CEPHALEXIN cephalexin for suspension |
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
Labeler – Ascend Laboratories, LLC (141250469)
| Establishment | |||
| Name | Address | ID/FEI | Operations |
| Alkem Laboratories Limited | 915628612 | MANUFACTURE(67877-544, 67877-545) | |
Frequently asked questions
- What are the best antibiotics for a tooth infection?
- Cephalexin – can this be used to treat an abscess in the mouth or gum infection?
- If people are allergic to amoxicillin can they take cephalexin?
- What is the best antibiotic to treat strep throat?
- Can you take cephalexin for a spider bite?
- Can you take antibiotics while pregnant?
- Cephalexin – is this a drug that can be abused by teens?
More about cephalexin
- Side Effects
- During Pregnancy or Breastfeeding
- Dosage Information
- Patient Tips
- Drug Images
- Drug Interactions
- Compare Alternatives
- Support Group
- Pricing & Coupons
- En Español
- 415 Reviews
- Drug class: first generation cephalosporins
Consumer resources
- Patient Information
- Cephalexin (Advanced Reading)
Professional resources
- Prescribing Information
- Cephalexin (Professional Patient Advice)
- Cephalexin (FDA)
- Cephalexin Tablets (FDA)
Other brands Keflex, Daxbia, Panixine
Related treatment guides
- Bacterial Infection
- Bladder Infection
- Bacterial Endocarditis Prevention
- Acne
- … +7 more
Medical Disclaimer