As we search for Periodic Table or P Table but we didn’t get the complete information regards periodic table but don’t need to be a worry here you get complete information regarding periodic table and in PDF file which you can easily save on your device and then use it. What we have done by our end that we have to make the list with some important links so by which you get all the information.
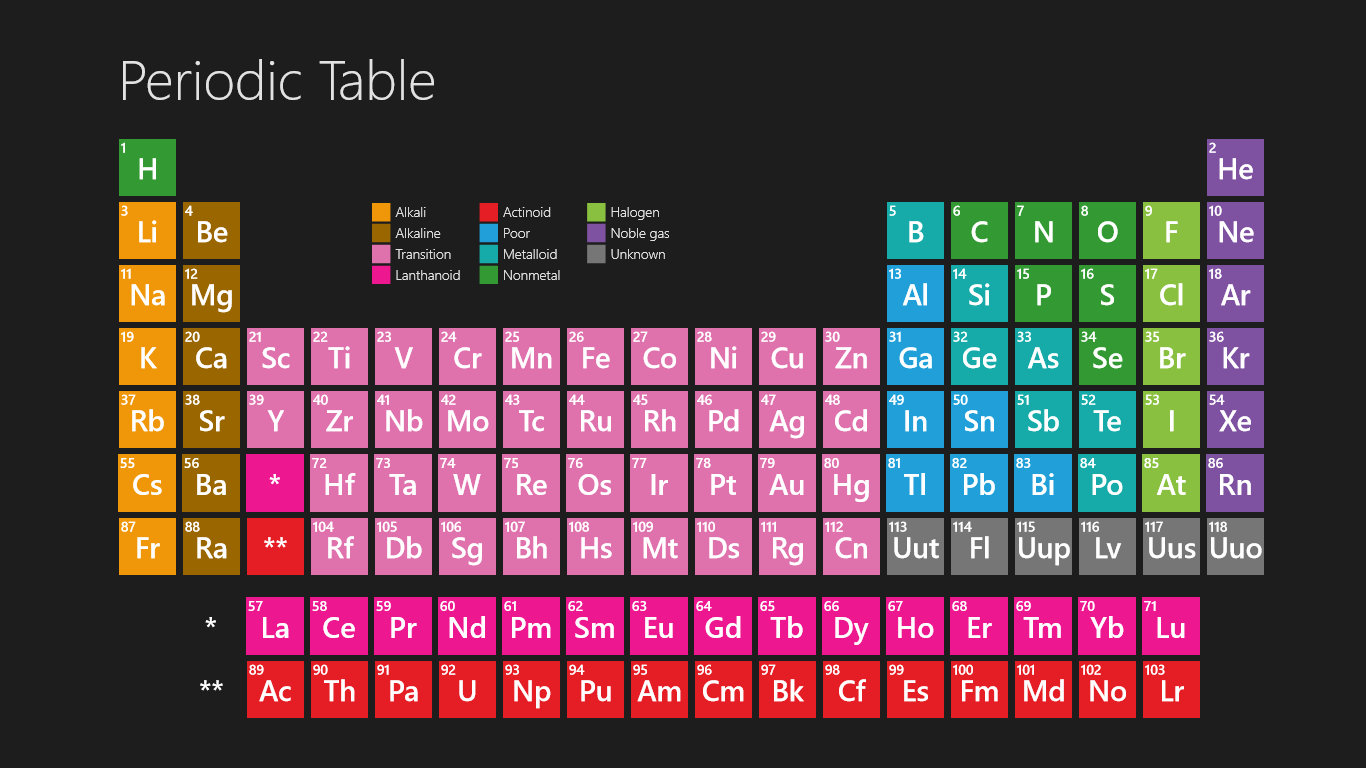

The HD periodic table for kids helps you a lot get clear information and which you can see on your device also. You can use it and fit it on your sheet also, and don’t need to take tension regarding if the paper is lost then what, so friends don’t worry about that because you can also take print as much as you can of this periodic table for your own personal use where you take it for homework problems or performing lab calculations.
- Hydrogen Valence Electrons
- Helium Valence Electrons
- Lithium Valence Electrons
- Beryllium Valence Electrons
- Boron Valence Electrons
- Carbon Valence Electrons
- Nitrogen Valence Electrons
- Oxygen Valence Electrons
- Fluorine Valence Electrons
- Neon Valence Electrons
- Sodium Valence Electrons
- Magnesium Valence Electrons
- Aluminum Valence Electrons
- Silicon Valence Electrons
- Phosphorus Valence Electrons
- Sulfur Valence Electrons
- Chlorine Valence Electrons
- Argon Valence Electrons
- Potassium Valence Electrons
- Calcium Valence Electrons
- Scandium Valence Electrons
- Titanium Valence Electrons
- Vanadium Valence Electrons
- Chromium Valence Electrons
- Manganese Valence Electrons
- Iron Valence Electrons
- Cobalt Valence Electrons
- Nickel Valence Electrons
- Copper Valence Electrons
- Zinc Valence Electrons
- Gallium Valence Electrons
- Germanium Valence Electrons
- Arsenic Valence Electrons
- Selenium Valence Electrons
- Bromine Valence Electrons
- Krypton Valence Electrons
- Rubidium Valence Electrons
- Strontium Valence Electrons
- YttriumValence Electrons
- Zirconium Valence Electrons
- Niobium Valence Electrons
- Molybdenum Valence Electrons
- Technetium Valence Electrons
- Ruthenium Valence Electrons
- Rhodium Valence Electrons
- Palladium Valence Electrons
- Free Printable Periodic Table
- Tablica okresowa z ładunkami
- Tablica okresowa z ładunkami atomowymi
- Tablica okresowa pierwiastków z nazwami
- Dynamiczny układ okresowy
- Pusty układ okresowy
- Periodic Table of Elements Printable
- Wartości IUPAC
- Printable Table Trends
- Wykres trendów tablicy okresowej
- Tablica Okresowa 2021
- Tapeta z układem okresowym
- Printable Periodic Table With Atomic Mass
- Periodic Table With Electronegativity
- Czarno-biały Układ Okresowy
- Interaktywny układ okresowy
- Interaktywny układ okresowy dla dzieci
- Darmowy Układ Okresowy PDF
- Tablica okresowa z masą
- Orbitale układu okresowego
- Orbitale S, P, D, F Układ Okresowy
Free Printable Periodic Table
As we all know there are 118 elements in the periodic table and this periodic table cites the keeping with most IUPAC values and by this, you can use it for your calculation and homework.
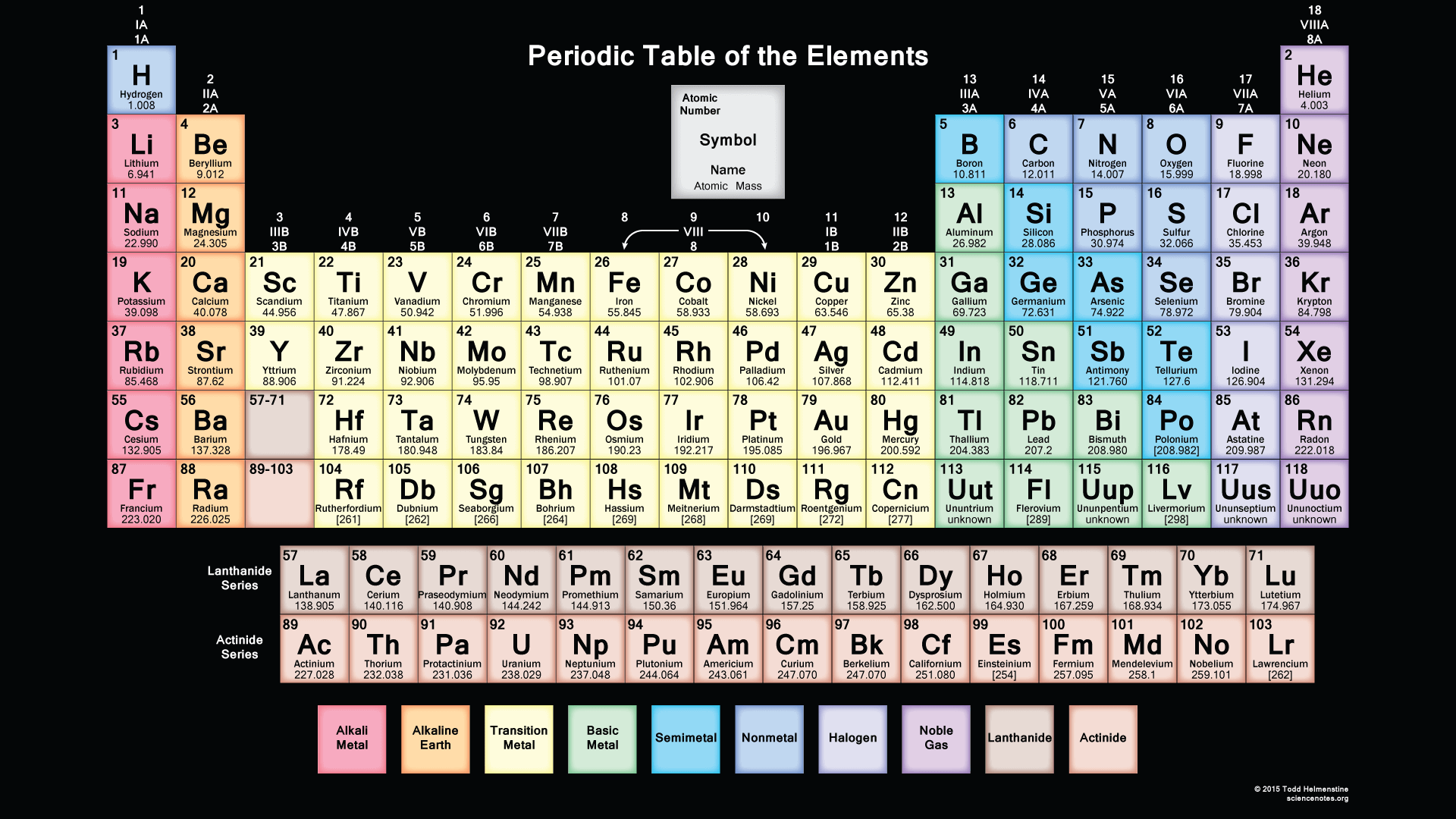

You can also print any interactive periodic table by your end which helps you to know more about this, there are some elements which are fundamentally different from the conventional periodic table and which is defined by charge positive or negative and valence statements were taken by these elements and these are the few things which make the periodic table much more effective.
Do tego istnieje również wiele książek na temat układu okresowego i każda książka dostarcza tych samych informacji na różne sposoby i nie możemy tego zaniedbać, ponieważ z każdej książki uczymy się czegoś nowego.
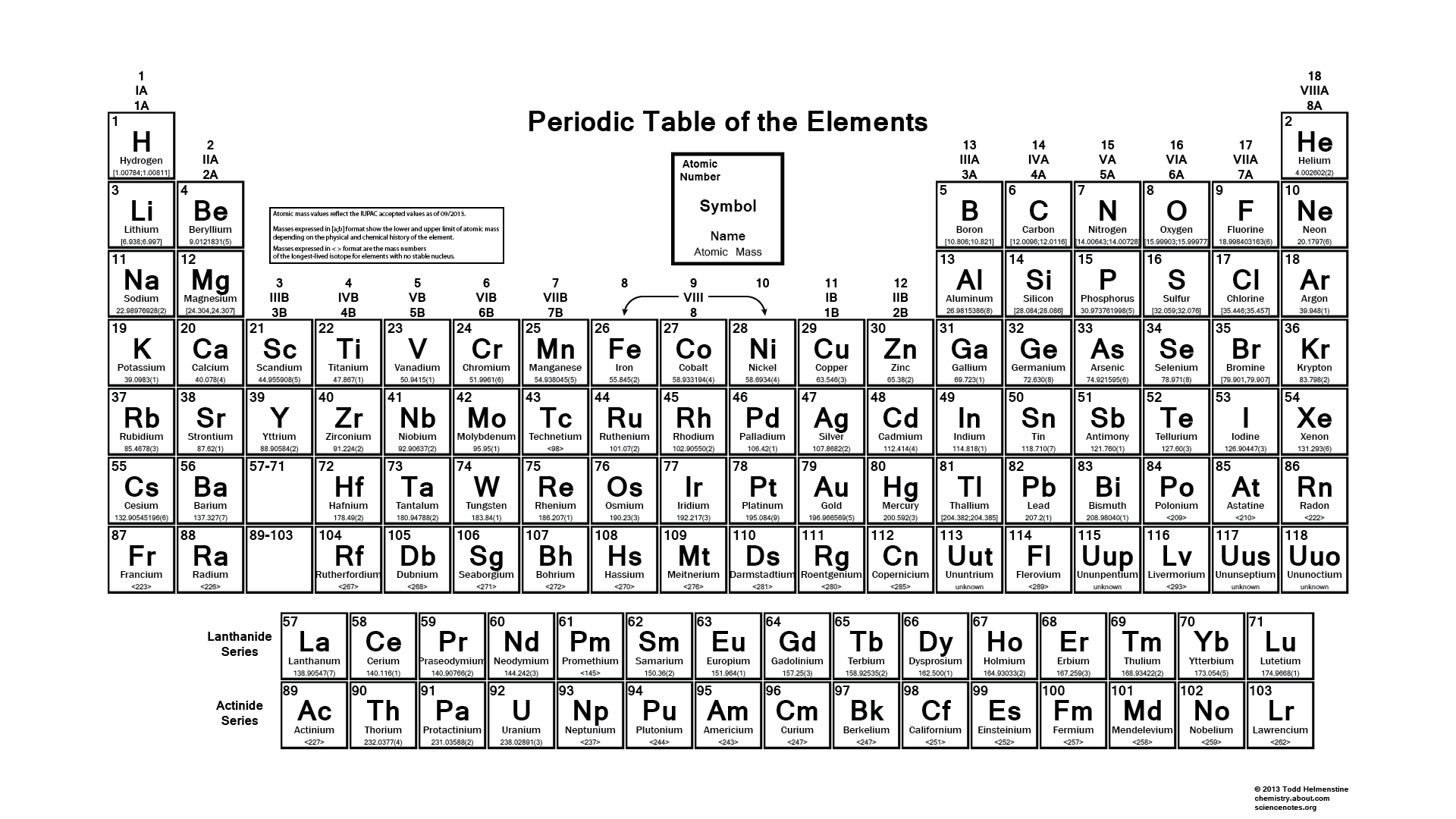

Widzimy również podstawową tabelę, którą uczniowie mogą również wypełnić na końcu, a którą nazywamy pustym układem okresowym. Uczeń może wypełnić i ten układ okresowy pomaga mu w lepszej nauce.
Tablica okresowa z ładunkami
Jak wszyscy wiemy, wartość układu okresowego jest tworzona przez ładunki dla atomów pierwiastków chemicznych. Możesz również użyć tego układu okresowego, aby dowiedzieć się więcej o ładunkach pierwiastków, a także o tym, jak pierwiastki tworzą wiązania z innymi pierwiastkami. Jak wszyscy wiemy ładunki atomu opiera się na elektron walencyjny lub stan utleniania. Atom pierwiastków jest stabilny, gdy jego najbardziej zewnętrzna komórka jest całkowicie wypełniona elektronami zewnętrznymi lub wypełniona w połowie. A te, które mają więcej elektronów są uważane za stabilne atomy.
W układzie okresowym, wodór jest na szczycie i składa się z 1 protonu i 1 niesparowanego elektronu, który uważamy za wolny rodnik, a ten niesparowany elektron z niecierpliwością czeka na utworzenie pary z innymi elektronami.
Tablica okresowa z ładunkami atomowymi
Gdy słyszymy słowo proton łatwo zakładamy, że oznacza ono pozytywny i oznacza również pozytywny jon wodoru znany jest jako proton. Proton jest formą wodoru, która produkuje enzym ATP.
Wodorowodór jest wodorem, który ma dodatkowy elektron, więc przyjmuje ujemny ładunek jonu lub anionu, tj. przyjmuje znak minus i tworzy zwykły atom wodoru.
Wodor cząsteczkowy jest formą, w której gdy dwa atomy wodoru tworzą wiązania razem i cząsteczki wodoru. H2 jest również wodór molekularny. I składa się z dwóch protonów i dwóch elektronów, i jest to najbardziej powszechna forma wodoru, ponieważ jest stabilny z neutralnymi ładunkami, i jest również przeciwutleniaczem w wodzie bogatej w wodór, i wodór cząsteczkowy jest najmniejszą cząsteczką wszechświata, czyli tam, gdzie nikt nie może iść, ta cząsteczka może łatwo iść.
Tutaj możesz również pobrać tablicę okresową z ładunkami pierwiastków.
Tablica okresowa pierwiastków z nazwami
Teraz podaję ci wszystkie pierwiastki tablicy okresowej z nazwami z rosnącą formą liczby atomowej. Jak wiadomo każdy pierwiastek ma jedno lub dwuliterowy symbol, który jest jakby formą obecnych i starych nazw. Numer pierwiastka to jego liczba atomowa, która jest liczbą protonów w atomach.
1 – A – wodór
2 – He – hel
3 – Li – lit
4 – Be – beryl
5 – B – bor
6 – C – węgiel
7 – N – azot
8 o – Oxygen
9 – F – Fluorine
10 – Do – Neon
11 – Na – Sodium
12 – Mg – Magnesium
13 – Al – aluminium
14 – Si – Silicon
15 – P – ang. fosfor
16 – S – siarka
17 – Cl – chlor
18 – Ar – argon
19 – K – potas
20 – Ca – wapń
21 – SC – technet
22 – Ti – Titanium
23 – 5 – Vanadium
24 – Cr – chrom
25 – MN – mangan
26 – Fe – Iron
27 – Co – Cobalt
28 – Ni – nickel
29 – Cu – Copper
30 – Zn – Zn – Cynk
31 – GA – Gal
32 – Ge – German
33 – As – Arsen
34 – Se – Selen
35 – br – Arsen
36 – K – Krypton
37 – RB – Rubid Rubid
38 – Sr – Stront
39 – Y – Itr
40 – Zr – Cyrkon
41 – Nb – Bizmut
42 – Mo – Molibden
43 – TC – Technet
44 – RU – ruten
45 – Rh – Rodos
46 – Pd – pallad
47 – Ag – srebro
48 – Cd – kadm
49 – IN – Indie
50 – Sn – cyna
51 – Sb – antymon
52 – Te – Tellurium
53 – 1 – Iodine
54 – Xe – Xenon
55 – CS – caesium
56 – Ba – Barium
57 – La – lanthanum
58 – Ce – cerium
59 – Co- Cobalt
60 – Nd – neodymium
61 – PM – promethium
62 – Sm – samarium
63- Eu – Europium
64 – Gd – gadolinium
65 – Tb – terbium
66 – Dy – dysprosium
67 – Ho – holmium
68 – Er – erbium
69 – Tm – thulium
70 – Yb – ytterbium
71 – Lu – lutetium
72 – Hf – Hafnium
73 – Ta – Osmium
74 – W – Tungsten
75 – Re – rhenium
76 – OS – osmium
77 – Ir – Iridium
78 – Pt – Platinum
79 – Au – Gold
80 – HG – Mercury
81 – Tl – Thallium
82 – Pb – Lead
83 – Bi – bismuth
84 – Po – Bismuth
85 – but – astatine
86 – R – radon
87 – FR – France
88 – Ra – Radium
90 – Th – Thorium
91 – PA – Protactinium
92 – U – uranium to
93 – NP – Neptune
94 – pu – Pluton
95 – Am – America
96 – Cm – Americium
97 – Bk – Berkelium
98 – CF – Kaliforniyum
99 – are – Einstein
100 – FM – Barium
101 – MD – Mendélévium
102 – No – Nobelium
103 – Lt. – Lawrence’a
104 – R – rutherfordium
105 – DB – Dubnium
106 – SG – Dubnium
107 – Hs – Bohrium
108 – Hs – Hass
109 – Mt – Meitnerium
110 – D – Darmstadtium
111 – RG – rubidium
112 – Cn – Copernicus
113 – NH – ang. Nihon
114 – Fl – Flerow
115 – Mc – Moskwa
116 – LV – Livermorium
117 – TS – Tennessee
118 – og – Oganesson
/div>
iv id=2,5
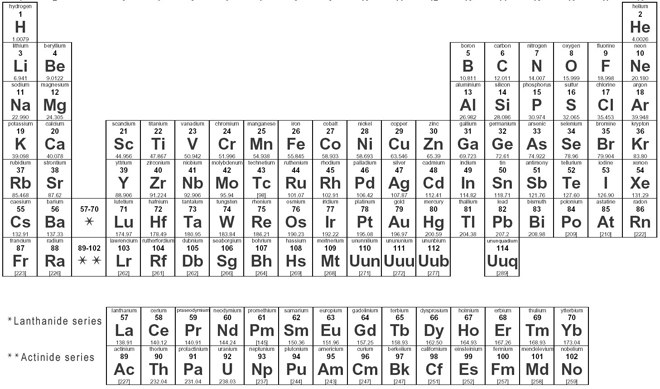

Dynamiczny układ okresowy
Przez dynamiczny układ okresowy, można uzyskać wszystkie informacje na temat układu okresowego i tutaj można łatwo pokryć wszystkie informacje dotyczące każdego elementu, w tym wszystko, jak elektrony, protony, neutrony, elektrony na najbardziej zewnętrznych orbitach i temperatury itp. i tutaj możesz zwizualizować dane układu okresowego, i tutaj możesz łatwo dowiedzieć się o każdym elemencie, który ma miejsce w układzie okresowym i muszę zasugerować, abyś go przejrzał, ponieważ tutaj mówię ci o wszystkich atomach, który z nich jest dodatni, który jest ujemny, a który jest neutralny, przez niektóre obrazy dostajesz wszystkie informacje, dynamiczny układ okresowy oznacza, że dostajesz wszystkie informacje przez obrazy i jest to tabelaryczny układ pierwiastków chemicznych, który jest uporządkowany według ich liczby atomowej.
Wszystkie pierwiastki od wodoru do oganesonu zostały odkryte lub zsyntetyzowane. Pierwsze 94 pierwiastki są pierwiastkami naturalnymi, a reszta pierwiastków jest badana w laboratoriach lub reaktorach jądrowych.
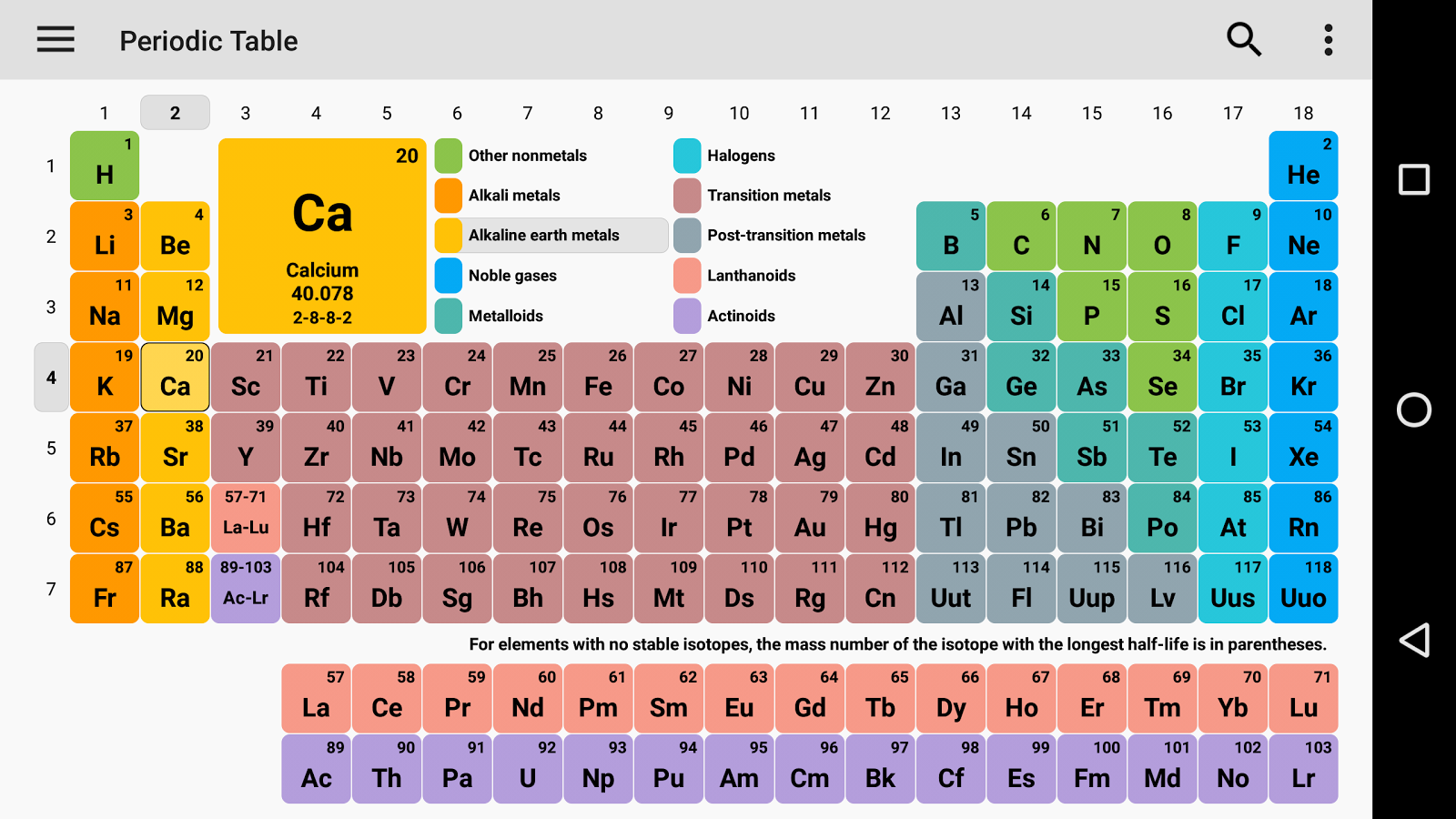

W układzie okresowym zaszły również pewne zmiany i nowe 4 pierwiastki to Nihonium, Moscovium, Tennessee i Oganesson. Jest to potwierdzone przez (IUPAC) 30 grudnia 2015 roku, a oficjalnie nazwane 28 listopada 2016 roku. A liczba atomowa niedawno dodane 113,115,117 i 118. I ta metoda stara się objąć wszystkie metody od szkoły do eksperta w branży. W ten sposób mogę spróbować powiedzieć wszystkim o układzie okresowym.
Pusty układ okresowy
W porównaniu z innym układem okresowym, pusty układ okresowy jest najlepszy, ponieważ jeśli widzę w nim, że wypełniamy układ okresowy na końcu i do nauki można go użyć, jeśli wiesz wszystko o układzie okresowym, a następnie wypełnić wszystkie kolumny i łatwo sprawdzić swoją wiedzę, można również użyć go do praktyki układu okresowego, a także użyć go w swoim podręczniku.
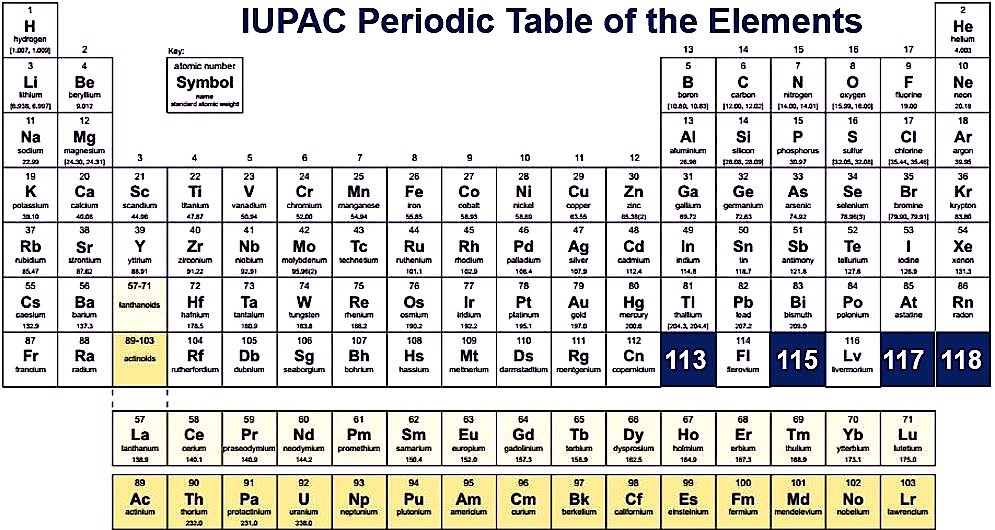

W tym celu musisz po prostu pobrać układ okresowy PDF na urządzenie i możesz również użyć wydruku na kartce A4. I w tej pustej kolumnie, można wypełnić wszystkie liczby atomowe, okresy i grupy, jeśli jest to pożądane. Można również wypełnić opcjonalny kolor w innej kolumnie jak metale alkaliczne, metale trans, lantanowce, aktynowce, metaloidy, chlorowce i gazy szlachetne. A najlepsze jest to, że jeśli popełnisz jakiś błąd to możesz łatwo poprawić ten błąd, ponieważ masz również szansę to zrobić i jak już mówiłem możesz również wziąć aż tyle stron pustego drukowanego układu okresowego, dzięki temu uczeń może również przygotować się do testu, a także sprawdzić swoją wiedzę.
You Can Download Here Blank Periodic Table Chart
Periodic Table of Elements Printable
W tym możesz łatwo znaleźć idealną tabelę do wydrukowania dla swoich potrzeb, tutaj możesz dostać całą kompletną kolekcję darmowych tablic okresowych do wydrukowania w formacie PDF lub PNG aby zapisać, wydrukować i używać. Staramy się umieścić kompletne informacje o układzie okresowym, a także umieścić wszystkie obrazy w jakości HD, które można wykorzystać jako wygaszacz ekranu na swoich urządzeniach.
Możesz go dopasować do swojego urządzenia, i możesz go łatwo odpalić na swoim urządzeniu, i kiedy weźmiesz druk w tym czasie również możesz go dopasować do kartki papieru, i biorąc druk możesz go również użyć do użytku osobistego, jak możesz wziąć tę stronę do obliczeń laboratoryjnych, ta tabela zmieniła rozmiar, więc możesz przeglądać lub drukować w dowolnym rozmiarze od małego do dużego rozmiaru plakatu zgodnie z twoim wyborem. W tym, można łatwo uzyskać wszystkie 118 elementów w rzeczywistości i liczby. W tej drukowanej tabeli okresowej masy atomowe i znaczące liczby i utrzymanie, że z najnowszymi wartościami IUPAC.
Wartości IUPAC
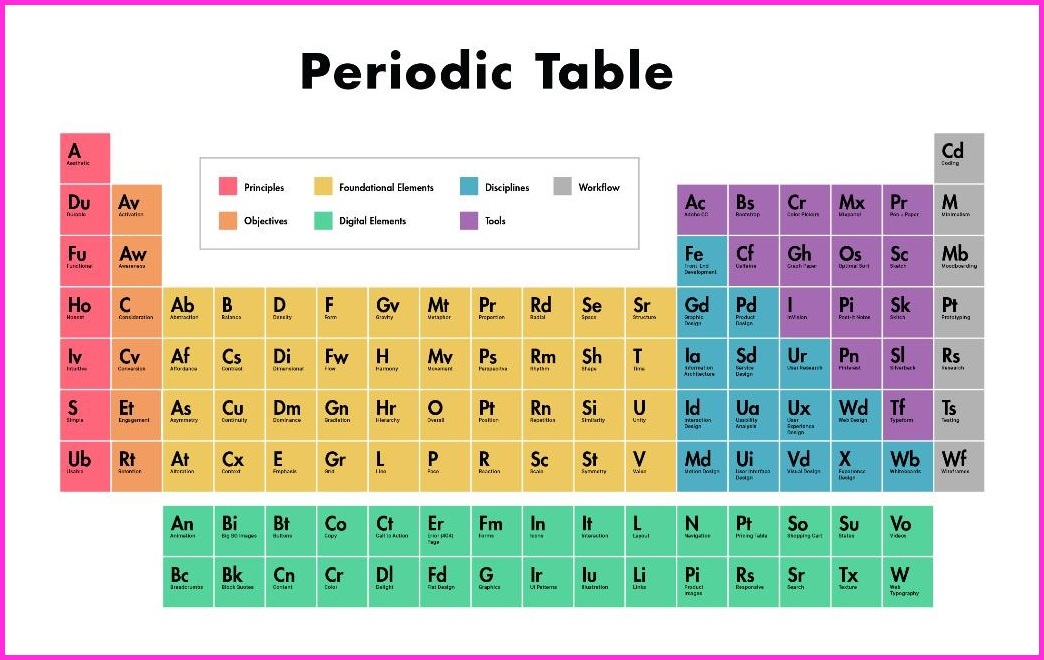

Jak już mówiłem, możesz użyć go do osobistego testu i w ten sposób, możesz łatwo sprawdzić swoją wiedzę i w tym nie ma żadnych granic, możesz wydrukować tyle ile możesz, a najlepsze jest to, że jest tam wiele obrazów, które są w HD i to również możesz zrobić tapetę na swoim urządzeniu jak telefon komórkowy, laptop, tab i wiele innych rzeczy i dzięki temu zawsze pamiętasz o tych rzeczach.
Dla zapamiętania tych rzeczy możesz również czytać książki tak bardzo jak możesz, ponieważ dzięki temu wiesz tylko o liczbie atomowej, masie atomowej i wielu innych rzeczach, ale po przeczytaniu książek możesz również wiedzieć o tym jak możesz wykorzystać tę praktykę, ponieważ jak wszyscy wiemy nauka zależy tylko od dowodu, nigdy nie zależy od innych rzeczy, więc moja sugestia jest bardzo prosta umieść tyle wysiłku ile możesz, dzięki czemu możesz poprawić swoją naukę, a także uzyskać wynik dotyczący twojej nauki.
Jeśli możesz szukać więcej szczegółów Idź tutaj: Periodic Table of Elements
Printable Table Trends
Możesz użyć tego wykresu, aby zobaczyć piękno układu okresowego z tendencjami elektronegatywności, energii jonizacji, promienia atomowego, charakteru metalicznego i powinowactwa elektronowego. Te elementy są strukturalnie jodły na periodic table.If mówię o elektronegativity to pokazuje, jak łatwo chemiczne tworzą wiązania chemiczne, i jak widzimy, że jest wzrost od lewej do prawej i spadek od prawej do lewej w grupie. Zauważyliśmy, że gazy szlachetne (ta kolumna, która jest po prawej stronie) są stosunkowo obojętne, więc elektronegativity zbliża się do zera (nie możemy wziąć tego ogólnego trendu).
Każdy atom ma dużą różnicę między wartościami elektronegativity, więcej atomów jest do utworzenia wiązania, które jest znane jako wiązanie chemiczne.
Wykres trendów tablicy okresowej
Tutaj możesz przejść przez Trendy Tablicy Okresowej
Energia jonizacji jest uważana za najmniejszą ilość energii i musi pomóc elektronowi oddalić się od atomu w formie gazowej. To zwiększa energię jonizacji i kiedy poruszać się od lewej do prawej, ponieważ zwiększa liczbę protonów mocniej i to jest naprawdę trudne do usunięcia, że.
Jądrowe zamiatanie jest oddzielenie od rdzenia do obwodowego stabilnego elektronu, podczas gdy zakres jonowy jest duża część separacji między dwoma rdzeni jądrowych, które są po prostu dotykając siebie. Ten powiązany esteem pokazać podobny wzór w tabeli okazjonalnej.
Tablica Okresowa 2021
Jak poruszasz się w dół tabeli okazjonalnej, składniki mają więcej protonów i podnoszą powłokę witalności elektronów, więc iotas wind up noticeably bigger. Jak poruszać się nad kolumną tabeli przerywanej, jest trochę więcej protonów i elektronów w nim, ale elektrony są trzymane bardziej intently do rdzenia, więc ogólny rozmiar iota zmniejsza.
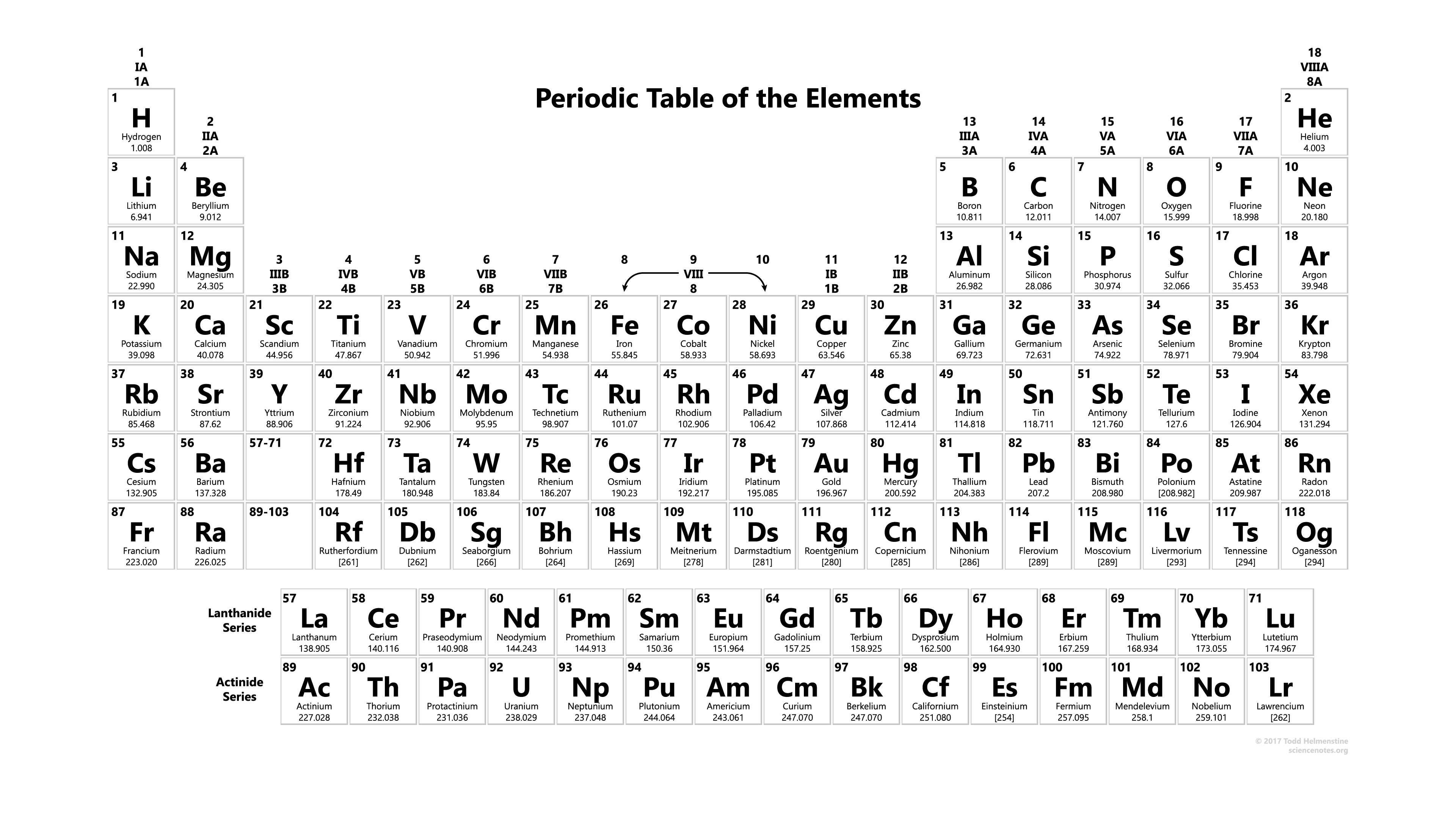

Wiele elementów w układzie okresowym są metalami, oznacza to, że wykazują metaliczny charakter. Wszystkie właściwości metali, takie jak metaliczny połysk, wysoka przewodność elektryczna i cieplna, ciągliwość, kowalność i kilka innych cech. Prawa strona układu okresowego zawiera niemetale, które nie wykazują wszystkich tych właściwości. Podobnie jak w przypadku wielu innych właściwości, charakter metaliczny, który odnosi się do konfiguracji elektronów walencyjnych.
Zdecydowana większość składników w tablicy przerywanej to metale, co oznacza, że wykazują one charakter metaliczny. Właściwości metali obejmują metaliczny blask, wysoką przewodność elektryczną i cieplną, giętkość, elastyczność i kilka różnych cech. Po prawej stronie tabeli okazjonalnej znajdują się niemetale, które nie wykazują tych właściwości. Podobnie z właściwościami alternatywnymi, charakter metaliczny utożsamia się z rozmieszczeniem elektronów walencyjnych.
Tapeta z układem okresowym
Tutaj masz wiele tapet do wydrukowania, w których uzyskasz kompletne informacje o układzie okresowym, które uzyskasz w inny sposób, w tym również wiesz o nazwie pierwiastka, rodzinie pierwiastków, liczbie atomowej, masie atomowej, symbolu pierwiastka, grupie i masie atomowej. W tym obrazie, widzisz wszystkie informacje i wydaje się bardzo lekki obraz więc nie napotkasz żadnego rodzaju problemu, aby go zobaczyć, a także zmienia rozmiar czysto dla innych rozdzielczości. This wallpaper of periodic table fresh update of original chart featured on this site.
There you also get some transparent wallpaper in HD quality, by this you don’t need to face any kind of problem; easily you see images without any pressure or effect on eyes, And this image also you can download and make it your wallpaper. I to naprawdę pomaga zrobić swoje notatki i projekty.
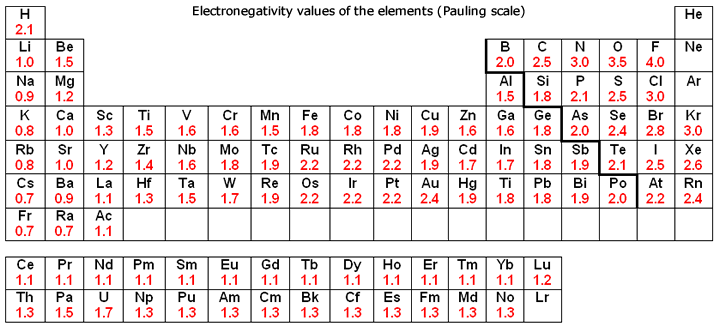

I w obrazach, można również zobaczyć wiele jakości jak czarno-biały kolor, wielobarwny układ okresowy, układ okresowy ze wszystkimi elementami, koło płytki układ okresowy i wiele więcej rodzajów obrazów.
Printable Periodic Table With Atomic Mass
W tym, dostajesz kompletną informację o masie atomowej wszystkich pierwiastków, którą używasz kiedy robisz badania lub kiedy robisz jakieś eksperymenty w laboratorium, i możesz także użyć tego lub możesz także wziąć wydruk do użycia. Otrzymasz również informacje o masach atomowych pierwiastków i w tym, również znasz dalsze informacje o właściwościach chemicznych, dane środowiskowe lub skutki zdrowotne, a ta lista zawiera około 118 elementów chemii i przez to, wiesz o masie atomowej każdego elementu.
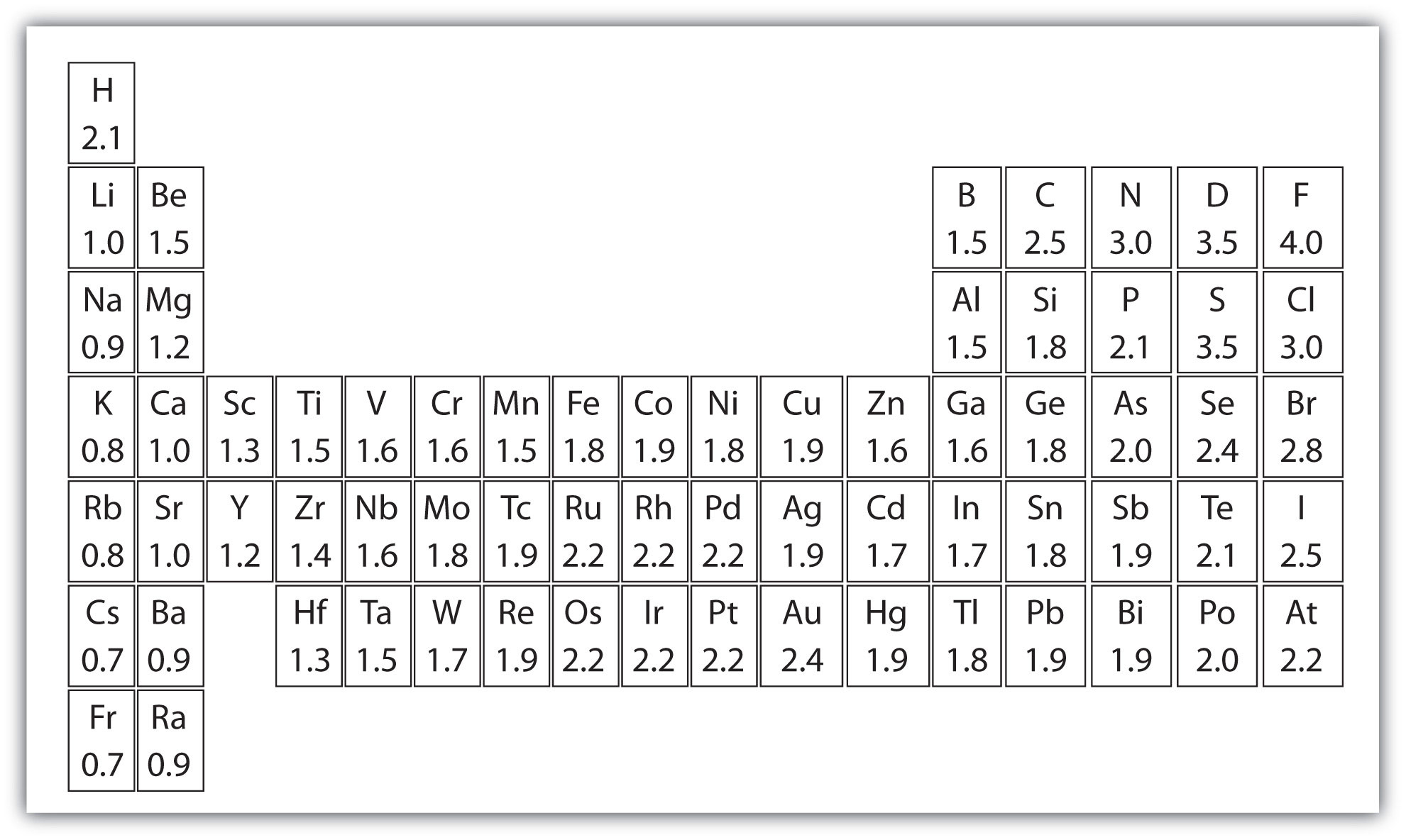

Download From Here: Periodic Table With Atomic Mass
Periodic Table With Electronegativity
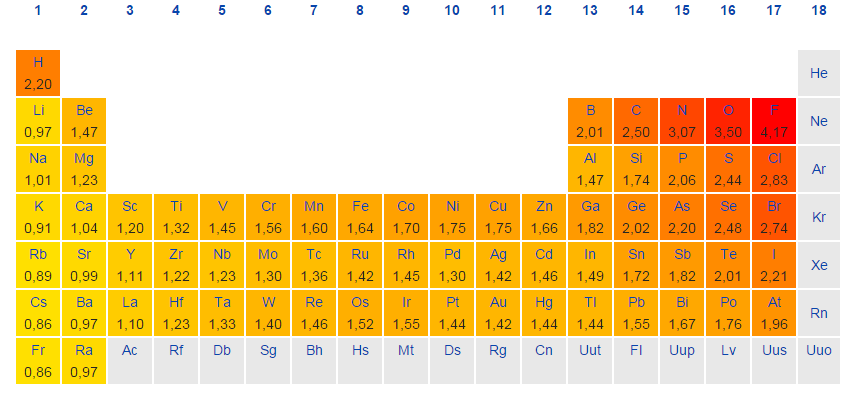

Elektronegatywność odnosi się do zdolności ioty do przyciągania współdzielonych elektronów w wiązaniu kowalencyjnym. Im wyższa szacunkowa ocena elektronegatywności, tym bardziej jednoznacznie dany składnik wciąga wzajemne elektrony.
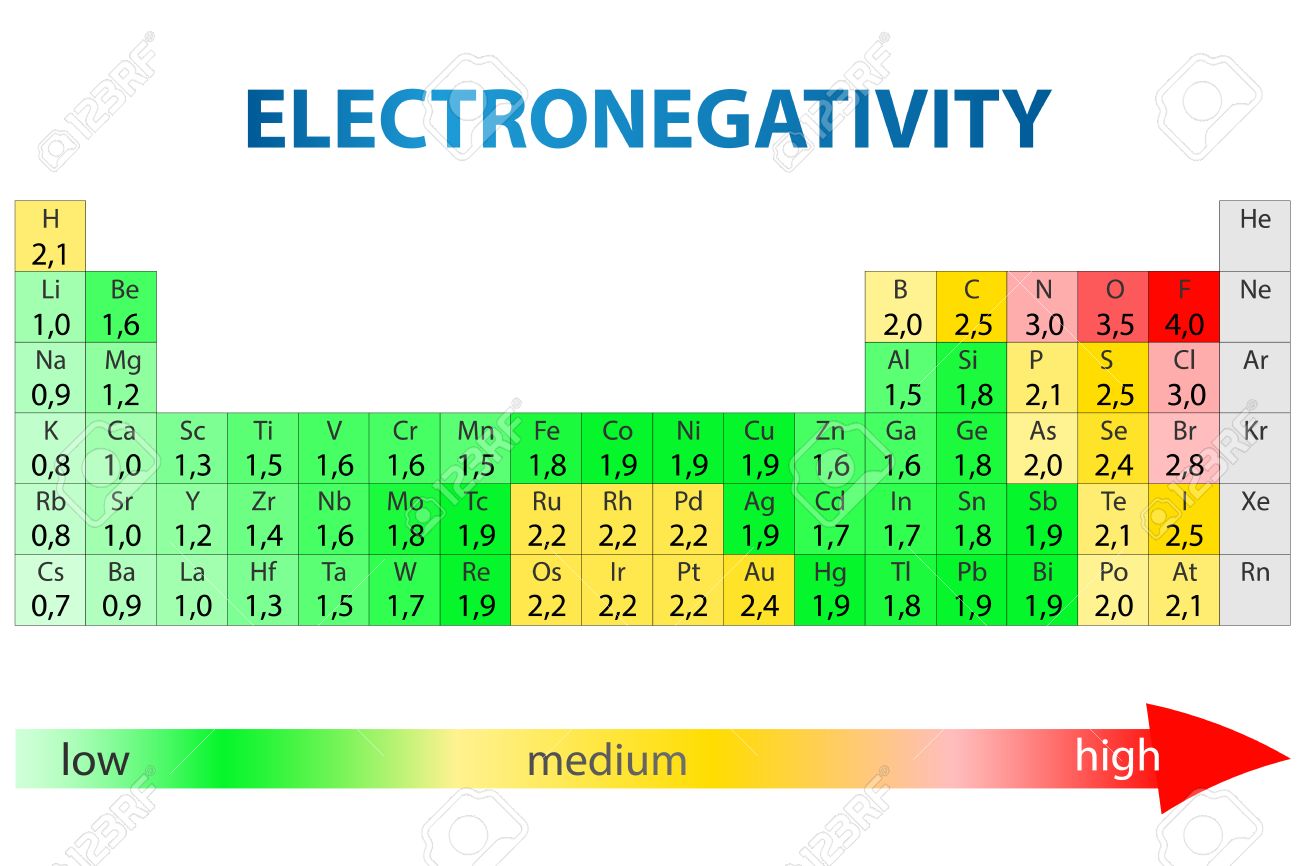

Czarno-biały Układ Okresowy
Pomysł elektronegatywności został przedstawiony przez Linusa Paulinga w 1932 roku; w skali Paulinga, fluor ma elektronegatywność 3,98, a inne składniki są skalowane w odniesieniu do tego szacunku. Inne skale elektronegatywności zawierają skalę Mullikena, zaproponowaną przez Roberta S. Mullikena w 1934 roku, w której główna witalność jonizacji i stronniczość elektronowa znajdują się w środkowej wartości razem, oraz skalę Allreda-Rochowa, która mierzy elektrostatyczną fascynację pomiędzy rdzeniem iota i jego elektronami walencyjnymi.
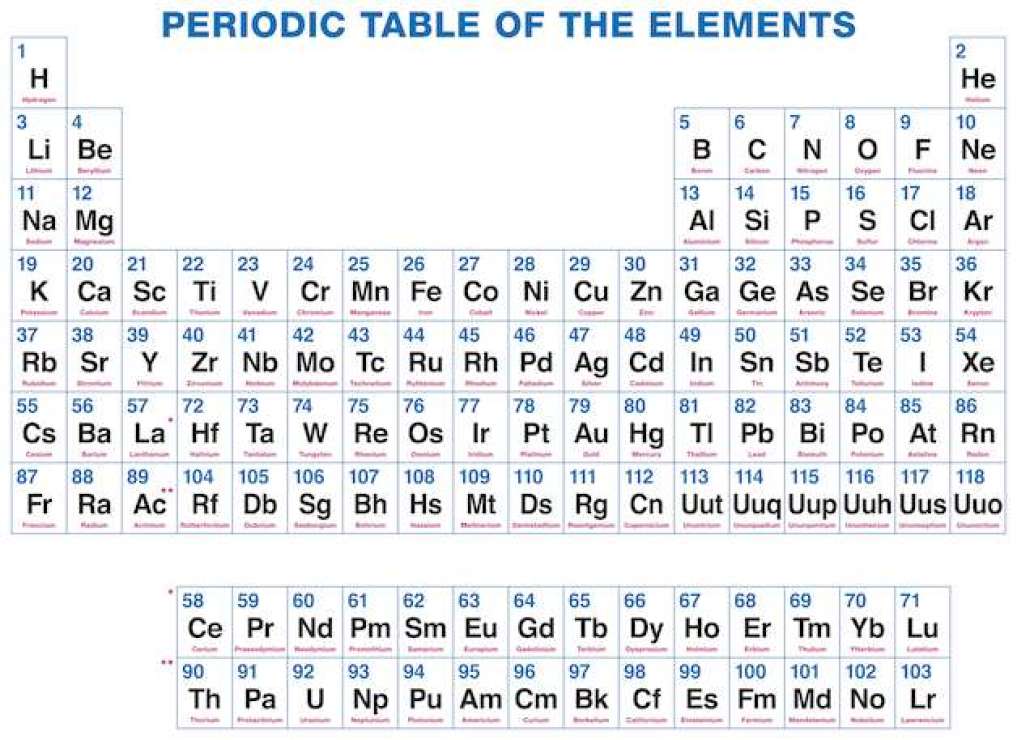

Elektronegatywność zmienia się typowo w tabeli przerywanej. Elektronegatywność przyrasta od podstawy do góry w zgromadzeniach, a przyrosty od lewej do odpowiedniej w poprzek okresów. Dlatego, fluor jest najbardziej elektronegatywny składnik, podczas gdy wapń jest jednym z najmniejszych elektronegatywnych. (Hel, neon i argon nie są rejestrowane w skali elektronegatywności Paulinga, pomimo faktu, że w skali Allreda-Rochowa, hel ma najbardziej godną uwagi elektronegatywność.
Interaktywny układ okresowy
Interaktywny układ okresowy jest o tym, jak bardzo znasz układ okresowy i jak bardzo jesteś w to zaangażowany, jeśli widzisz, że jest tam tylko liczba i alfabet, ale jeśli rozumiesz, widzisz kompletny świat w tym, który jest związany z nauką i to naprawdę pomaga we wszystkich terminach.
Jak wiemy atomy są naprawdę ważne w tym, który składa się z cząstek subatomowych takich jak proton, neutron i elektrony. Cząstki te mają różne – różne układy z dawaniem elektronów, rzecz, którą musimy pamiętać w każdym stanie jest to, że proton, neutron, elektron są dokładnie takie same jak proton, neutron i elektron z deferent innych elementów, w zasadzie jest to układy liczby, która sprawia, że różne elementy. Ale przed tym, generalnie zadajemy pytanie, co to jest proton, neutron lub elektron? więc tutaj staram się odpowiedzieć na to pytanie.
Interaktywny układ okresowy dla dzieci
Proton jest dodatnio naładowaną cząstką i waży 1 jednostkę masy atomowej (1.67xgrama) i ten znajduje się w jądrze.
Neutron jest neutralnie ujemnie naładowaną cząstką i waży około 1 masy atomowej i ten znajduje się w jądrze.
Elektrony są ujemnie naładowanymi cząstkami i ważą zero jednostek masy atomowej i znajdują się w różnych orbitach poziomu energetycznego, a masa elektronów wynosi 9,11x, co oznacza, że potrzeba 1830 elektronów, aby wyrównać masę jednego protonu.
Okazjonalna tabela składników substancji jest spisem znanych pierwiastków. W tabeli składniki są przedstawione na żądanie ich liczby atomowe, zaczynając od najmniejszej liczby. Liczba atomowa składnika jest taka sama jak liczba protonów w tym konkretnym atomie. W tabeli przerywanej składniki są uporządkowane w okresy i zbiory. Kolumna składników nad tabelą nazywana jest okresem. Każdy okres ma swój numer: od 1 do 8. W okresie 1 znajdują się tylko 2 składniki: wodór i hel. Okres 2 i 3 mają po 8 składników. Różne okresy są dłuższe. Składniki w okresie mają ciągłe liczby atomowe.
Darmowy Układ Okresowy PDF
Odcinek składników w tabeli nazywany jest gromadą. W standardowym stole okolicznościowym znajduje się 18 wiązek. Każde zgromadzenie ma swój numer: od 1 do 18. Komponenty w jednym zbiorze mają elektrony opanowane w porównywalny sposób, co daje im porównywalne właściwości mikstury (zachowują się w porównywalny sposób). Na przykład, zespół 18 jest znany jako gazy honorowe, ponieważ są one w większości gazami i nie łączą się z innymi cząsteczkami.
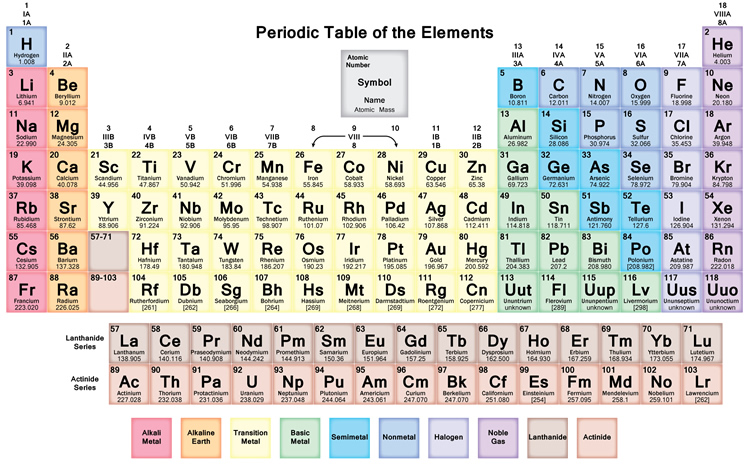

Istnieją dwa systemy numeracji zgromadzeń; jeden wykorzystujący cyfry arabskie (1,2,3) i dwa pozostałe wykorzystujące cyfry rzymskie (I, II, III).
Nazwy rzymskie zostały wykorzystane na początku i są zwyczajowymi nazwami; arabskie nazwy numeryczne są bardziej aktualne nazwy, które Międzynarodowa Unia Chemii Czystej i Stosowanej (IUPAC) wybrała do użytku również. Nazwy IUPAC miały zastąpić bardziej ugruntowane rzymskie ramy liczbowe. Układ okresowy został wymyślony i zaaranżowany przez rosyjskiego fizyka Dmitrija Iwanowicza Mendelejewa (1834-1907). W związku z tym składnik 101 został nazwany jego imieniem, mendelevium.
Tutaj znajduje się Układ Okresowy PDF Elementy
Układ okresowy jest również używany przez chemików do obserwacji wzoru i związku między elementami, który element jest związany z którym elementem, a także istnieją 3 główne grupy w układzie okresowym metal, metaloidy i gazy.
Tablica okresowa z masą
Jak wszyscy wiemy każdy element ma swoją unikalną masę, która jest mierzona przez wielu ekspertów w laboratorium i wtedy wychodzi wynik, a masa jest bardzo ważna, ponieważ przez to otrzymujemy wynik i otrzymujemy jak element, którego używamy do danego eksperymentu.
Masa jest ważna w wielu terminach i przez tablicę okresową wiemy łatwo, który element ma ile masy, więc w tym celu musisz po prostu pobrać tablicę okresową z masą, dzięki której wiesz ile każdy element zawiera. I możesz również nosić ze sobą pojedynczą kartkę papieru.
Orbitale układu okresowego
Jak wszyscy wiemy o układzie okresowym ich każda komórka podzielona przez ich orbitale i jest to rodzaj regionu prawdopodobieństwa, gdzie elektron może być znaleziony. I te całe regiony mają swój własny kształt.
Istnieje wiele orbitali takich jak orbitale S, orbitale P, orbitale D, i każdy orbital ma swoją własną unikalność i każdy orbital ma swój własny blok również.
Orbitale S, P, D, F Układ Okresowy
Jakbym mówił o orbitalu S jest pierwszym miejscem elektronu i znajduje się on w atomie. Następnie orbital P ma swoją własną wyjątkowość, że został wypełniony pełnym poziomem energii, elektrony zaczynają wypełniać się w następnym wyższym stylu orbitalnym. D orbitale również mają swoją własną wyjątkowość, że istnieją dwa inne style, które jest trochę skomplikowane do zrozumienia.