 Så kallad ”åderförkalkning” leder till förhöjt blodtryck och är i slutändan en betydande riskfaktor för trombos och hjärtsjukdomar. Förhärdningsprocessen är i själva verket förkalkning av blodkärlens vävnader med samma mineralform som i ben, ett kalciumfosfat som är besläktat med mineralet hydroxyapatit. Förkalkningen kan ske på fettavlagringar (aterosklerotiska plack) på insidan av blodkärlet (intimal eller aterosklerotisk förkalkning) eller i det mellersta skiktet av blodkärlsväggen (medial förkalkning), där den sistnämnda typiskt sett är förknippad med åldrande, diabetes och njursjukdom.
Så kallad ”åderförkalkning” leder till förhöjt blodtryck och är i slutändan en betydande riskfaktor för trombos och hjärtsjukdomar. Förhärdningsprocessen är i själva verket förkalkning av blodkärlens vävnader med samma mineralform som i ben, ett kalciumfosfat som är besläktat med mineralet hydroxyapatit. Förkalkningen kan ske på fettavlagringar (aterosklerotiska plack) på insidan av blodkärlet (intimal eller aterosklerotisk förkalkning) eller i det mellersta skiktet av blodkärlsväggen (medial förkalkning), där den sistnämnda typiskt sett är förknippad med åldrande, diabetes och njursjukdom.
Det finns betydande bevis för att cellerna i blodkärlsväggen (vaskulära glattmuskelceller) förändras när de utsätts för påfrestningar till mer benliknande celler och börjar uttrycka proteiner som typiskt sett är förknippade med förkalkning av ben. Här finns många frågor: Vad utlöser förkalkningsprocessen i blodkärlen, hur binder kalciumfosfatpartiklarna till blodkärlsvävnaden eller till fettavlagringar, varför är vissa förkalkade plack i blodkärlen stabila, medan andra har bitar som bryts av och orsakar blockeringar av blodkärlen?
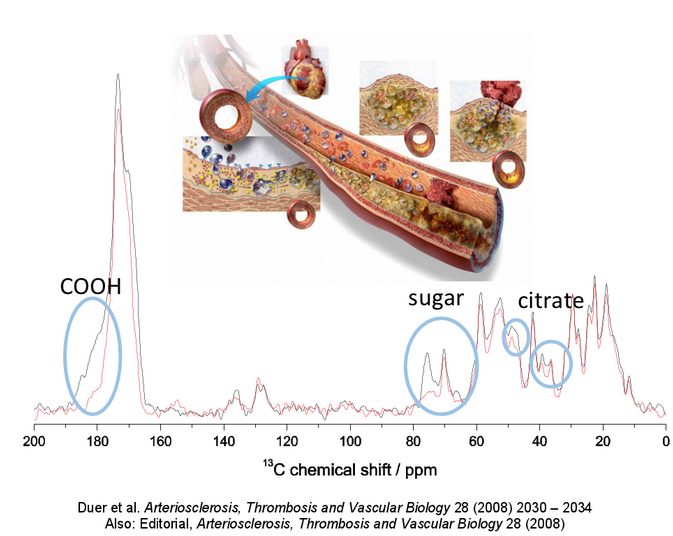
Vårt inledande arbete på detta område (Arteriosclerosis, Thrombosis and Vascular Biology, 2008) visade att samma molekyler som är ansvariga för att binda kalciumfosfatpartiklar i ben – funktionaliserade sockerarter – är ansvariga för samma process vid kärlförkalkning. Vi arbetar för närvarande med att identifiera vad dessa sockerarter är, i hopp om att man sedan kan utforma hämmare för deras funktion vid kärlförkalkning.
I vårt senaste arbete har vi visat att huruvida citrat införlivas i de vaskulära kalciumfosfatpartiklarna eller inte har en enorm effekt på både partiklarnas storlek och form och på hur giftiga de är för cellerna (Biomaterials, 2013). Faktum är att citrat ofta införlivas i förkalkade vävnader, inklusive ben (Calcified Tissue International, 2013), troligen på grund av att kalcium transporteras till förkalkningsställen i form av citratkomplex, och att de små, nanoskopiska porerna som förkalkning ofta sker i inte tillåter det transporterande citratet att ”komma undan”. Vi undersöker nu möjligheten att citratet märkbart påverkar kalciumfosfatpartiklarnas mekaniska egenskaper, och kan förklara varför vissa förkalkade kärlplack är stabila och andra märkbart mindre stabila.
Ett annat kännetecken för kärlförkalkning är att den alltid omedelbart föregås av cellnekros, så vi undersöker vilka cellmolekyler som avsätts i blodkärlsväggen som ett resultat av denna process. Det är detta som vi hoppas ska göra det möjligt för oss att fastställa vilka de funktionaliserade sockerarter som binder kalciumfosfatpartiklarna till vävnaden kan vara.
Samarbetspartners: Professor Cathy Shanahan (Kings College London), Dr Jeremy Skepper (PDN, University of Cambridge), Dr Karin Muller (PDN, University of Cambridge)
Finansiering: Vi har en gemensam överenskommelse om att använda oss av en ny metod för att utveckla och förbättra den nya metoden: Finansiering: British Heart Foundation