Knut Eichhorn-Mulligan, MD, PhD och Ivana K. Kim, MD, Boston
Choroidala nevi, särskilt små, är vanliga. Uppskattningar av deras förekomst varierar från 5 till 10 procent av den allmänna befolkningen. I Blue Mountains Eye Study registrerades choroidal nevi hos 6,5 procent av en prospektivt studerad population av mestadels medelålders vita australiensare.1 Choroidala melanom däremot är lyckligtvis sällsynta, med en uppskattad incidens på cirka sex per miljon. Trots detta är choroidalmelanom den vanligaste primära intraokulära maligniteten hos vuxna, och en snabb och korrekt diagnos är viktig.
Karakteristik av nevi
Histologiskt sett är nevi godartade neoplasmer av melanocyter som befinner sig i de yttre lagren av aorta. De uppträder vanligtvis som en platt, skiffergrå lesion under näthinnan. Nevi kan dock vara helt opigmenterade i upp till 10 procent av fallen.2 Risken för malign omvandling uppskattas vara ganska låg.3 Nevi har dock potential att orsaka synstörningar, särskilt om de är belägna nära fovea. Genom att komprimera den överliggande choriocapillaris kan tjockare nevi hindra blodflödet till RPE och de yttre näthinneskikten och leda till degeneration av RPE och fotoreceptorer.4 Nevi har förknippats med synfältsdefekter hos ett förvånansvärt stort antal patienter, även om dessa brister, om de är perifera, inte nödvändigtvis blir symtomatiska.5,6 Mer visuellt betydelsefulla komplikationer som observerats i samband med godartade nevi är bland annat serösa avlossningar av RPE och näthinnan och choroidal neovaskularisering.4 En nyligen genomförd granskning av synfunktionen hos mer än 3 400 patienter med nevi vid Wills Eye Hospital visade att den uppskattade risken för synförlust under 15 år var 2 procent hos patienter med extrafoveala nevi, men 26 procent hos patienter med subfoveolära nevi.7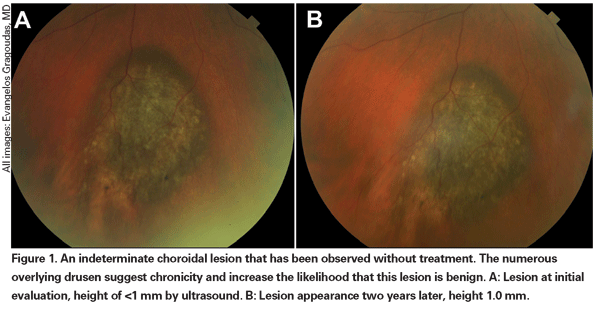
Om melanom uppstår från redan existerande nevi, eller om det i själva verket är en separat enhet, är något kontroversiellt. Analyser av enukleerade ögon har visat histologiska drag som är karakteristiska för nevi i kanterna på maligna melanom, vilket tyder på att åtminstone vissa melanom kan utvecklas från malign omvandling inom redan existerande nevi.8 Icke desto mindre anses risken för att ett choroidalt nevus ska förvandlas till ett melanom generellt sett vara extremt låg. Uppskattningar av den årliga andelen maligna förändringar varierar mellan en på 4 800 och en på 8 800.3,9
I allmänhet förstoras små choroidala nevi sällan. I Blue Mountains-studien visade endast ett av 160 nevi (medeldiameter 1,25 mm), för vilka minst fem års uppföljning fanns tillgänglig, en liten ökning av diametern.10 Det finns dock flera rapporter om histologiskt bekräftade choroidala nevi som hade uppvisat en progressiv förstoring, men som vid noggrann granskning saknade maligna drag.11,12 I en analys av mer än 2 500 ögon som följdes i en tertiär remissmottagning noterade Carol Shields, MD, och kollegor dessutom en förstoring hos 3 till 4 procent av nevi utan kännetecken på malign omvandling.2 Nevi i denna klinikbaserade kohort var betydligt större vid baslinjen än de i den befolkningsbaserade Blue Mountains-studien, med en genomsnittlig diameter på cirka 5 mm.

Detektering av små melanom
Pigmenterade choroidala lesioner som är svagt förhöjda kan kallas indeterminerade lesioner och utgör en utmaning när det gäller diagnos och behandling. Med tanke på riskerna och begränsningarna när det gäller att få histologisk bekräftelse av malignitet måste oftalmologer förlita sig på kliniska egenskaper som identifierats som prediktiva för tillväxt och metastasering för att skilja små melanom från förhöjda choroidala melanocytära tumörer som troligen är godartade. Dr. Shields och kollegor identifierade fem faktorer som är förknippade med risken för tillväxt av små choroidala melanocytiska lesioner som är mindre än 3 mm tjocka från retrospektiva analyser av cirka 1 300 patienter.13 Dessa faktorer var: Dessa faktorer var följande: 1) tumörtjocklek större än 2,0 mm, 2) subretinal vätska, 3) visuella symtom, 4) orangefärgat pigment, 5) bakre tumörmarginal som rör vid skivan. Lesionstillväxt observerades hos 4 procent av patienterna utan någon av dessa riskfaktorer, 36 procent av dem med en riskfaktor och hos mer än 50 procent av dem med tre eller fler faktorer.14 Kliniska faktorer som var förknippade med ökad risk för metastasering var bl.a: 1) bakre marginal som berör diskus, 2) dokumenterad tillväxt och 3) ökad tumörtjocklek (större än/jämnt med 1,1 mm).13 I den observationsstudie av små tumörer som genomfördes av Collaborative Ocular Melanoma Study (COMS) Group identifierades liknande riskfaktorer som är förknippade med tumörtillväxt, nämligen 1) större apikal tumörtjocklek, 2) större ursprunglig basal diameter, 3) förekomst av orangefärgat pigment, 4) avsaknad av drusen och 5) avsaknad av förändring av retinapigmentepitelet i anslutning till tumören.15 Dessa två sista faktorer bekräftar den kliniska observationen att närvaron av drusen och pigmentförändringar är indikatorer på kronicitet, och därför är det mer sannolikt att de ses över vilande, godartade lesioner. 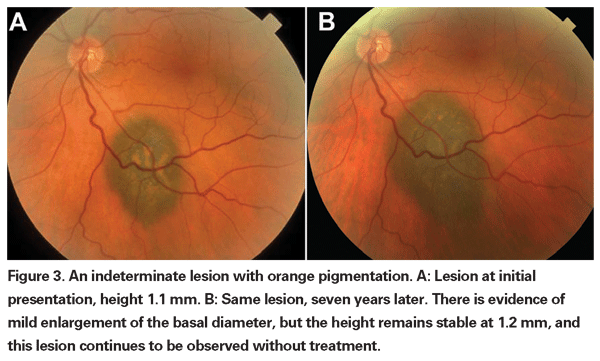
Bildgivande egenskaper kan också vara till hjälp vid bedömning av potentiell malignitet. Närvaron av en inre lugn zon på B-scan ultraljud och heta fläckar på fluoresceinangiografi har visat sig vara prediktorer för tumörtillväxt.16 Den roll som optisk koherenstomografi spelar i utvärderingen av choroidala lesioner håller också på att utforskas. Gabriella Espinoza, MD, och kollegor har föreslagit att OCT kan vara värdefullt för att skilja mellan aktiv subretinal vätska, där näthinnan som överlagrar lesionen är förhöjd men i övrigt normal till utseendet, och kroniska förändringar som retinala gallringar eller intraretinala cystor. I sin lilla serie fann de en korrelation mellan en aktiv subretinal vätska på OCT och dokumenterad tumörtillväxt.17
Förtida behandling vs. Observation
När enucleation var den enda accepterade behandlingsformen för melanom förespråkades observation tills dokumenterad tillväxt för små tumörer som inte definitivt kunde diagnostiseras som melanom vid första presentationen. Nu när det finns tillgång till och påvisad effekt av globesparande behandlingar kan man argumentera för tidigare behandling av dessa obestämda lesioner. Uppgifter från COMS-försöken visar att den melanomrelaterade dödligheten varierar med tumörstorleken vid behandlingstillfället. För medelstora tumörer (definierade som tumörer 2,5 till 10 mm i apikal höjd och upp till 16 mm i största basala diameter) var den melanomspecifika dödligheten 10 procent efter fem år och 18 procent efter 10 år.18 För stora tumörer (de som överskrider storlekskriterierna för medelstora tumörer i antingen apikal höjd eller största basala diameter; eller peripapillära tumörer med en apikal höjd större än 8 mm) ökade frekvenserna till cirka 27 procent vid fem år och 40 procent vid 10 år.19 Dessutom har, som nämnts ovan, dokumenterad tillväxt före behandling visat sig vara en riskfaktor för metastasering. Tillväxt kan dock vara en markör för mer aggressiva tumörer, och det har inte bevisats att behandling av dessa tumörer tidigare minskar dödligheten.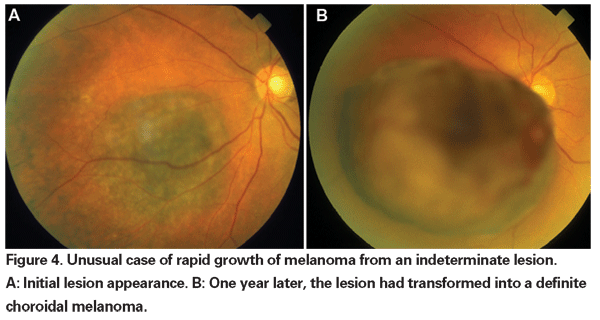
Våra nuvarande strålbehandlingsmetoder möjliggör effektiv lokal tumörkontroll med bevarande av globen, men den visuella morbiditeten är fortfarande hög. Det är därför nödvändigt att väga den mortalitetsrisk som uppstår genom noggrann observation före behandling av obestämda lesioner mot konsekvenserna av den synförlust som terapin medför. I COMS-observationsstudien om små tumörer inträffade sex melanomrelaterade dödsfall i en grupp på 67 patienter med tumörer som behandlades efter en inledande observationsperiod.20 Endast två av dessa dödsfall inträffade inom fem år efter inskrivningen, vilket resulterade i en ungefärlig femårig melanomspecifik dödlighet på 3 procent. Mer nyligen rapporterade forskare vid Bascom Palmer Eye Institute en femårig melanomspecifik dödlighet på 3,9 procent i en liten grupp patienter med misstänkt choroidalt melanom som observerades för tillväxt eller utveckling av orangefärgat pigment före behandling med plackstrålning.21 Dessa studier tyder på låg dödlighet i samband med fördröjd behandling av obestämda lesioner. Dessutom visade en liten retrospektiv serie ingen ökning av melanomspecifik mortalitet mellan snabbt behandlade och initialt observerade patienter.22 Hittills finns det inga bevis som visar på en överlevnadsfördel av tidigare jämfört med fördröjd behandling av små tumörer som inte slutgiltigt kan diagnostiseras som melanom. Därför är det inte klart att det definitivt kommer att rädda fler liv om man offrar synen hos ett större antal patienter med obestämda lesioner.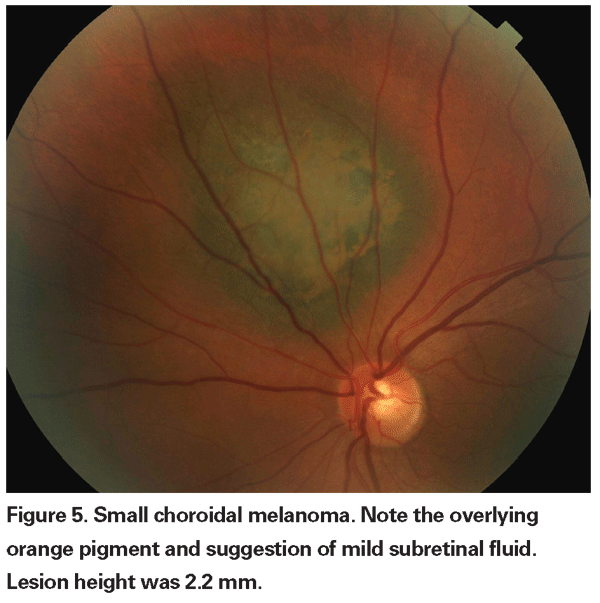
För att sammanfatta kan choroidala pigmenterade lesioner delas in i tre kategorier: 1) små, platta lesioner som tydligt är choroidala nevi, 2) små lesioner med förhöjning <2,5 mm som kan ha orangefärgat pigment eller subretinal vätska eller någon av de andra faktorerna som väcker misstanke om malignitet – de s.k. obestämda lesionerna, och 3) kupol- eller svampformade choroidala tumörer som är större än/jämnt med 2,5 mm och som tydligt är melanom. Det är behandlingen av de obestämda lesionerna som fortfarande är ett kontroversiellt område, och utvärdering och behandling av dessa lesioner utförs bäst av okulära onkologer. En klinisk prövning som jämför tidig respektive fördröjd behandling av obestämda lesioner är kanske inte genomförbar på grund av det stora antalet patienter och den långa uppföljningstid som krävs för att uppnå entydiga resultat. Med pågående framsteg inom molekylärdiagnostiska tekniker ligger det bästa hoppet om att öka överlevnaden för patienter med choroidalt melanom i utvecklingen av effektiva behandlingar för metastaserande sjukdom och i sökandet efter biomarkörer som mer exakt kan förutsäga malign omvandling.
Dr Eichhorn-Mulligan är specialistläkare i oftalmologi vid Harvard Medical School. Dr Kim är biträdande professor vid avdelningen för oftalmologi vid Harvard Medical School, Retina Service, Massachusetts Eye and Ear Infirmary.
1. Sumich P, Mitchell P, Wang J. Choroidal nevi in a white population – the Blue Mountains Eye Study. Arch of Ophthalmol 1998;116: 645-650.
2. Shields CL, Furuta M, Mashayekhi A, Berman EL, Zahler JD, Hoberman DM, Dinh DH, Shields JA. Kliniskt spektrum av choroidal nevi baserat på ålder vid presentationen i 3 422 konsekutiva ögon. Ophthalmology 2007: Dec 5 .
3. Singh AD, Kalyani P, Topham A. Uppskattning av risken för malign omvandling av en choroidal nevus. Ophthalmology 2005;112: 1784-1789.
4. Gonder JR, Augsburger JJ, McCarthy EF, Shields JA. Synförlust i samband med choroidala nevi. Ophthalmology 1982;89:961-965.
5. Tamler E, Maumenee AE. Klinisk undersökning av choroidala nevi. Arch Ophthalmol 1959;62:196-202.
6. Flindall RJ, Drance SM. Studier av synfältet vid godartade choroidala melanomata. Arch Ophthalmol 1969;81:41-44.
7. Shields CL, Furuta M, Mashayekhi A, Berman EL, Zahler JD, Hoberman DM, Dinh DH, Shields JA. Synskärpa hos 3 422 konsekutiva ögon med choroidal nevus. Arch Ophthalmol 2007;125:1501-1507.
8. Yanoff M, Zimmerman LE. Histogenes av maligna melanom i uvea. II. Förhållandet mellan uveala nevi och maligna melanom. Cancer 1967;20:493-507.
9. Ganley JP, Comstock GW. Godartade nevi och maligna melanom i aderhinnan. Am J Ophthalmol 1973;76:19-25.
10. Thiagalingam S, Wang JJ, Mitchell P. Ingen förändring av choroidal nevi över 5 år i en äldre population. Arch Ophthalmol 2004;122:89-93.
11. MacIlwaine WA, Anderson B Jr, Klintworth GK. Utvidgning av en histologiskt dokumenterad choroidal nevus. Am J Ophthalmol 1979;87:480-486.
12. Elner VM, Flint A, Vine AK. Histopatologi av dokumenterad tillväxt i små melanocytära choroidala tumörer. Arch Ophthalmol 2004;122:1876-1878.
13. Shields CL, Shields JA, Kiratli H, De Potter P, Cater JR. Riskfaktorer för tillväxt och metastasering av små choroidala melanocytiska lesioner. Ophthalmology 1995;102:1351-1361.
14. Shields CL, Cater J, Shields JA, Singh AD, Santos MCM, Carvalho C. Kombination av kliniska faktorer som förutsäger tillväxt av små choroidala melanocytära tumörer. Arch Ophthalmol 2000;118:360-364.
15. Collaborative Ocular Melanoma Study Group. Faktorer som förutsäger tillväxt och behandling av små choroidala melanom. Arch Ophthalmol 1997;115:1537-1544.
16. Butler P, Char DH, Zarbin M, Kroll S. Natural history of indeterminate pigmented choroidal tumors. Ophthalmology 1994;101: 710-716.
17. Espinoza G, Rosenblatt B, Harbour W. Optical coherence tomography in the evaluation of retinal changes associated with suspicious choroidal melanocytic tumors. Am J Ophthalmol 2004;137:90-95.
18. The Collaborative Ocular Melanoma Study Group. Den randomiserade COMS-studien av jod 125-brachyterapi för choroidal melanom: V. Tolvårsmortalitet och prognostiska faktorer: COMS-rapport nr 28. Arch Ophthalmol 2006;1684-1693.
19. Hawkins BS, The Collaborative Ocular Melanoma Study Group. Collaborative Ocular Melanoma Study (COMS) randomiserad studie av strålning före kärnbildning av stora choroidala melanom: IV. Tioårig dödlighet och prognostiska faktorer. COMS-rapport nr 24. Am J Ophthalmol 2004;138:936-951.
20. The Collaborative Ocular Melanoma Study Group. Mortalitet hos patienter med små choroidala melanom. Arch of Ophthalmol 1997;115:886-893.
21. Sobrin L, Schiffman JC, Markoe AM, Murray TG. Utfallet av strålbehandling med jod 125 plackradioterapi efter initial observation av misstänkta små choroidala melanom. Ophthalmology 2005;112:1777-1783.
22. Augsburger JJ, Vrabec TR. Impact of delayed treatment in growing posterior uveal melanomas. Arch Ophthalmol 1993;111:1382-6.