Dit is een kort overzicht van de informatie met betrekking tot de goedkeuring van de FDA om dit product op de markt te brengen. Zie de links hieronder naar de samenvatting van de veiligheids- en doeltreffendheidsgegevens (SSED) en de productetikettering voor meer volledige informatie over dit product, de indicaties voor gebruik, en de basis voor de goedkeuring van de FDA.
Productnaam: Inspire® Upper Airway Stimulation (UAS)
PMA Aanvrager: Inspire Medical Systems, Inc.
Adres: 5500 Wayzata Blvd. Suite 1600
Golden Valley, MN 55416 US
Approval Date: April 14, 2020
Goedkeuringsbrief: Approval Order
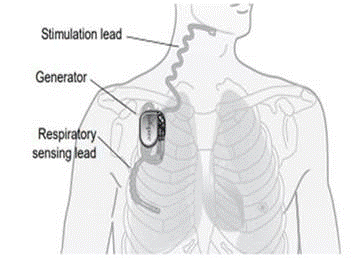
Wat is het? Het Inspire® Upper Airway Stimulation (UAS)-systeem is een implanteerbare zenuwstimulator die wordt gebruikt om matige tot ernstige obstructieve slaapapneu (OSA) te behandelen. Het Inspire® UAS-systeem bestaat uit geïmplanteerde componenten, waaronder de implanteerbare pulsgenerator (IPG), stimulatie lead, en sensing lead en externe componenten zoals het programmeerapparaat voor de arts en het programmeerapparaat voor de patiënt.
Deze goedkeuring breidt de indicaties uit voor het gebruik van de Inspire® UAS bij patiënten tussen 18 en 21 jaar met matige tot ernstige OSA die:
- geen volledige blokkade van de bovenste luchtwegen hebben
- niet in staat zijn, of niet effectief worden behandeld door, het verwijderen van amandelen en ander zacht weefsel achter de neus
- niet in staat zijn, of PAP-therapie niet kunnen verdragen ondanks pogingen om de therapietrouw te verbeteren
- de standaard zorg hebben gevolgd bij het overwegen van alle andere alternatieve / aanvullende therapieën
Hoe werkt het? De implanteerbare pulsgenerator detecteert het ademhalingspatroon van de patiënt en houdt de luchtwegen open door middel van milde zenuwstimulatie. De arts kan de stimulatie-instellingen configureren met behulp van het externe programmeerapparaat van de arts. Met de slaapafstandsbediening kan de patiënt de therapie aanzetten voordat hij gaat slapen en uitzetten wanneer hij wakker wordt.
Wanneer wordt het gebruikt? Het Inspire® UAS-systeem wordt gebruikt voor de behandeling van een subgroep van patiënten met matige tot ernstige OSA. De ernst van apneu (ademverlies) of hypopneu (gedeeltelijk verlies van adem) wordt bepaald door een schaal die apneu-hypopneu-index (AHI) wordt genoemd. Matige tot ernstige OSA wordt beschreven als een AHI van groter dan of gelijk aan 15 en kleiner dan of gelijk aan 65. Inspire® UAS wordt gebruikt bij volwassen patiënten van 18 jaar en ouder bij wie is bevestigd dat ze behandelingen met positieve luchtwegdruk (PAP) (zoals continue positieve luchtwegdruk of bi-level positieve luchtwegdrukmachines) niet goed verdragen of niet kunnen verdragen en bij wie de bovenste luchtweg niet volledig is geblokkeerd.
PAP-falen wordt gedefinieerd als een onvermogen om OSA te elimineren (AHI van meer dan 15 ondanks PAP-gebruik), en PAP-intolerantie wordt gedefinieerd als:
- Onvermogen om PAP te gebruiken (meer dan 5 nachten per week gebruik; gebruik gedefinieerd als meer dan 4 uur gebruik per nacht), of
- Onwil om PAP te gebruiken (bijvoorbeeld een patiënt stuurt het PAP-systeem terug na een poging het te gebruiken).
Wat wordt er bereikt? Honderd zesentwintig (126) patiënten hebben deelgenomen aan een klinische studie op 22 onderzoekslocaties ter ondersteuning van de oorspronkelijke goedkeuring van Inspire® UAS. Inspire® UAS-therapie bood de meerderheid van de patiënten klinisch zinvolle verminderingen in de ernst van hun obstructieve slaapapneu en verbeteringen in hun kwaliteit van leven. Meer dan de helft van alle patiënten werden beschouwd als responders voor Inspire® UAS-therapie, met ten minste 50% vermindering van de AHI en een AHI van minder dan 20 gebeurtenissen per uur op het eindpunt van 12 maanden. Inspire® UAS-therapieresponders ervoeren ook een vermindering van ten minste 25% in de zuurstofdesaturatie-index (ODI), een schaal die wordt gebruikt om de ernst van slaapapneu aan te geven. De resultaten van deze studie, in aanvulling op een kleine klinische studie bij pediatrische patiënten met het syndroom van Down, ondersteunden de uitbreiding van de indicaties naar oudere adolescenten tussen 18 en 21 jaar.
Wanneer mag het niet worden gebruikt? Het Inspire® UAS-systeem mag niet worden gebruikt voor de volgende zaken:
- Typen apneu (centraal en gemengd) anders dan obstructief zijn meer dan 25% van de totale AHI
- Elke fysieke bevinding die de werking van de stimulatie van de bovenste luchtwegen in gevaar zou brengen, zoals de aanwezigheid van een volledige blokkade van de bovenste luchtweg
- Een aandoening of procedure die de neurologische controle van de bovenste luchtweg heeft aangetast
- Patiënten die niet in staat zijn of niet de nodige hulp hebben om de slaapafstandsbediening te bedienen
- Patiënten die zwanger zijn of van plan zijn zwanger te worden
- Patiënten met een implanteerbaar apparaat dat vatbaar kan zijn voor onbedoelde interactie met het Inspire®-systeem. Raadpleeg de fabrikant van het hulpmiddel om de mogelijkheid van interactie te beoordelen.
- Patiënten die magnetische resonantie beeldvorming (MRI) nodig hebben, anders dan wat is gespecificeerd in de MR-etikettering onder voorwaarden
Aanvullende informatie (inclusief waarschuwingen, voorzorgsmaatregelen en bijwerkingen):
- Samenvatting van gegevens over veiligheid en doeltreffendheid (SSED)
- etikettering door arts
- etikettering door patiënt
- PMA-databankinvoer