Ceci est un bref aperçu des informations relatives à l’autorisation de la FDA de commercialiser ce produit. Consultez les liens ci-dessous vers le résumé des données de sécurité et d’efficacité (SSED) et l’étiquetage du produit pour obtenir des informations plus complètes sur ce produit, ses indications d’utilisation et les bases de l’approbation de la FDA.
Nom du produit : Inspire® Stimulation des voies aériennes supérieures (UAS)
Demandeur de l’AMM : Inspire Medical Systems, Inc.
Adresse : 5500 Wayzata Blvd. Suite 1600
Golden Valley, MN 55416 US
Date d’approbation : 14 avril 2020
La lettre d’approbation : Approval Order
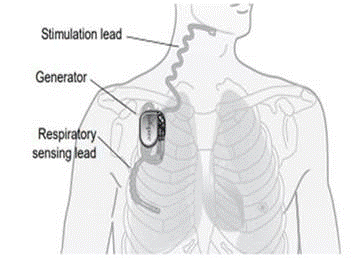
Qu’est-ce que c’est ? Le système Inspire® de stimulation des voies aériennes supérieures (SAU) est un stimulateur nerveux implantable utilisé pour traiter l’apnée obstructive du sommeil (SAOS) modérée à sévère. Le système Inspire® UAS est constitué de composants implantés, notamment le générateur d’impulsions implantable (IPG), la sonde de stimulation et la sonde de détection, et de composants externes tels que le programmateur du médecin et le programmateur du patient.
Cette autorisation élargit les indications d’utilisation du système Inspire® UAS chez les patients âgés de 18 à 21 ans atteints de SAOS modéré à sévère qui :
- ne présentent pas d’obstruction complète des voies aériennes supérieures
- ne peuvent pas, ou ne sont pas traités efficacement par l’ablation des amygdales et autres tissus mous derrière le nez
- Il a été confirmé que le traitement par PAP échoue ou ne peut pas être toléré malgré les tentatives d’amélioration de l’observance
- Ils ont suivi les soins standard en considérant toutes les autres thérapies alternatives/adjointes
Comment cela fonctionne-t-il ? Le générateur d’impulsions implantable détecte le schéma respiratoire du patient et maintient les voies respiratoires ouvertes par une légère stimulation nerveuse. Le médecin est en mesure de configurer les paramètres de stimulation à l’aide du programmateur externe du médecin. La télécommande de sommeil du patient permet à ce dernier d’activer la thérapie avant de s’endormir et de l’éteindre à son réveil.
Quand est-il utilisé ? Le système Inspire® UAS est utilisé pour traiter un sous-ensemble de patients présentant un SAOS modéré à sévère. La gravité des apnées (perte de souffle) ou des hypopnées (perte partielle de souffle) est déterminée par une échelle appelée indice d’apnée-hypopnée (IAH). Un SAOS modéré à sévère est décrit par un IAH supérieur ou égal à 15 et inférieur ou égal à 65. L’Inspire® UAS est utilisé chez les patients adultes âgés de 18 ans et plus dont il a été confirmé qu’ils échouent ou ne tolèrent pas les traitements par pression positive (PAP) (tels que les machines à pression positive continue ou à pression positive à deux niveaux) et qui ne présentent pas une obstruction complète des voies aériennes supérieures.
L’échec de la PAP est défini comme une incapacité à éliminer le SAOS (IAH supérieur à 15 malgré l’utilisation de la PAP), et l’intolérance à la PAP est définie comme :
- Incapacité à utiliser la PAP (plus de 5 nuits par semaine d’utilisation ; utilisation définie comme plus de 4 heures d’utilisation par nuit), ou
- Maladresse à la PAP (par exemple, un patient retourne le système de PAP après avoir tenté de l’utiliser).
Qu’est-ce que cela va accomplir ? Cent vingt-six (126) patients ont participé à une étude clinique à travers 22 sites d’investigation pour soutenir l’approbation initiale du SAU Inspire®. Le traitement par Inspire® UAS a permis à la majorité des patients d’obtenir une réduction cliniquement significative de la sévérité de leur apnée obstructive du sommeil et une amélioration de leur qualité de vie. Plus de la moitié des patients ont été considérés comme des répondeurs au traitement Inspire® UAS, avec une réduction d’au moins 50 % de l’IAH et un IAH inférieur à 20 événements par heure au terme des 12 mois. Les répondeurs à la thérapie Inspire® UAS ont également enregistré une réduction d’au moins 25 % de l’indice de désaturation en oxygène (ODI), une échelle utilisée pour indiquer la gravité de l’apnée du sommeil. Les résultats de cette étude, en plus d’une petite étude clinique chez des patients pédiatriques atteints du syndrome de Down, ont apporté un soutien à l’élargissement des indications pour inclure les adolescents plus âgés, entre 18 et 21 ans.
Quand ne doit-on pas l’utiliser ? Le système Inspire® UAS ne doit pas être utilisé dans les cas suivants :
- Les types d’apnée (centrale et mixte) autres qu’obstructive représentent plus de 25 % de l’IAH total
- Toute constatation physique qui compromettrait la performance de la stimulation des voies aériennes supérieures, telle que la présence d’une obstruction complète des voies aériennes supérieures
- Toute affection ou procédure ayant compromis le contrôle neurologique des voies aériennes supérieures
- Patients qui ne peuvent pas ou ne disposent pas de l’assistance nécessaire pour faire fonctionner la télécommande de sommeil
- Patients enceintes ou qui prévoient de l’être
- Patients ayant un dispositif implantable susceptible d’interagir de manière involontaire avec le système Inspire®. Consulter le fabricant du dispositif pour évaluer la possibilité d’interaction.
- Patients nécessitant une imagerie par résonance magnétique (IRM) autre que ce qui est spécifié dans la notice MR conditionnelle
Informations supplémentaires (y compris avertissements, précautions et effets indésirables) :
- Résumé des données de sécurité et d’efficacité (SSED)
- Étiquetage par le médecin
- Étiquetage par le patient
- Entrée dans la base de données de l’AMM
.