Generic Name: heparin sodium
Dosage Form: injection, solution
Medically reviewed by Drugs.com. Last updated on February 19, 2021.
- Overview
- Side Effects
- Dosage
- Professional
- Tips
- Interactions
- More
WARNING:
NOT FOR USE IN NEONATES
Description
SOLUTION IS INTENDED FOR MAINTENANCE OF PATENCY OF INTRAVENOUS INJECTION DEVICES ONLY AND IS NOT TO BE USED FOR ANTICOAGULANT THERAPY.
Heparin Lock Flush Solution, USP is a sterile, nonpyrogenic, hypertonic preparation of heparin sodium injection, USP with sodium chloride in water for injection.
Each milliliter (mL) contains: ヘパリンナトリウム、10または100 USP単位(ブタの腸粘膜由来)、塩化ナトリウム9mg、安定剤として添加された無水エデト酸二ナトリウム0.1mg、保存料として添加されたベンジルアルコール9mgを注射用水で含有しています。 pH6.5(5.0~7.5)の水酸化ナトリウムを含むことがある。 これらの溶液のオスモル濃度は 392 mOsmol/L(カルク)である。
Heparin Lock Flush Solution, USPは、静脈注射器の開存性の維持のみを目的としており、抗凝固療法には使用されません。
Heparin Sodium, USPは、抗凝固特性を有するグリコサミノグリカンと呼ばれる直鎖アニオン性ムコ多糖の不均一なグループであり、このムコ多糖は抗凝固特性を有する。 ヘパリンに含まれる主な糖は、以下の通りです。 (a-L-イズロン酸2-硫酸、2-デオキシ-2-スルファミノ-a-D-グルコース6-硫酸、b-D-グルクロン酸、2-アセトアミド-2-デオキシ-a-D-グルコース、5)a-L-イズロン酸などである。 これらの糖は、通常、(2)よりも(1)よりも(4)よりも(3)よりも(5)の順に多く存在し、グリコシド結合により、様々な大きさのポリマーを形成している。 ヘパリンは硫酸基とカルボン酸基が共有結合しているため、強酸性である。 ヘパリンナトリウムでは、硫酸基の酸性プロトンの一部がナトリウムイオンで置き換えられています。
ヘパリンナトリウムの構造(代表的なサブユニット):
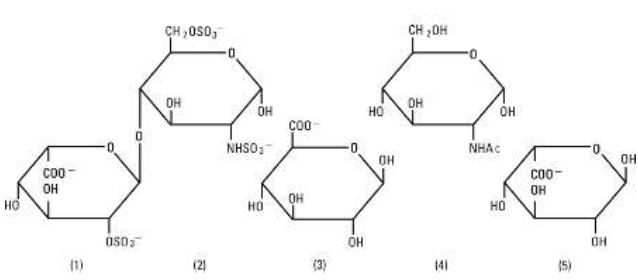
塩化ナトリウム(USP)は化学名NaCl、水に自由に溶ける白い結晶性の化合物であります。 この半硬質バイアルは、特別に処方されたポリオレフィンから製造されています。 これは、エチレンとプロピレンの共重合体です。 このプラスチックは、プラスチック容器のUSP生物学的規格に準拠した動物実験により、安全性が確認されています。
ヘパリンは、in vitroおよびin vivoの両方で、血液の凝固やフィブリン凝塊の形成につながる反応を阻害します。 ヘパリンは正常な凝固系の複数の部位に作用する。 少量のヘパリンとアンチトロンビンIII(ヘパリン補酵素)の併用により、活性化された第X因子を不活性化し、プロトロンビンのトロンビンへの変換を阻害することで血栓を抑制することができます。 いったん活性化した血栓症が進行すると、より多量のヘパリンはトロンビンを不活性化し、フィブリノーゲンからフィブリンへの変換を阻害することにより、さらなる凝固を抑制することができる。 また、ヘパリンはフィブリン安定化因子の活性化を阻害することで、安定したフィブリン塊の形成を阻害します。 出血時間は通常、ヘパリンによる影響を受けません。 凝固時間は、治療用量のヘパリンを全量投与すると延長されます。ほとんどの場合、低用量のヘパリンでは測定不能なほどの影響はありません。 60歳以上の患者は、同量のヘパリンを投与した場合、60歳未満の患者と比較して、血漿中のヘパリン濃度が高く、活性化部分トロンボプラスチン時間(APTT)が長くなることがあります。 ヘパリンの血漿中濃度のピークは皮下投与後2~4時間で達成されますが、かなりの個人差があります。 広範囲の投与量におけるヘパリン血漿濃度の時間に対する対数線形プロットは線形であり、ゼロ次過程が存在しないことが示唆されます。 肝臓および網状内皮系は生体内変換の場である。 二相性の排泄曲線は、急速に減少するα相(t½ =10#)と40歳以降の遅いβ相であり、臓器への取り込みを示す。 抗凝固剤の半減期と半減期濃度の間に関係がないのは、ヘパリンの蛋白結合などの要因を反映していると思われる。 ヘパリンには線溶活性がないため、既存の血栓を溶かすことはありません。 ヘパリンロックフラッシュ液は、静脈内注射器の開存性維持に使用する場合、1mL当たり10又は100USP単位の単回投与では、全身性抗凝固作用を示さない。 ただし、カテーテルのプライミング量と同量のヘパリン-生理食塩水を吸引し、廃棄してから血液を採取しないと、こうした器具から採取した血液サンプルの実験室検査に支障を来すことがあります。 等張濃度の塩化ナトリウムは、ナトリウム損失を超えるか等しい塩化物損失を非経口的に補うのに 適している。
水中の塩化ナトリウムは解離してナトリウムイオン(Na+)と塩化物イオン(Cl-)を生成する。
水中の塩化ナトリウムは解離してナトリウム(Na+)と塩化物(Cl-)になり、ナトリウム(Na+)は細胞外液の主要陽イオンで、体液および電解質異常の治療に大きな役割を担っています。 塩化物(Cl-)は、赤血球内で酸素と二酸化炭素の交換が行われる際に、緩衝作用として不可欠な役割を担っている。 ナトリウム(Na+)の分布と排泄は、摂取と排泄のバランスを保つ腎臓の制御下にあります。
ヘパリンロック・フラッシュ液(USP)が提供する少量の液体と塩化ナトリウムの量は、静脈注射装置の開存性を維持するための媒体としてのみ使用する場合、おそらく非常に小さな乳児を除いて、液体および電解質バランスに大きな影響を及ぼす可能性はありません。 静脈への装置の最初の設置後、薬剤の各注入後、または実験室分析のための採血後に使用されることがあります。
禁忌
新生児におけるベンジルアルコールの潜在的毒性により、ベンジルアルコールを含む溶液はこの患者集団に使用してはならない。 ベンジルアルコールを含む非経口製剤は、体液または塩化ナトリウムの補充に使用してはならない。 ヘパリンナトリウムは、患者に使用してはならない。 ヘパリンに対して過敏症のある患者;制御不可能な活動的出血状態(播種性血管内凝固による場合を除く)(警告を参照);適切な血液凝固検査(例えば、全血凝固時間、部分トロンボプラスチン時間など)を必要間隔で行うことができない患者;などです。
警告
ヘパリンロックフラッシュソリューション、USPの複数回投与バイアル製剤の保存料であるベンジルアルコールは、新生児における毒性と関連付けられています。 ベンジルアルコールは、未熟児の胎児の「Gasping Syndrome」と関連することが報告されています。 この年齢層における他の防腐剤の毒性に関するデータはありません。 防腐剤フリーのヘパリン・ロック・フラッシュ液(USP)は、新生児の静脈注射器具の開存性を維持するために使用されるべきです。 ヘパリンロック・フラッシュ・ソリューション、USPは、筋肉内使用、全身性抗凝固または非経口投与経路による注射を意図していません。 ヘパリンに対する過敏症が証明されている患者には、明らかに生命を脅かす状況でのみ投与されるべきです。
出血:ヘパリンを投与されている患者では、事実上あらゆる部位で出血が発生する可能性があります。 原因不明のヘマトクリット値の低下、血圧の低下、その他原因不明の症状は、出血性事象を真剣に検討する必要があります。 ヘパリンナトリウムは、出血の危険性が高まる疾患状態において、細心の注意を払って使用する必要があります。 出血の危険が増加するある状態のいくつかがある:
心循環器-亜急性の細菌の心内膜炎。
消化器系-胃や小腸の潰瘍性病変や持続的なチューブドレナージ
その他-月経、止血障害を伴う肝疾患
凝固能検査。 凝固検査:凝固検査が不当に長引いた場合、または出血が生じた場合は、速やかにヘパリンナトリウムを中止すること。 10 USPヘパリンユニット/mLの濃度を有するヘパリン溶液は、血液凝固検査の結果を変化させることがある。 ヘパリン濃度が10 USP Heparin Units/mLを超えると、血液凝固検査結果が変化する。
血小板減少症。 血小板減少症:ヘパリン投与患者において血小板減少症が報告されており、その発現率は0~30%と報告されています。 軽度の血小板減少症(10万/mm3以上)は、ヘパリンを継続投与しても安定または回復することがあります。 しかし、どの程度の血小板減少症であっても、注意深く観察する必要があります。 血小板数が10万/mm3以下になった場合、または血栓症の再発(白色血栓症、注意事項を参照)の場合は、ヘパリン製剤を中止する必要があります。 ヘパリン治療の継続が不可欠な場合、別の臓器由来のヘパリン投与を慎重に再開することができる。 ナトリウムイオンを含む溶液は、うっ血性心不全、重篤な腎不全の患者及びナトリウム貯留を伴う浮腫が存在する臨床状態において、使用する場合には十分注意すること。 すべての容器への単回または複数回の注入・抜去は無菌操作で行うこと。 本剤のヘパリンナトリウムは動物組織由来であるため、アレルギー歴のある患者には慎重に使用すること。
臨床検査への干渉
ヘパリンは血清チロキシン測定の競合タンパク結合法に干渉し、誤った値を上昇させることがあります。 ヘパリンロックフラッシュ液は、グルコース、血清ナトリウム、血清塩化物などの血液化学検査、血液凝固検査などの臨床検査を妨害したり、結果を変化させることがあります。 (臨床薬理学参照) ヘパリンナトリウムの全身性抗凝固剤としての使用に関連する以下の情報は、ヘパリンロックに対する本剤の使用に該当することが知られていないため、参考情報として記載した。
全般:
a. 白色血栓症候群:
ヘパリンを投与されている患者さんでは、ヘパリンによる血小板の不可逆的凝集による血小板減少に伴い、新しい血栓形成を起こすことがあり、いわゆる「白色血栓症候群」と呼ばれることが報告されています。 この過程は、皮膚壊死、切断に至る四肢壊疽、心筋梗塞、肺塞栓症、脳卒中、場合によっては死亡などの重篤な血栓塞栓性合併症を引き起こす可能性がある。 そのため、血小板減少に伴い新たな血栓症が発生した場合には、速やかにヘパリン投与を中止する必要があります。
b. ヘパリン耐性:
発熱、血栓症、血栓性静脈炎、血栓傾向のある感染症、心筋梗塞、癌、術後の患者などで、ヘパリンに対する耐性の増加が頻繁に見られます。
c.
薬物相互作用:
ヘパリンロック・フラッシュ・ソリューション(USP)は、静脈注射装置の開存性維持にのみ使用することを目的としているため、複数回投与バイアルに添加物を加えてはいけません。 ヘパリンナトリウムは一段階プロトロンビン時間を延長させる可能性がある。 そのため、ヘパリンナトリウムをジクマロール又はワルファリンナトリウムと併用する場合、有効なプロトロンビン時間を得るためには、最後の静脈内投与から少なくとも5時間以上経過してから採血すること
血小板阻害剤。 アセチルサリチル酸、デキストラン、フェニルブタゾン、イブプロフェン、インドメタシン、ジピリダモール、ヒドロキシクロロキンなど、血小板凝集反応(ヘパリン投与患者の主な止血防御)を阻害する薬剤は出血を誘発することがあり、ヘパリンナトリウム投与患者は慎重に使用しなければならない。
他の相互作用:ヘパリンナトリウム投与患者は血小板凝集反応を阻害する薬剤は使用しないでください。
薬物/実験室相互作用:
高アミノ酸塩血症(Hyperaminotransferasemia)。 ヘパリンを投与された患者(および健康な被験者)の高い割合で、アミノトランスフェラーゼ(SGOTおよびSGPT)値の著しい上昇が起こっています。
発がん性、変異原性、生殖能力障害:
ヘパリンの発がん性を評価するための動物での長期試験は行われていません。
妊娠:
催奇形性作用がある。 妊娠カテゴリーC。ヘパリンナトリウムまたは塩化ナトリウムを用いた動物生殖研究は行われていません。 また、ヘパリンナトリウムまたは塩化ナトリウムを妊婦に投与した場合に胎児に害を与えるか、生殖能力に影響を与えるかどうかはわかっていません。 ヘパリンナトリウムまたは塩化ナトリウムは、明らかに必要な場合にのみ妊婦に投与されるべきです。
非異常性作用。 ヘパリンは胎盤関門を通過しません。
授乳婦:
ヘパリンは母乳中に排泄されません。
小児用:
小児における安全性及び有効性は確立していません。 新生児には使用しない(警告参照)。
老人用:
60歳以上の患者、特に女性で出血の発生率が高いことが報告されています(注意事項、一般的な注意事項参照)。
有害反応
0.5mgの静脈内または皮下注射による有害反応。9%ベンジルアルコールは、ヒトで発生することは知られていないが、数種の動物における0.9%ベンジルアルコールを含む少量の非経口製剤の実験研究では、推定30mLまでの静脈内投与は毒性作用なしに成人に安全に与えられることが示された。 6kgの乳児に推定9mLを投与すると、血圧の変化を引き起こす可能性がある。 ヘパリンロックフラッシュ液は、いかなる局所的または全身的な有害作用も引き起こすことは知られていない。
用法・用量
非経口剤は、投与前に溶液や容器が許す限り、粒子状物質や変色を目視で検査する必要があります。 わずかな変色は効能に影響を与えない。 (ヘパリンロックフラッシュ液、USP10または100USP単位/mLは、単回投与として、静脈留置器と同量の溶液を使用して静脈内注射器に注入される。 静脈留置装置をすぐに使用しない場合は、静脈穿刺後に1回分を注射する。 静脈留置装置を使用して注射、点滴、採血等を行う場合は、ヘパリンロックの効果を回復させるため、1回につきもう1回注射する。 ヘパリン液の量は、静脈留置装置の内腔内での凝固を防ぐのに十分な量(通常0.2~0.3mL以上保持しない)であり、最大24時間まで保持することができる。 ヘパリンと相容れない薬剤を投与するために静脈留置装置を使用する場合、薬剤投与の前後にヘパリンロックセット全体を0.9%塩化ナトリウム注射液(USP)でフラッシュする必要がある。 2回目のフラッシュ後、ヘパリンロックの効果を回復させるために、もう1回ヘパリン溶液を注入すること。 留置装置が分析用血液サンプルの反復採取に使用され、ヘパリン又は生理食塩水の存在が目的の血液検査の結果を妨害又は変更する可能性がある場合、目的の血液サンプルを採取する前に1mLの吸引及び廃棄により留置装置からヘパリン洗浄液を除去すること。 (See PRECAUTIONS.)
How Supplied
Heparin Lock Flush Solution, USP is supplied in the following dosage forms:
| List No. | Dosage Form | Heparin Sodium (USP Units/mL) |
Solution Volume (mL) |
| 0409-1151-12 | LifeShield Plastic Multple-dose Fliptop vial |
10 | 10 |
| 0409-1151-70 | Plastic Mutliple- dose Fliptop vial |
10 | 10 |
| 0409-1151-78 | Plastic Mutliple- dose Fliptop vial |
10 | 30 |
| 0409-1152-14 | LifeShield Plastic Multple-dose Fliptop vial |
100 | 30 |
| 0409-1152-70 | Plastic Mutliple- dose Fliptop vial |
100 | 10 |
| 0409-1152-78 | Plastic Mutliple- dose Fliptop vial |
100 | 30 |
All of the above may be used with sharp needles. In addition, the LifeShield® products may be used with the LifeShield® Blunt Cannula.
Store at 20° to 25°C (68° to 77°F).
Rev: June 2007
EN-1543
Printed in USA
HOSPIRA, INC., LAKE FOREST, IL 60045 USA
Sample Outer Label

| HEPARIN LOCK FLUSH heparin sodium solution |
|||||||||||||
|
|||||||||||||
|
|||||||||||||
|
|||||||||||||
|
|||||||||||||
Labeler – General Injectables & Vaccines, Inc (108250663)
Medical Disclaimer