Generic Name: heparin sodium
Dosage Form: injection, solution
Medically reviewed by Drugs.com. Last updated on February 19, 2021.
- Overview
- Side Effects
- Dosage
- Professional
- Tips
- Interactions
- More
WARNING:
NOT FOR USE IN NEONATES
Description
SOLUTION IS INTENDED FOR MAINTENANCE OF PATENCY OF INTRAVENOUS INJECTION DEVICES ONLY AND IS NOT TO BE USED FOR ANTICOAGULANT THERAPY.
Heparin Lock Flush Solution, USP is a sterile, nonpyrogenic, hypertonic preparation of heparin sodium injection, USP with sodium chloride in water for injection.
Each milliliter (mL) contains: Heparinenatrium, 10 of 100 USP eenheden (afkomstig van varkens darmslijmvlies); natriumchloride 9 mg; edetaatdinatrium, watervrij 0,1 mg toegevoegd als stabilisator; en benzylalcohol 9 mg toegevoegd als conserveermiddel in water voor injectie. Kan natriumhydroxide bevatten voor aanpassing van de pH. pH 6,5 (5,0 tot 7,5). De osmolaire concentraties van deze oplossingen zijn 392 mOsmol/L (calc). Herhaalde afnames kunnen worden gedaan uit de injectieflacon met meerdere doses.
Heparine Lock Flush Solution, USP is uitsluitend bedoeld voor het handhaven van de doorgankelijkheid van intraveneuze injectiehulpmiddelen en mag niet worden gebruikt voor antistollingstherapie.
Heparinenatrium, USP is een heterogene groep van anionische mucopolysachariden met rechte ketens, glycosaminoglycanen genaamd, met antistollingseigenschappen. Hoewel er andere aanwezig kunnen zijn, zijn de voornaamste suikers die in heparine voorkomen (1) a-L-iduronzuur 2-sulfaat, (2) 2-deoxy-2-sulfamino-a-D-glucose 6-sulfaat, (3) b-D-glucuronzuur, (4) 2-acetamido-2-deoxy-a-D-glucose, en (5) a-L-iduronzuur. Deze suikers zijn aanwezig in afnemende hoeveelheden, gewoonlijk in de volgorde (2)groter dan(1)groter dan(4)groter dan(3)groter dan(5), en zijn verbonden door glycosidebindingen, waardoor polymeren van verschillende grootte worden gevormd. Heparine is sterk zuur door zijn gehalte aan covalent verbonden sulfaat- en carboxylzuurgroepen. In heparinenatrium worden de zure protonen van de sulfaateenheden gedeeltelijk vervangen door natriumionen. De werkzaamheid wordt bepaald door een biologische bepaling met behulp van een USP-referentiestandaard op basis van eenheden heparineactiviteit per milligram.
Structuur van heparinenatrium (representatieve subeenheden):
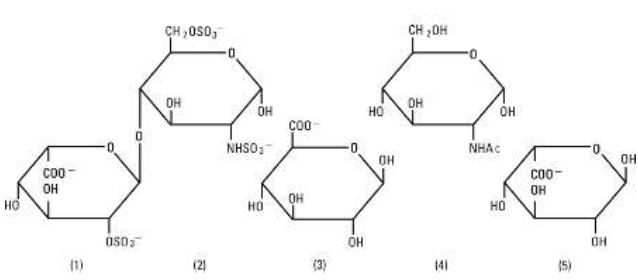
Natriumchloride, USP is chemisch aangeduid als NaCl, een witte kristallijne verbinding die goed oplosbaar is in water. De halfstijve flacons zijn vervaardigd van een speciaal samengestelde polyolefine. Het is een copolymeer van ethyleen en propyleen. De veiligheid van de kunststof is bevestigd door tests op dieren volgens de biologische USP-normen voor kunststof houders. De verpakking vereist
geen dampbarrière om de juiste geneesmiddelconcentratie te handhaven.
Clinische farmacologie
Heparine remt reacties die leiden tot de stolling van bloed en de vorming van fibrinestolsels, zowel in vitro als in vivo. Heparine werkt op meerdere plaatsen in het normale stollingssysteem. Kleine hoeveelheden heparine in combinatie met antitrombine III (heparine-cofactor) kunnen trombose remmen door geactiveerde Factor X te inactiveren en de omzetting van protrombine in trombine te verhinderen. Zodra actieve trombose is ontstaan, kunnen grotere hoeveelheden heparine verdere stolling remmen door trombine te inactiveren en de omzetting van fibrinogeen in fibrine te verhinderen. Heparine verhindert ook de vorming van een stabiele fibrinestolsel door de activering van de fibrinestabiliserende factor te remmen. De bloedingstijd wordt gewoonlijk niet beïnvloed door heparine. De stollingstijd wordt verlengd door volledige therapeutische doses heparine; in de meeste gevallen wordt deze niet meetbaar beïnvloed door lage doses heparine. Patiënten ouder dan 60 jaar kunnen na vergelijkbare doses heparine hogere plasmaspiegels van heparine en langere geactiveerde partiële tromboplastinetijden (APTT’s) hebben in vergelijking met patiënten jonger dan 60 jaar. De piekplasmaspiegels van heparine worden 2 tot 4 uur na subcutane toediening bereikt, hoewel er aanzienlijke individuele variaties zijn. Loglineaire plotten van heparine plasmaconcentraties met tijd voor een breed scala van dosisniveaus zijn lineair, hetgeen de afwezigheid van nul-orde processen suggereert. De lever en het reticulo-endotheliale systeem zijn de plaatsen waar de biotransformatie plaatsvindt. De bifasische eliminatiecurve, een snel dalende alfa-fase (t½ =10#) en na het 40e levensjaar een langzamere bèta-fase, wijst op opname in organen. Het ontbreken van een verband tussen de antistollingshalfwaardetijd en de concentratie van de halfwaardetijd kan te wijten zijn aan factoren zoals de eiwitbinding van heparine. Heparine heeft geen fibrinolytische activiteit; daarom zal het bestaande stolsels niet doen lyseren. Heparine Lock Flush Solution induceert geen systemische antistollingswerking bij eenmalige doses van 10 of 100 USP eenheden per ml wanneer het wordt gebruikt voor het handhaven van de patency van intraveneuze injectieapparaten. Het kan interfereren met laboratoriumtests op bloedmonsters die uit dergelijke hulpmiddelen worden genomen, tenzij het volume in situ heparine-zout, gelijk aan dat van het primingvolume van de katheter, wordt opgezogen en weggegooid voordat dergelijke monsters worden genomen. Isotone concentraties van natriumchloride zijn geschikt voor parenterale vervanging van chlorideverliezen die groter zijn dan of gelijk zijn aan het natriumverlies. Hypotone concentraties van natriumchloride zijn geschikt voor parenteraal onderhoud van de waterbehoefte wanneer slechts kleine hoeveelheden zout gewenst zijn.
Natriumchloride in water dissocieert en levert natrium- (Na+) en chloride- (Cl-) ionen. Natrium (Na+) is het belangrijkste kation van de extracellulaire vloeistof en speelt een grote rol bij de behandeling van vocht- en elektrolytstoornissen. Chloride (Cl-) speelt een integrale rol in de bufferende werking bij de uitwisseling van zuurstof en kooldioxide in de rode bloedcellen. De distributie en uitscheiding van natrium (Na+) worden grotendeels gecontroleerd door de nieren, die een evenwicht handhaven tussen inname en uitvoer. Het kleine volume vloeistof en de hoeveelheid natriumchloride die worden geleverd door Heparin Lock Flush Solution, USP, wanneer uitsluitend gebruikt als een middel om de doorgankelijkheid van een intraveneus injectieapparaat te handhaven, zal waarschijnlijk geen significant effect hebben op de vloeistof- en elektrolytenbalans, behalve mogelijk bij zeer kleine zuigelingen.
Indicaties en gebruik
Heparin Lock Flush Solution, USP is uitsluitend geïndiceerd om de doorgankelijkheid van een intraveneus injectieapparaat te handhaven. Het kan worden gebruikt na de eerste plaatsing van het apparaat in de ader, na elke injectie van een geneesmiddel of na afname van bloed voor laboratoriumonderzoek. De oplossing mag niet worden gebruikt voor antistollingstherapie.
Contra-indicaties
In verband met de mogelijke toxiciteit van benzylalcohol bij pasgeborenen mogen oplossingen die benzylalcohol bevatten niet worden gebruikt bij deze patiëntenpopulatie. Parenterale bereidingen met benzylalcohol mogen niet worden gebruikt voor vloeistof- of natriumchloridevervanging. Heparinenatrium mag niet worden gebruikt bij patiënten: Met overgevoeligheid voor heparine; Met een oncontroleerbare actieve bloedingstoestand (zie WAARSCHUWINGEN), behalve wanneer dit te wijten is aan gedissemineerde intravasale stolling; Met onvermogen om geschikte bloedstollingstests uit te voeren, bv. volbloedstollingstijd, partiële tromboplastinetijd, enz. met de vereiste intervallen. Het is gewoonlijk niet nodig om het effect van laaggedoseerde heparine te controleren bij patiënten met normale stollingsparameters.
Waarschuwingen
Benzylalcohol, een conserveermiddel in de multiple-dose flaconpreparaten van Heparin Lock Flush Solution, USP is in verband gebracht met toxiciteit bij neonaten. Benzylalcohol is in verband gebracht met een foetaal “hijgsyndroom” bij premature zuigelingen. Er zijn geen gegevens beschikbaar over de toxiciteit van andere conserveermiddelen in deze leeftijdsgroep. Heparine Lock Flush Solution, USP zonder conserveermiddel moet worden gebruikt om de doorgankelijkheid van intraveneuze injectieapparatuur bij pasgeborenen te handhaven. Heparin Lock Flush Solution, USP is niet bestemd voor intramusculair gebruik, systemische antistolling of injectie via enige parenterale toedieningsweg.
Hypersensitiviteit: Patiënten met gedocumenteerde overgevoeligheid voor heparine mogen het middel alleen in duidelijk levensbedreigende situaties toegediend krijgen.
Bloedingen: Bloedingen kunnen op vrijwel elke plaats optreden bij patiënten die heparine krijgen. Bij een onverklaarbare daling van het hematocriet, een daling van de bloeddruk of een ander onverklaarbaar symptoom moet ernstig rekening worden gehouden met een hemorragisch voorval. Heparinenatrium dient met uiterste voorzichtigheid te worden gebruikt bij ziektetoestanden waarbij er een verhoogd gevaar is voor bloedingen. Enkele aandoeningen waarbij een verhoogd gevaar op bloedingen bestaat zijn:
Cardiovasculair- Subacute bacteriële endocarditis. Ernstige hypertensie.
Chirurgisch- Tijdens en direct na (a) een ruggenprik of spinale anesthesie of (b) een grote operatie, met name van de hersenen, het ruggenmerg of het oog.
Hematologisch- Aandoeningen die gepaard gaan met een verhoogde bloedingsneiging, zoals hemofilie, trombocytopenie en sommige vasculaire purpura’s.
Gastro-intestinaal – Ulceratieve laesies en continue buisdrainage van de maag of dunne darm.
Overig- Menstruatie, leverziekte met gestoorde hemostase.
Coagulatietest: Als de stollingstest onnodig wordt verlengd of als een bloeding optreedt, moet heparinenatrium onmiddellijk worden gestaakt. Heparineoplossingen met een concentratie van 10 USP Heparine-eenheden/ml kunnen de resultaten van bloedstollingstests veranderen. Heparineconcentraties hoger dan 10 USP Heparine-eenheden/ml kunnen de resultaten van bloedstollingstests veranderen.
Thrombocytopenie: Trombocytopenie is gemeld bij patiënten die heparine krijgen met een gerapporteerde incidentie van 0 tot 30%. Milde trombocytopenie (aantal groter dan 100.000/mm3) kan stabiel blijven of omkeren, zelfs als de heparine wordt voortgezet. Trombocytopenie van elke graad moet echter nauwlettend in de gaten worden gehouden. Als het aantal daalt tot onder 100.000/mm3 of als zich recidiverende trombose
ontwikkelt (zie Witte stolsyndroom, VOORZORGSMAATREGELEN), dient het heparineproduct te worden gestaakt. Indien voortzetting van de heparinetherapie noodzakelijk is, kan de toediening van heparine uit een andere orgaanbron met voorzichtigheid worden hervat. Natriumionen bevattende oplossingen dienen met grote voorzichtigheid te worden gebruikt, indien überhaupt, bij patiënten met congestief hartfalen, ernstige nierinsufficiëntie en in klinische toestanden waarin sprake is van oedeem met natriumretentie.
Voorzorgsmaatregelen
Niet gebruiken tenzij de oplossing helder is en de verpakking onbeschadigd is. Gebruik aseptische techniek voor enkelvoudige of meervoudige in- en uitname uit alle containers. Aangezien heparinenatrium in dit product afkomstig is van dierlijk weefsel, moet het met voorzichtigheid worden gebruikt bij patiënten met een voorgeschiedenis van allergie.
Storing van laboratoriumtests
Heparine stoort de concurrerende eiwitbindingsmethoden voor serumthyroxinebepalingen, wat leidt tot foutief verhoogde waarden. Heparine Lock Flush Solution kan interfereren met laboratoriumanalyses of de resultaten van bloedchemische tests zoals glucose, serumnatrium en serumchloride, bloedstollingsonderzoek, enz. wijzigen. (Zie KLINISCHE FARMACOLOGIE.) De volgende informatie die betrekking heeft op het gebruik van heparine-natrium als systemisch antistollingsmiddel is slechts opgenomen ter informatie, aangezien het niet bekend is of deze van toepassing is op het gebruik van het geneesmiddel voor heparineslot.
Algemeen:
a. Witte-klonter-syndroom:
Er is gerapporteerd dat patiënten die heparine gebruiken nieuwe trombusvorming kunnen ontwikkelen in samenhang met trombocytopenie als gevolg van irreversibele aggregatie van bloedplaatjes geïnduceerd door heparine, het zogenaamde “witte-klonter-syndroom”. Dit proces kan leiden tot ernstige trombo-embolische complicaties zoals huidnecrose, gangreen van de ledematen dat kan leiden tot amputatie, myocardinfarct, longembolie, beroerte, en mogelijk overlijden. Daarom moet de toediening van heparine onmiddellijk worden gestaakt als een patiënt nieuwe trombose ontwikkelt in combinatie met trombocytopenie.
b. Heparineresistentie:
Verhoogde resistentie tegen heparine komt vaak voor bij koorts, trombose, tromboflebitis, infecties met tromboserende neigingen, myocardinfarct, kanker en bij postoperatieve patiënten.
c. Verhoogd risico bij oudere patiënten, vooral vrouwen:
Er is een hogere incidentie van bloedingen gemeld bij patiënten, vooral vrouwen, ouder dan 60 jaar.
Gewrichtsinteracties:
Aangezien Heparine Lock Flush Solution, USP alleen bedoeld is voor gebruik bij het handhaven van de doorgankelijkheid van intraveneuze injectiehulpmiddelen, mogen er geen toevoegingen worden gedaan aan injectieflacons met meerdere doses.
Oral anticoagulantia: Heparinenatrium kan de éénfase protrombinetijd verlengen. Daarom moet, wanneer heparinenatrium samen met dicumarol of warfarinenatrium wordt gegeven, een periode van ten minste 5 uur na de laatste intraveneuze dosis verstrijken voordat bloed wordt afgenomen, wil een geldige PROTHROMBIN-tijd worden verkregen.
Plateletremmers: Geneesmiddelen zoals acetylsalicylzuur, dextran, fenylbutazon, ibuprofen, indomethacine, dipyridamol, hydroxychloroquine en andere die interfereren met plaatjesaggregatiereacties (de belangrijkste hemostatische verdediging van heparininiserende patiënten) kunnen bloedingen induceren en moeten met voorzichtigheid worden gebruikt bij patiënten die heparinenatrium krijgen.
Andere interacties: Digitalis, tetracyclines, nicotine, anti-histaminica of I.V. nitroglycerine kunnen de antistollingswerking van heparinenatrium gedeeltelijk teniet doen.
Geneesmiddelen/laboratoriuminteracties:
Hyperaminotransferasemie: Significante verhogingen van de aminotransferasespiegel (SGOT en SGPT ) zijn opgetreden bij een hoog percentage patiënten (en gezonde personen) die heparine hebben gekregen. Aangezien aminotransferasebepalingen belangrijk zijn bij de differentiële diagnose van myocardinfarct, leveraandoeningen en longembolie, moeten stijgingen die veroorzaakt kunnen zijn door geneesmiddelen (zoals heparine) met voorzichtigheid worden geïnterpreteerd.
Carcinogenese, mutagenese, verminderde vruchtbaarheid:
Er zijn geen langetermijnstudies bij dieren uitgevoerd om het carcinogene potentieel van heparine te evalueren. Ook zijn er geen reproductiestudies bij dieren uitgevoerd naar mutagenese of verminderde vruchtbaarheid.
Zwangerschap:
Teratogene effecten: Zwangerschapscategorie C. Er zijn geen reproductiestudies bij dieren uitgevoerd met heparine-natrium of natriumchloride. Het is ook niet bekend of heparinenatrium of natriumchloride schade aan de foetus kan toebrengen bij toediening aan een zwangere vrouw of het voortplantingsvermogen kan beïnvloeden. Heparinenatrium of natriumchloride mag alleen aan een zwangere vrouw worden gegeven als dit duidelijk nodig is.
Nonteratogene effecten: Heparine passeert de placentabarrière niet.
Voedende moeders:
Heparine wordt niet uitgescheiden in de moedermelk.
Pediatrisch gebruik:
Veiligheid en werkzaamheid bij pediatrische patiënten zijn niet vastgesteld. Niet gebruiken bij pasgeborenen (zie WAARSCHUWINGEN).
Geriatrisch gebruik:
Er is een hogere incidentie van bloedingen gemeld bij patiënten ouder dan 60 jaar, vooral bij vrouwen (zie VOORZORGSMAATREGELEN, Algemeen). Uit klinisch onderzoek blijkt dat bij deze patiënten lagere doses heparine aangewezen kunnen zijn (zie CLINICAL PHARMACOLOGY en DOSAGE AND ADMINISTRATION).
Adverse Reactions
Hoewel bijwerkingen van intraveneuze intramusculaire of subcutane injectie van 0.9% benzylalcohol bij de mens niet voorkomen, hebben experimentele studies van parenterale preparaten met een klein volume 0,9% benzylalcohol bij verschillende diersoorten aangetoond dat een geschatte intraveneuze dosis tot 30 ml veilig aan een volwassene kan worden toegediend zonder toxische effecten. Toediening van een geschatte 9 ml aan een zuigeling van 6 kg kan mogelijk bloeddrukveranderingen veroorzaken. Heparine Lock Flush Solution veroorzaakt, voor zover bekend, geen schadelijke lokale of systemische effecten. Hoewel de mogelijkheid van een overgevoeligheidsreactie bestaat bij het in de circulatie brengen van extreem kleine subtherapeutische hoeveelheden van de oplossing, is een dergelijk voorval niet gerapporteerd.
Dosering en toediening
Parenterale geneesmiddelen dienen vóór toediening visueel te worden geïnspecteerd op deeltjes en verkleuring, wanneer de oplossing en de verpakking dit toelaten. Lichte verkleuring verandert de werkzaamheid niet. (Zie VOORZORGSMAATREGELEN.) Heparine Lock Flush Solution, USP 10 of 100 USP eenheden/ml, wordt als een eenmalige dosis geïnjecteerd in een intraveneus injectieapparaat met een volume van de oplossing dat gelijk is aan dat van het intraveneuze venapunctieapparaat. Een eenmalige dosis moet worden geïnjecteerd na venapunctie wanneer het verblijfsapparaat niet onmiddellijk moet worden gebruikt. Na elk gebruik
van het verblijfsondersteunende venapunctieapparaat voor injectie of infusie van medicatie, of afname van bloedmonsters, moet een nieuwe dosis worden geïnjecteerd om de effectiviteit van het heparineslot te herstellen. De hoeveelheid heparineoplossing is voldoende om stolling binnen het lumen van verblijfsapparaten voor veneuze punctie te voorkomen (gewoonlijk niet meer dan 0,2 tot 0,3 ml) gedurende maximaal vierentwintig uur. Wanneer het verblijfsapparaat wordt gebruikt voor de toediening van een geneesmiddel dat niet verenigbaar is met heparine, moet de gehele heparineslotset vóór en na de toediening van het geneesmiddel worden gespoeld met 0,9% natriumchloride-injectie, USP. Na de tweede spoeling moet een nieuwe dosis heparineoplossing worden geïnjecteerd om de effectiviteit van het heparineslot te herstellen. Wanneer het verblijfslichaam wordt gebruikt voor herhaalde afname van bloedmonsters voor laboratoriumanalyses en het waarschijnlijk is dat de aanwezigheid van heparine of zoutoplossing de resultaten van de gewenste bloedtesten verstoort of wijzigt, moet de in situ heparinespoelingoplossing uit het verblijfslichaam worden verwijderd door 1 ml op te zuigen en weg te gooien voordat het gewenste bloedmonster wordt afgenomen. (See PRECAUTIONS.)
How Supplied
Heparin Lock Flush Solution, USP is supplied in the following dosage forms:
| List No. | Dosage Form | Heparin Sodium (USP Units/mL) |
Solution Volume (mL) |
| 0409-1151-12 | LifeShield Plastic Multple-dose Fliptop vial |
10 | 10 |
| 0409-1151-70 | Plastic Mutliple- dose Fliptop vial |
10 | 10 |
| 0409-1151-78 | Plastic Mutliple- dose Fliptop vial |
10 | 30 |
| 0409-1152-14 | LifeShield Plastic Multple-dose Fliptop vial |
100 | 30 |
| 0409-1152-70 | Plastic Mutliple- dose Fliptop vial |
100 | 10 |
| 0409-1152-78 | Plastic Mutliple- dose Fliptop vial |
100 | 30 |
All of the above may be used with sharp needles. In addition, the LifeShield® products may be used with the LifeShield® Blunt Cannula.
Store at 20° to 25°C (68° to 77°F).
Rev: June 2007
EN-1543
Printed in USA
HOSPIRA, INC., LAKE FOREST, IL 60045 USA
Sample Outer Label

| HEPARIN LOCK FLUSH heparin sodium solution |
|||||||||||||
|
|||||||||||||
|
|||||||||||||
|
|||||||||||||
|
|||||||||||||
Labeler – General Injectables & Vaccines, Inc (108250663)
Medical Disclaimer