Generic Name: heparin sodium
Dosage Form: injection, solution
Medically reviewed by Drugs.com. Last updated on February 19, 2021.
- Overview
- Side Effects
- Dosage
- Professional
- Tips
- Interactions
- More
WARNING:
NOT FOR USE IN NEONATES
Description
SOLUTION IS INTENDED FOR MAINTENANCE OF PATENCY OF INTRAVENOUS INJECTION DEVICES ONLY AND IS NOT TO BE USED FOR ANTICOAGULANT THERAPY.
Heparin Lock Flush Solution, USP is a sterile, nonpyrogenic, hypertonic preparation of heparin sodium injection, USP with sodium chloride in water for injection.
Each milliliter (mL) contains: Obsahuje: heparin sodný, 10 nebo 100 jednotek USP (získaný z prasečí střevní sliznice); chlorid sodný 9 mg; edetát disodný, bezvodý 0,1 mg přidaný jako stabilizátor; a benzylalkohol 9 mg přidaný jako konzervační látka ve vodě na injekci. Může obsahovat hydroxid sodný pro úpravu pH. pH 6,5 (5,0 až 7,5). Osmolární koncentrace těchto roztoků je 392 mOsmol/l (calc). Z vícedávkové lahvičky lze opakovaně odebírat.
Heparin Lock Flush Solution, USP je určen pouze k udržování průchodnosti intravenózních injekčních zařízení a nemá se používat k antikoagulační léčbě.
Heparin Sodium, USP je heterogenní skupina aniontových mukopolysacharidů s přímým řetězcem, tzv. glykosaminoglykanů, které mají antikoagulační vlastnosti. Ačkoli mohou být přítomny i další, hlavními cukry vyskytujícími se v heparinu jsou: (1) 2-sulfát kyseliny a-L-iduronové, (2) 2-deoxy-2-sulfamino-a-D-glukosa 6-sulfát, (3) kyselina b-D-glukuronová, (4) 2-acetamido-2-deoxy-a-D-glukosa a (5) kyselina a-L-iduronová. Tyto cukry jsou přítomny v klesajícím množství, obvykle v pořadí (2) větší než (1) větší než (4) větší než (3) větší než (5), a jsou spojeny glykosidickými vazbami, které tvoří polymery různých velikostí. Heparin je silně kyselý, protože obsahuje kovalentně vázané sulfátové a karboxylové skupiny. V heparinu sodném jsou kyselé protony sulfátových jednotek částečně nahrazeny sodnými ionty. Účinnost se stanovuje biologickým testem pomocí referenčního standardu USP na základě jednotek aktivity heparinu na miligram.
Struktura heparinu sodného (reprezentativní podjednotky):
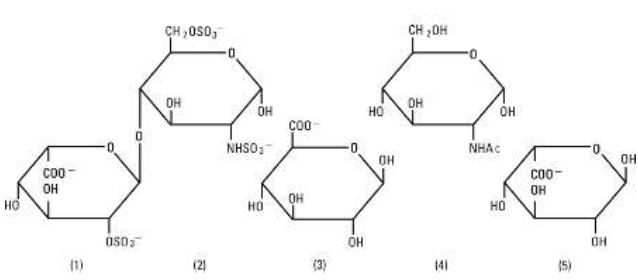
Chlorid sodný, USP je chemicky označován NaCl, bílá krystalická sloučenina volně rozpustná ve vodě. Polotuhé lahvičky jsou vyrobeny ze speciálně upraveného polyolefinu. Jedná se o kopolymer ethylenu a propylenu. Bezpečnost tohoto plastu byla potvrzena testy na zvířatech podle biologických norem USP pro plastové nádoby. Nádobka nevyžaduje
žádnou parotěsnou zábranu, aby se udržela správná koncentrace léčiva.
Klinická farmakologie
Heparin inhibuje reakce, které vedou ke srážení krve a tvorbě fibrinových sraženin jak in vitro, tak in vivo. Heparin působí na více místech normálního koagulačního systému. Malá množství heparinu v kombinaci s antitrombinem III (heparinový kofaktor) mohou inhibovat trombózu tím, že inaktivují aktivovaný faktor X a inhibují přeměnu protrombinu na trombin. Po vzniku aktivní trombózy může větší množství heparinu inhibovat další koagulaci inaktivací trombinu a zabráněním přeměny fibrinogenu na fibrin. Heparin také brání vzniku stabilní fibrinové sraženiny tím, že inhibuje aktivaci fibrin stabilizujícího faktoru. Doba krvácení není obvykle heparinem ovlivněna. Čas srážení se prodlužuje plnými terapeutickými dávkami heparinu; ve většině případů není měřitelně ovlivněn nízkými dávkami heparinu. Pacienti starší 60 let mohou mít po podání podobných dávek heparinu vyšší plazmatické hladiny heparinu a delší aktivovaný parciální tromboplastinový čas (APTT) než pacienti mladší 60 let. Vrcholových plazmatických hladin heparinu je dosaženo za 2 až 4 hodiny po subkutánním podání, i když existují značné individuální rozdíly. Loglineární grafy plazmatických koncentrací heparinu s časem pro širokou škálu dávek jsou lineární, což naznačuje nepřítomnost procesů nultého řádu. Místem biotransformace jsou játra a retikuloendoteliální systém. Dvoufázová eliminační křivka, rychle klesající alfa fáze (t½ =10#) a po 40. roce věku pomalejší beta fáze, ukazuje na absorpci v orgánech. Absence vztahu mezi poločasem antikoagulancia a koncentrací poločasu může odrážet faktory, jako je vazba heparinu na bílkoviny. Heparin nemá fibrinolytickou aktivitu, proto nelyzuje existující sraženiny. Heparin Lock Flush Solution nevyvolává systémový antikoagulační účinek v jednotlivých dávkách 10 nebo 100 USP jednotek na ml, pokud se používá k udržení průchodnosti intravenózních injekčních zařízení. Může interferovat s laboratorními testy vzorků krve odebraných z těchto zařízení, pokud není před odběrem těchto vzorků odsát a zlikvidován objem heparin-salinu in situ, který se rovná objemu zálivky katétru. Izotonické koncentrace chloridu sodného jsou vhodné pro parenterální náhradu ztrát chloridů, které jsou vyšší nebo stejné jako ztráty sodíku. Hypotonické koncentrace chloridu sodného jsou vhodné pro parenterální udržování potřeby vody, pokud je požadováno pouze malé množství soli.
Chlorid sodný ve vodě disociuje za vzniku sodíkových (Na+) a chloridových (Cl-) iontů. Sodík (Na+) je hlavním kationtem
extracelulární tekutiny a hraje velkou roli v terapii poruch tekutin a elektrolytů. Chlorid (Cl-) má nedílnou úlohu v pufrovacím působení při výměně kyslíku a oxidu uhličitého v červených krvinkách. Distribuce a vylučování sodíku (Na+) jsou do značné míry pod kontrolou ledvin, které udržují rovnováhu mezi příjmem a výdejem. Malý objem tekutiny a množství chloridu sodného poskytované přípravkem Heparin Lock Flush Solution, USP, pokud se používá pouze jako vehikulum pro udržení průchodnosti intravenózního injekčního zařízení, pravděpodobně nebude mít významný vliv na rovnováhu tekutin a elektrolytů, s výjimkou možná velmi malých kojenců.
Indikace a použití
Heparin Lock Flush Solution, USP je indikován pouze k udržení průchodnosti intravenózního injekčního zařízení. Může být použit po prvním umístění zařízení do žíly, po každé injekci léku nebo po odběru krve na laboratorní analýzu. Roztok se nesmí používat k antikoagulační léčbě.
Kontraindikace
Vzhledem k možné toxicitě benzylalkoholu u novorozenců se roztoky obsahující benzylalkohol nesmí u této populace pacientů používat. Parenterální přípravky s benzylalkoholem se nesmí používat k náhradě tekutin nebo chloridu sodného. Heparin sodný se u pacientů nesmí používat: s přecitlivělostí na heparin; s nekontrolovatelným stavem aktivního krvácení (viz VAROVÁNÍ), s výjimkou případů, kdy je způsobeno diseminovanou intravaskulární koagulací; s neschopností provádět v požadovaných intervalech vhodné testy krevní srážlivosti, např. čas srážení plné krve, parciální tromboplastinový čas atd. U pacientů s normálními koagulačními parametry obvykle není třeba sledovat účinek nízkých dávek heparinu.
Upozornění
Benzylalkohol, konzervační látka v přípravcích Heparin Lock Flush Solution, USP ve vícedávkových lahvičkách, byl spojován s toxicitou u novorozenců. Bylo hlášeno, že benzylalkohol je spojován se „syndromem lapání po dechu“ u plodu u předčasně narozených dětí. Údaje o toxicitě jiných konzervačních látek u této věkové skupiny nejsou k dispozici. K udržení průchodnosti intravenózních injekčních zařízení u novorozenců by se měl používat Heparin Lock Flush Solution, USP bez konzervačních látek. Heparin Lock Flush Solution, USP není určen k intramuskulárnímu použití, systémové antikoagulaci ani k injekčnímu podání jakoukoli parenterální cestou.
Přecitlivělost: Pacientům s dokumentovanou přecitlivělostí na heparin by měl být přípravek podáván pouze v případech zjevného ohrožení života.
Krvácení: U pacientů, kteří dostávají heparin, může dojít ke krvácení prakticky na kterémkoli místě. Nevysvětlitelný pokles hematokritu, pokles krevního tlaku nebo jakýkoli jiný nevysvětlitelný příznak by měl vést k vážnému zvážení krvácivé příhody. Heparin sodný by měl být používán s mimořádnou opatrností u chorobných stavů, u kterých je zvýšené nebezpečí krvácení. Některé ze stavů, u kterých existuje zvýšené nebezpečí krvácení, jsou:
Kardiovaskulární- Subakutní bakteriální endokarditida. Těžká hypertenze.
Chirurgické- Během a bezprostředně po (a) spinální punkci nebo spinální anestezii nebo (b) velkém chirurgickém zákroku, zejména v oblasti mozku, míchy nebo oka.
Hematologické- Stavy spojené se zvýšenou tendencí ke krvácení, jako je hemofilie, trombocytopenie a některé cévní purpury.
Gastrointestinální – Vředové léze a kontinuální drenáž žaludku nebo tenkého střeva sondou.
Ostatní- Menstruace, onemocnění jater s poruchou hemostázy.
Koagulační vyšetření: Pokud je koagulační test nepřiměřeně prodloužen nebo pokud dojde ke krvácení, je třeba podávání heparinu sodného neprodleně přerušit. Roztoky heparinu o koncentraci 10 USP heparinových jednotek/ml mohou změnit výsledky krevních koagulačních testů. Koncentrace heparinu vyšší než 10 USP heparinových jednotek/ml změní výsledky testů krevní srážlivosti.
Trombocytopenie: U pacientů užívajících heparin byl hlášen výskyt trombocytopenie s udávanou incidencí 0 až 30 %. Mírná trombocytopenie (počet vyšší než 100 000/mm3) může zůstat stabilní nebo se zvrátit i při pokračování podávání heparinu. Trombocytopenie jakéhokoli stupně by však měla být pečlivě sledována. Pokud počet klesne pod 100 000/mm3 nebo pokud se objeví recidivující trombóza
(viz Syndrom bílých krvinek, OPATŘENÍ), je třeba heparinový přípravek vysadit. Pokud je pokračování léčby heparinem nezbytné, lze s opatrností obnovit podávání heparinu z jiného orgánového zdroje. Roztoky obsahující sodíkové ionty by měly být používány s velkou opatrností, pokud vůbec, u pacientů s městnavým srdečním selháním, těžkou renální insuficiencí a u klinických stavů, při kterých existuje edém s retencí sodíku.
Preventivní opatření
Nepoužívejte, pokud roztok není čirý a obal není poškozen. Používejte aseptickou techniku pro jednorázový nebo vícenásobný vstup a odběr ze všech nádob. Vzhledem k tomu, že sodná sůl heparinu v tomto přípravku pochází ze zvířecí tkáně, měla by být používána s opatrností u pacientů s alergií v anamnéze.
Interference s laboratorními testy
Heparin interferuje s metodami kompetitivní vazby proteinů pro stanovení tyroxinu v séru, což vede k falešně zvýšeným hladinám. Heparin Lock Flush Solution může interferovat s laboratorními analýzami nebo měnit výsledky krevních chemických testů, jako je stanovení glukózy, sodíku a chloridů v séru, vyšetření krevní srážlivosti atd. (Viz KLINICKÁ FARMAKOLOGIE.) Následující informace, které se týkají použití sodné soli heparinu jako systémového antikoagulancia, jsou uvedeny pouze pro zajímavost, protože není známo, že by se vztahovaly na použití přípravku pro heparinový zámek.
Všeobecně:
a. Syndrom bílé sraženiny:
Bylo hlášeno, že u pacientů užívajících heparin může dojít k tvorbě nových trombů v souvislosti s trombocytopenií v důsledku ireverzibilní agregace trombocytů vyvolané heparinem, tzv. syndromu bílé sraženiny. Tento proces může vést k závažným tromboembolickým komplikacím, jako je nekróza kůže, gangréna končetin, která může vést k amputaci, infarkt myokardu, plicní embolie, mozková mrtvice a případně i smrt. Proto by mělo být podávání heparinu neprodleně přerušeno, pokud se u pacienta objeví nová trombóza v souvislosti s trombocytopenií.
b. Rezistence na heparin:
Se zvýšenou rezistencí na heparin se často setkáváme při horečce, trombóze, tromboflebitidě, infekcích s trombotizující tendencí, infarktu myokardu, rakovině a u pacientů po operaci.
c. Zvýšené riziko u starších pacientů, zejména žen:
U pacientů, zejména žen, starších 60 let byl hlášen vyšší výskyt krvácení.
Lékové interakce:
Jelikož je Heparin Lock Flush Solution, USP určen pouze k použití pro udržení průchodnosti intravenózních injekčních zařízení, neměly by se do vícedávkových lahviček přidávat žádné přísady.
Orální antikoagulancia: Heparin sodný může prodloužit jednostupňový protrombinový čas. Proto pokud je heparin sodný podáván s dikumarolem nebo warfarinem sodným, měla by před odběrem krve uplynout doba nejméně 5 hodin od poslední intravenózní dávky, pokud má být získán platný PROTHROMBINOVÝ čas.
Inhibitory destiček: Léky jako kyselina acetylsalicylová, dextran, fenylbutazon, ibuprofen, indometacin, dipyridamol, hydroxychlorochin a další, které interferují s reakcemi agregace krevních destiček (hlavní hemostatická obrana heparinizovaných pacientů), mohou vyvolat krvácení a měly by být u pacientů užívajících heparin sodný používány s opatrností.
Jiné interakce: Digitalis, tetracykliny, nikotin, antihistaminika nebo nitroglycerin podávaný nitrožilně mohou částečně působit proti antikoagulačnímu účinku heparinu sodného.
Lékové/laboratorní interakce:
Hyperaminotransferázie: U vysokého procenta pacientů (a zdravých osob), kteří dostávali heparin, došlo k významnému zvýšení hladin aminotransferáz (SGOT a SGPT ). Vzhledem k tomu, že stanovení aminotransferáz je důležité v diferenciální diagnostice infarktu myokardu, jaterních onemocnění a plicní embolie, je třeba vzestupy, které by mohly být způsobeny léky (jako je heparin), interpretovat s opatrností.
Karcinogeneze, mutageneze, poškození fertility:
Nebyly provedeny žádné dlouhodobé studie na zvířatech, které by hodnotily karcinogenní potenciál heparinu. Rovněž nebyly provedeny žádné reprodukční studie na zvířatech týkající se mutageneze nebo poškození fertility.
Těhotenství:
Teratogenní účinky: Kategorie těhotenství C. Reprodukční studie na zvířatech nebyly s heparinem sodným ani chloridem sodným prováděny. Rovněž není známo, zda heparin sodný nebo chlorid sodný může při podání těhotným ženám způsobit poškození plodu nebo zda může ovlivnit reprodukční schopnost. Heparin sodný nebo chlorid sodný by měl být podáván těhotné ženě pouze v případě, že je to jednoznačně nutné.
Nonteratogenní účinky: Heparin neprochází placentární bariérou.
Kojící matky:
Heparin se nevylučuje do lidského mléka.
Pediatrické použití:
Bezpečnost a účinnost u pediatrických pacientů nebyla stanovena. Není určen pro použití u novorozenců (viz UPOZORNĚNÍ).
Geriatrické použití:
U pacientů starších 60 let, zejména u žen, byl hlášen vyšší výskyt krvácení (viz PRECAUTIONS, General). Klinické studie naznačují, že u těchto pacientů mohou být indikovány nižší dávky heparinu (viz KLINICKÁ FARMAKOLOGIE a DÁVKOVÁNÍ A PODÁVÁNÍ).
Nežádoucí účinky
Ačkoli nežádoucí reakce na intravenózní intramuskulární nebo subkutánní injekci 0.9% benzylalkoholu nejsou u člověka známy, experimentální studie malých objemů parenterálních přípravků obsahujících 0,9% benzylalkohol u několika druhů zvířat ukázaly, že odhadovaná intravenózní dávka do 30 ml může být bezpečně podána dospělému člověku bez toxických účinků. Podání odhadované dávky 9 ml kojenci o hmotnosti 6 kg je potenciálně schopno vyvolat změny krevního tlaku. Není známo, že by Heparin Lock Flush Solution způsoboval jakékoliv nežádoucí lokální nebo systémové účinky. Ačkoli existuje vzdálená možnost reakce z přecitlivělosti při vniknutí extrémně malého subterapeutického množství roztoku do oběhu, takový výskyt nebyl hlášen.
Dávkování a způsob podání
Parenterální léčivé přípravky by měly být před podáním vizuálně zkontrolovány na přítomnost částic a změnu barvy, kdykoli to roztok a obal dovolí. Mírná změna barvy nemění účinnost. (Viz PRECAUTIONS.) Heparin Lock Flush Solution, USP 10 nebo 100 USP jednotek/ml se podává jako jednotlivá dávka do nitrožilního injekčního zařízení s použitím objemu roztoku odpovídajícího objemu nitrožilního venepunkčního zařízení. Jednorázová dávka by měla být vstříknuta po venepunkci, pokud nemá být indovenční zařízení použito okamžitě. Po každém použití
vnitřního venepunkčního zařízení pro injekci nebo infuzi léků nebo odběr krevních vzorků by měla být vstříknuta další dávka, aby se obnovila účinnost heparinového zámku. Množství roztoku heparinu je dostatečné k zabránění srážení krve v lumen indovenčního zařízení (obvykle se neudrží více než 0,2 až 0,3 ml) po dobu až 24 hodin. Pokud se indovenční zařízení používá k podávání léku, který je inkompatibilní s heparinem, měla by se celá souprava heparinového zámku před podáním léku a po něm propláchnout 0,9% injekčním chloridem sodným, USP. Po druhém propláchnutí by měla být podána další dávka roztoku heparinu, aby se obnovila účinnost heparinového zámku. Pokud se indikační zařízení používá k opakovaným odběrům vzorků krve pro laboratorní analýzy a je pravděpodobné, že přítomnost heparinu nebo fyziologického roztoku bude interferovat s výsledky požadovaných krevních testů nebo je změní, měl by se proplachovací roztok heparinu in situ ze zařízení odstranit odsátím a vyhozením 1 ml před odběrem požadovaného vzorku krve. (See PRECAUTIONS.)
How Supplied
Heparin Lock Flush Solution, USP is supplied in the following dosage forms:
| List No. | Dosage Form | Heparin Sodium (USP Units/mL) |
Solution Volume (mL) |
| 0409-1151-12 | LifeShield Plastic Multple-dose Fliptop vial |
10 | 10 |
| 0409-1151-70 | Plastic Mutliple- dose Fliptop vial |
10 | 10 |
| 0409-1151-78 | Plastic Mutliple- dose Fliptop vial |
10 | 30 |
| 0409-1152-14 | LifeShield Plastic Multple-dose Fliptop vial |
100 | 30 |
| 0409-1152-70 | Plastic Mutliple- dose Fliptop vial |
100 | 10 |
| 0409-1152-78 | Plastic Mutliple- dose Fliptop vial |
100 | 30 |
All of the above may be used with sharp needles. In addition, the LifeShield® products may be used with the LifeShield® Blunt Cannula.
Store at 20° to 25°C (68° to 77°F).
Rev: June 2007
EN-1543
Printed in USA
HOSPIRA, INC., LAKE FOREST, IL 60045 USA
Sample Outer Label

| HEPARIN LOCK FLUSH heparin sodium solution |
|||||||||||||
|
|||||||||||||
|
|||||||||||||
|
|||||||||||||
|
|||||||||||||
Labeler – General Injectables & Vaccines, Inc (108250663)
Medical Disclaimer