Generic Name: heparin sodium
Dosage Form: injection, solution
Medically reviewed by Drugs.com. Last updated on February 19, 2021.
- Overview
- Side Effects
- Dosage
- Professional
- Tips
- Interactions
- More
WARNING:
NOT FOR USE IN NEONATES
Description
SOLUTION IS INTENDED FOR MAINTENANCE OF PATENCY OF INTRAVENOUS INJECTION DEVICES ONLY AND IS NOT TO BE USED FOR ANTICOAGULANT THERAPY.
Heparin Lock Flush Solution, USP is a sterile, nonpyrogenic, hypertonic preparation of heparin sodium injection, USP with sodium chloride in water for injection.
Each milliliter (mL) contains: Heparyna sodowa, 10 lub 100 jednostek USP (pochodząca z błony śluzowej jelita świń); chlorek sodu 9 mg; disodu edetynian, bezwodny 0,1 mg dodany jako stabilizator; oraz alkohol benzylowy 9 mg dodany jako środek konserwujący w wodzie do wstrzykiwań. Może zawierać sodu wodorotlenek do dostosowania pH. pH 6,5 (5,0 do 7,5). Stężenia osmolarne tych roztworów wynoszą 392 mOsmol/L (calc). Heparin Lock Flush Solution, USP jest przeznaczony wyłącznie do utrzymywania drożności urządzeń do wstrzyknięć dożylnych i nie może być stosowany w terapii przeciwzakrzepowej.
Heparin Sodium, USP jest heterogeniczną grupą anionowych mukopolisacharydów o prostym łańcuchu, zwanych glikozaminoglikanami o właściwościach przeciwzakrzepowych. Chociaż mogą występować inne, głównymi cukrami występującymi w heparynie są: (1) 2-siarczan kwasu a-L-iduronowego, (2) 6-siarczan 2-deoksy-2-sulfamino-a-D-glukozy, (3) kwas b-D-glukuronowy, (4) 2-acetamido-2-deoksy-a-D-glukoza oraz (5) kwas a-L-iduronowy. Cukry te występują w zmniejszających się ilościach, zwykle w kolejności (2)większej niż (1)większej niż (4)większej niż (3)większej niż (5), i są połączone wiązaniami glikozydowymi, tworząc polimery o różnej wielkości. Heparyna jest silnie kwaśna ze względu na zawartość kowalencyjnie połączonych grup siarczanowych i karboksylowych. W heparynie sodowej kwaśne protony jednostek siarczanowych są częściowo zastąpione przez jony sodowe. Siła działania jest określana za pomocą testu biologicznego z zastosowaniem standardu referencyjnego USP opartego na jednostkach aktywności heparyny na miligram.
Struktura heparyny sodowej (reprezentatywne podjednostki):
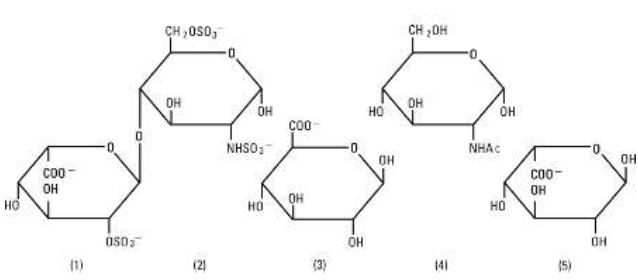
Sodium Chloride, USP jest chemicznie oznaczany jako NaCl, biały krystaliczny związek swobodnie rozpuszczalny w wodzie. Półsztywne fiolki są wykonane ze specjalnie opracowanej poliolefiny. Jest to kopolimer etylenu i propylenu. Bezpieczeństwo tworzywa zostało potwierdzone badaniami na zwierzętach zgodnie z normami biologicznymi USP dla pojemników z tworzyw sztucznych. Pojemnik nie wymaga
bariery parowej do utrzymania odpowiedniego stężenia leku.
Farmakologia kliniczna
Heparyna hamuje reakcje, które prowadzą do krzepnięcia krwi i tworzenia się skrzepów fibrynowych zarówno in vitro, jak i in vivo. Heparyna działa w wielu miejscach w prawidłowym układzie krzepnięcia. Małe ilości heparyny w połączeniu z antytrombiną III (kofaktor heparyny) mogą hamować zakrzepicę poprzez inaktywację aktywowanego czynnika X i hamowanie przekształcania protrombiny w trombinę. Po rozwinięciu się aktywnej zakrzepicy, większe ilości heparyny mogą hamować dalsze krzepnięcie poprzez inaktywację trombiny i zapobieganie przekształcaniu fibrynogenu w fibrynę. Heparyna zapobiega również tworzeniu się stabilnego skrzepu fibrynowego poprzez hamowanie aktywacji czynnika stabilizującego fibrynę. Czas krwawienia jest zwykle niezmieniony przez heparynę. Czas krzepnięcia wydłużają pełne dawki terapeutyczne heparyny; w większości przypadków małe dawki heparyny nie mają na niego wymiernego wpływu. U pacjentów w wieku powyżej 60 lat, po podaniu podobnych dawek heparyny, może wystąpić większe stężenie heparyny w osoczu i dłuższy czas częściowej tromboplastyny po aktywacji (APTT) w porównaniu z pacjentami w wieku poniżej 60 lat. Szczytowe stężenie heparyny w osoczu osiągane jest po 2 do 4 godzinach od podania podskórnego, chociaż istnieją znaczne różnice indywidualne. Wykresy log-liniowe stężenia heparyny w osoczu w funkcji czasu dla szerokiego zakresu dawek są liniowe, co sugeruje brak procesów zerowego rzędu. Miejscem biotransformacji jest wątroba i układ siateczkowo-śródbłonkowy. Dwufazowa krzywa eliminacji, szybko malejąca faza alfa (t½ =10#) i po 40 roku życia wolniejsza faza beta, wskazuje na wchłanianie w narządach. Brak zależności między okresem półtrwania antykoagulantu i stężeniem okresu półtrwania może odzwierciedlać takie czynniki, jak wiązanie heparyny z białkami. Heparyna nie wykazuje aktywności fibrynolitycznej, dlatego nie powoduje rozpadu istniejących zakrzepów. Heparin Lock Flush Solution nie wywołuje ogólnoustrojowego działania przeciwzakrzepowego w pojedynczych dawkach wynoszących 10 lub 100 jednostek USP na mL, gdy jest stosowany do utrzymania drożności urządzeń do wstrzyknięć dożylnych. Może on zakłócać wyniki badań laboratoryjnych próbek krwi pobranych z takich urządzeń, chyba że objętość heparyny-soliny in situ, równa objętości zalewowej cewnika, zostanie odessana i wyrzucona przed pobraniem takich próbek. Izotoniczne stężenia chlorku sodu są odpowiednie do pozajelitowego uzupełniania utraty chlorków, która przewyższa lub jest równa utracie sodu. Stężenia hipotoniczne chlorku sodu są odpowiednie do pozajelitowego podtrzymywania zapotrzebowania na wodę, gdy pożądane są jedynie niewielkie ilości soli.
Chlorek sodu w wodzie dysocjuje, tworząc jony sodu (Na+) i chlorku (Cl-). Sód (Na+) jest głównym kationem płynu zewnątrzkomórkowego i odgrywa dużą rolę w terapii zaburzeń płynowych i elektrolitowych. Chlorek (Cl-) ma integralną rolę w działaniach buforowych, gdy tlen i dwutlenek węgla wymiany występuje w krwinkach czerwonych. Dystrybucja i wydalanie sodu (Na+) są w dużej mierze kontrolowane przez nerki, które utrzymują równowagę pomiędzy pobraniem a wydalaniem. Niewielka objętość płynu i ilość chlorku sodu dostarczona przez Heparin Lock Flush Solution, USP, gdy jest stosowany wyłącznie jako nośnik do utrzymania drożności urządzenia do wstrzykiwań dożylnych, prawdopodobnie nie będzie miała znaczącego wpływu na równowagę płynów i elektrolitów, z wyjątkiem prawdopodobnie bardzo małych niemowląt.
Wskazania i stosowanie
Heparin Lock Flush Solution, USP jest wskazany wyłącznie do utrzymania drożności urządzenia do wstrzykiwań dożylnych. Może być stosowany po pierwszym umieszczeniu urządzenia w żyle, po każdym wstrzyknięciu leku lub po pobraniu krwi do analizy laboratoryjnej. Roztworu nie należy stosować do terapii przeciwzakrzepowej.
Przeciwwskazania
Z uwagi na potencjalną toksyczność alkoholu benzylowego u noworodków, roztworów zawierających alkohol benzylowy nie wolno stosować w tej populacji pacjentów. Preparatów pozajelitowych z alkoholem benzylowym nie należy stosować do wymiany płynów lub chlorku sodu. Sól sodowa heparyny nie powinna być stosowana u pacjentów: Z nadwrażliwością na heparynę; Z niekontrolowanym stanem czynnego krwawienia (patrz OSTRZEŻENIA), z wyjątkiem sytuacji, gdy jest to spowodowane rozsianym wykrzepianiem wewnątrznaczyniowym; Z niemożnością wykonania w wymaganych odstępach czasu odpowiednich testów krzepnięcia krwi, np. czasu krzepnięcia pełnej krwi, czasu częściowej tromboplastyny itp. Zazwyczaj nie ma potrzeby monitorowania działania heparyny w małych dawkach u pacjentów z prawidłowymi parametrami krzepnięcia.
Ostrzeżenia
Alkohol benzylowy, środek konserwujący w wielodawkowych fiolkach preparatu Heparin Lock Flush Solution, USP był związany z toksycznością u noworodków. Zgłaszano, że alkohol benzylowy jest związany z „zespołem gasnącego płodu” u wcześniaków. Dane dotyczące toksyczności innych środków konserwujących w tej grupie wiekowej są niedostępne. Do utrzymania drożności urządzeń do wstrzyknięć dożylnych u noworodków należy stosować roztwór do płukania Heparin Lock Flush Solution, USP, niezawierający konserwantów. Heparin Lock Flush Solution, USP nie jest przeznaczony do stosowania domięśniowego, ogólnoustrojowej antykoagulacji lub wstrzykiwania pozajelitowego.
Nadwrażliwość: Pacjenci z udokumentowaną nadwrażliwością na heparynę powinni otrzymywać lek tylko w sytuacjach wyraźnego zagrożenia życia.
Krwotok: Krwotok może wystąpić praktycznie w każdym miejscu u pacjentów otrzymujących heparynę. Niewyjaśniony spadek hematokrytu, spadek ciśnienia krwi lub jakikolwiek inny niewyjaśniony objaw powinien prowadzić do poważnego rozważenia zdarzenia krwotocznego. Heparyna sodowa powinna być stosowana z zachowaniem szczególnej ostrożności w stanach chorobowych, w których istnieje zwiększone ryzyko krwotoku. Niektóre ze stanów chorobowych, w których istnieje zwiększone ryzyko krwotoku, to:
Sercowo-naczyniowe – podostre bakteryjne zapalenie wsierdzia. Ciężkie nadciśnienie tętnicze.
Chirurgiczne – Podczas i bezpośrednio po (a) nakłuciu kręgosłupa lub znieczuleniu rdzeniowym lub (b) poważnym zabiegu chirurgicznym, zwłaszcza dotyczącym mózgu, rdzenia kręgowego lub oka.
Hematologiczne – Stany związane ze zwiększoną skłonnością do krwawień, takie jak hemofilia, małopłytkowość i niektóre plamice naczyniowe.
Jelitowe – Zmiany wrzodziejące i ciągły drenaż żołądka lub jelita cienkiego.
Pozostałe – Menstruacja, choroby wątroby z upośledzoną hemostazą.
Badanie krzepliwości: Jeśli test krzepnięcia jest nadmiernie wydłużony lub jeśli wystąpi krwotok, należy niezwłocznie przerwać podawanie heparyny sodowej. Roztwory heparyny o stężeniu 10 jednostek heparyny USP/mL mogą zmieniać wyniki badań krzepliwości krwi. Stężenia heparyny większe niż 10 jednostek USP heparyny na litr mogą wpływać na wyniki badań krzepliwości krwi.
Trombocytopenia: U pacjentów otrzymujących heparynę zgłaszano występowanie trombocytopenii z częstością od 0 do 30%. Łagodna małopłytkowość (liczba płytek krwi większa niż 100 000/mm3) może pozostać stabilna lub ulec odwróceniu nawet w przypadku kontynuowania podawania heparyny. Jednakże, małopłytkowość każdego stopnia powinna być ściśle monitorowana. Jeśli liczba małopłytkowości spadnie poniżej 100 000/mm3 lub jeśli wystąpi nawracająca zakrzepica (patrz: Zespół białych skrzepów, PRZECIWWSKAZANIA), należy przerwać stosowanie heparyny. Jeśli kontynuacja leczenia heparyną jest niezbędna, można ostrożnie wznowić podawanie heparyny z innego źródła narządowego. Roztwory zawierające jony sodu należy stosować bardzo ostrożnie, jeśli w ogóle, u pacjentów z zastoinową niewydolnością serca, ciężką niewydolnością nerek oraz w stanach klinicznych, w których występuje obrzęk z zatrzymaniem sodu.
Środki ostrożności
Nie stosować, jeśli roztwór nie jest klarowny, a pojemnik nie jest uszkodzony. Stosować technikę aseptyczną przy jednorazowym lub wielokrotnym podawaniu i pobieraniu leku ze wszystkich pojemników. Ponieważ heparyna sodowa w tym produkcie pochodzi z tkanek zwierzęcych, należy ją stosować ostrożnie u pacjentów z alergią w wywiadzie.
Interferencja z testami laboratoryjnymi
Heparyna zakłóca konkurencyjne metody wiązania białek do oznaczeń stężenia tyroksyny w surowicy, co skutkuje fałszywie podwyższonym poziomem. Heparin Lock Flush Solution może zakłócać analizy laboratoryjne lub zmieniać wyniki badań chemii krwi, takich jak stężenie glukozy, sodu i chlorków w surowicy, badania krzepliwości krwi itp. (Patrz FARMAKOLOGIA KLINICZNA.) Poniższe informacje, które dotyczą stosowania heparyny sodowej jako ogólnoustrojowego leku przeciwzakrzepowego, zamieszczono wyłącznie jako ciekawostkę, ponieważ nie wiadomo, czy mają one zastosowanie w przypadku stosowania leku do blokady heparynowej.
Ogólne:
a. Zespół białego skrzepu:
Zgłaszano, że u pacjentów przyjmujących heparynę może dochodzić do powstawania nowych skrzeplin w związku z małopłytkowością wynikającą z nieodwracalnej agregacji płytek krwi wywołanej przez heparynę, tzw. „zespół białego skrzepu”. Proces ten może prowadzić do ciężkich powikłań zakrzepowo-zatorowych, takich jak martwica skóry, zgorzel kończyn, która może prowadzić do amputacji, zawał serca, zatorowość płucna, udar mózgu, a nawet zgon. Dlatego też należy natychmiast przerwać podawanie heparyny, jeśli u pacjenta wystąpi nowa zakrzepica w połączeniu z małopłytkowością.
b. Oporność na heparynę:
Zwiększona oporność na heparynę jest często spotykana w gorączce, zakrzepicy, zakrzepowym zapaleniu żył, zakażeniach ze skłonnością do zakrzepów, zawale serca, nowotworach i u pacjentów po zabiegach chirurgicznych.
c. Zwiększone ryzyko u pacjentów w podeszłym wieku, zwłaszcza kobiet:
Zgłaszano większą częstość występowania krwawień u pacjentów, zwłaszcza kobiet, w wieku powyżej 60 lat.
Interakcje lekowe:
Ponieważ Heparin Lock Flush Solution, USP jest przeznaczony wyłącznie do stosowania w utrzymaniu drożności urządzeń do wstrzyknięć dożylnych, nie należy dodawać żadnych dodatków do fiolek zawierających wiele dawek.
Oralne antykoagulanty: Heparyna sodowa może wydłużać jednostopniowy czas protrombinowy. Dlatego, gdy heparyna sodowa jest podawana z dikumarolem lub warfaryną sodową, przed pobraniem krwi powinno upłynąć co najmniej 5 godzin od podania ostatniej dawki dożylnej, aby można było uzyskać prawidłowy czas protrombinowy.
Inhibitory płytek krwi: Leki takie jak kwas acetylosalicylowy, dekstran, fenylbutazon, ibuprofen, indometacyna, dipirydamol, hydroksychlorochina i inne, które zakłócają reakcje agregacji płytek krwi (główna hemostatyczna obrona heparynizowanych pacjentów) mogą wywoływać krwawienie i powinny być stosowane z ostrożnością u pacjentów otrzymujących heparynę sodową.
Inne interakcje: Naparstnica, tetracykliny, nikotyna, leki przeciwhistaminowe lub nitrogliceryna podawana dożylnie mogą częściowo przeciwdziałać przeciwzakrzepowemu działaniu heparyny sodowej.
Interakcje lekowe/laboratoryjne:
Hyperaminotransferazemia: Znaczne podwyższenie poziomu aminotransferaz (SGOT i SGPT ) wystąpiło u dużego odsetka pacjentów (i osób zdrowych), którzy otrzymywali heparynę. Ponieważ oznaczenia aminotransferaz są ważne w diagnostyce różnicowej zawału serca, chorób wątroby i zatorów płucnych, wzrosty, które mogą być spowodowane przez leki (takie jak heparyna) powinny być interpretowane z ostrożnością.
Karcynogeneza, mutageneza, upośledzenie płodności:
Nie przeprowadzono długoterminowych badań na zwierzętach w celu oceny potencjału rakotwórczego heparyny. Nie przeprowadzono również badań na zwierzętach dotyczących mutagenezy lub upośledzenia płodności.
Ciąża:
Działanie teratogenne: Kategoria ciążowa C. Nie przeprowadzono badań reprodukcji na zwierzętach z użyciem heparyny sodowej lub chlorku sodu. Nie wiadomo również, czy heparyna sodowa lub chlorek sodu mogą powodować uszkodzenia płodu po podaniu kobiecie w ciąży lub wpływać na zdolność reprodukcji. Heparyna sodowa lub chlorek sodu powinny być podawane kobiecie w ciąży tylko w przypadku zdecydowanej konieczności.
Działanie antyteratogenne: Heparyna nie przekracza bariery łożyskowej.
Matki karmiące:
Heparyna nie jest wydzielana do mleka ludzkiego.
Stosowanie u dzieci:
Bezpieczeństwo i skuteczność u pacjentów pediatrycznych nie zostały ustalone. Nie stosować u noworodków (patrz OSTRZEŻENIA).
Stosowanie u pacjentów geriatrycznych:
Zgłaszano większą częstość występowania krwawień u pacjentów w wieku powyżej 60 lat, zwłaszcza u kobiet (patrz PRZECIWWSKAZANIA, Postanowienia ogólne). Badania kliniczne wskazują, że u tych pacjentów mogą być wskazane mniejsze dawki heparyny (patrz FARMAKOLOGIA KLINICZNA oraz DAWKOWANIE I ADMINISTRACJA).
Działania niepożądane
Mimo że u ludzi nie są znane działania niepożądane po podaniu dożylnym domięśniowym lub podskórnym 0.9% alkoholu benzylowego nie występują u ludzi, badania doświadczalne preparatów pozajelitowych o małej objętości zawierających 0,9% alkohol benzylowy u kilku gatunków zwierząt wykazały, że szacunkowa dawka dożylna do 30 mL może być bezpiecznie podana osobie dorosłej bez działania toksycznego. Podanie szacunkowej dawki 9 mL niemowlęciu o masie ciała 6 kg może potencjalnie wywołać zmiany ciśnienia krwi. Nie wiadomo, czy Heparin Lock Flush Solution powoduje jakiekolwiek niepożądane działania miejscowe lub ogólnoustrojowe. Chociaż istnieje niewielka możliwość wystąpienia reakcji nadwrażliwości w przypadku przedostania się do krążenia bardzo małych, subterapeutycznych ilości roztworu, nie odnotowano takiego przypadku.
Dawkowanie i podawanie
Przed podaniem należy sprawdzić wzrokowo, czy nie ma cząstek stałych i przebarwień, o ile roztwór i pojemnik na to pozwalają. Lekkie przebarwienia nie zmieniają siły działania. (Heparin Lock Flush Solution, USP 10 lub 100 jednostek USP/ml, wstrzykuje się jako pojedynczą dawkę do urządzenia do wstrzykiwań dożylnych, używając objętości roztworu odpowiadającej objętości urządzenia do wkłucia do żyły. Pojedyncza dawka powinna być wstrzyknięta po nakłuciu żyły, jeśli urządzenie do wkłucia nie ma być natychmiast użyte. Po każdym użyciu urządzenia do nakłuwania żył w celu wstrzyknięcia lub infuzji leków lub pobrania próbek krwi, należy wstrzyknąć kolejną dawkę w celu przywrócenia skuteczności blokady heparynowej. Ilość roztworu heparyny jest wystarczająca, aby zapobiec tworzeniu się skrzepów w świetle urządzenia do nakłuwania żył (zwykle nie mieści więcej niż 0,2 do 0,3 mL) przez okres do dwudziestu czterech godzin. Jeśli urządzenie do wkłuć jest używane do podawania leku niekompatybilnego z heparyną, cały zestaw blokady heparynowej należy przepłukać 0,9% chlorkiem sodu (Sodium Chloride Injection, USP) przed i po podaniu leku. Po drugim płukaniu należy wstrzyknąć kolejną dawkę roztworu heparyny, aby przywrócić skuteczność blokady heparynowej. Jeśli urządzenie wewnątrzszpikowe jest używane do wielokrotnego pobierania próbek krwi do analiz laboratoryjnych, a obecność heparyny lub soli fizjologicznej może zakłócić lub zmienić wyniki pożądanych badań krwi, roztwór heparyny do płukania in situ powinien zostać usunięty z urządzenia poprzez aspirację i wyrzucenie 1 mL przed pobraniem pożądanej próbki krwi. (See PRECAUTIONS.)
How Supplied
Heparin Lock Flush Solution, USP is supplied in the following dosage forms:
| List No. | Dosage Form | Heparin Sodium (USP Units/mL) |
Solution Volume (mL) |
| 0409-1151-12 | LifeShield Plastic Multple-dose Fliptop vial |
10 | 10 |
| 0409-1151-70 | Plastic Mutliple- dose Fliptop vial |
10 | 10 |
| 0409-1151-78 | Plastic Mutliple- dose Fliptop vial |
10 | 30 |
| 0409-1152-14 | LifeShield Plastic Multple-dose Fliptop vial |
100 | 30 |
| 0409-1152-70 | Plastic Mutliple- dose Fliptop vial |
100 | 10 |
| 0409-1152-78 | Plastic Mutliple- dose Fliptop vial |
100 | 30 |
All of the above may be used with sharp needles. In addition, the LifeShield® products may be used with the LifeShield® Blunt Cannula.
Store at 20° to 25°C (68° to 77°F).
Rev: June 2007
EN-1543
Printed in USA
HOSPIRA, INC., LAKE FOREST, IL 60045 USA
Sample Outer Label

| HEPARIN LOCK FLUSH heparin sodium solution |
|||||||||||||
|
|||||||||||||
|
|||||||||||||
|
|||||||||||||
|
|||||||||||||
Labeler – General Injectables & Vaccines, Inc (108250663)
Medical Disclaimer